
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Температуры кипения и замерзания растворов (второй закон Рауля)
|
|
|
|
Понижение давления пара над раствором обуславливает изменение температур кипения и замерзания растворов по отношению к чистому растворителю. Жидкость кипит, когда давление ее насыщенного пара становится равным внешнему давлению. Поэтому раствор (вследствие пониженного давления пара) закипает при более высокой, а кристаллизуется при более низкой температуре, чем чистый растворитель.
Согласно 2-му закону Рауля изменение температур кипения и замерзания растворов пропорционально моляльности растворов:
∆tкип=Кэ∙Сm; ∆tзам=Кк∙Сm,
где Кэ –эблуоскопическая («абулио» - кипеть), а Кк – криоскопическая («криос» - холод) константы растворителя. Например, Кэ для воды и бензола соответственно равна 0,52 и 2,57оС, Ккр=1,86 и 5,14оС. Сm-моляльная концентрация.
Для растворов электролитов концентрация частиц возрастает за счет диссоциации молекул на ионы. Вследствие этого изменяются рассмотренные ниже свойства растворов на величину поправочного (изотонического) коэффициента, который обозначается i. Изотонический коэффициент зависит от степени диссоциации α вещества и определяется уравнением i =I+d∙(n-1), где n – число ионов, на которое диссоциирует молекула вещества. Например, для сульфата натрия Na2SO4 n=3: Na2SO4 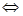 2Na++SO42-. i для растворов неэлектролитов равен I, для электролитов i >I.
2Na++SO42-. i для растворов неэлектролитов равен I, для электролитов i >I.
Поэтому для растворов электролитов законы Вант-Гоффа и Рауля принимают следующий вид:
Росм=iСМRT; ∆Р/P=i∙N; ∆tкип=i∙Кэ∙Сm; ∆tзам=i∙Ккр∙Cm.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 614; Нарушение авторских прав?; Мы поможем в написании вашей работы!