
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример 3. Вычислить молярную массу мочевины, если водный раствор, содержащий 0,3680 г мочевины в 200см3 при 20°С имеет осмотическое давление 74630 Па
|
|
|
|
Пример 2
Пример 1
Вычислить молярную массу мочевины, если водный раствор, содержащий 0,3680 г мочевины в 200см3 при 20°С имеет осмотическое давление 74630 Па.
| M -? | Cu | В данной задаче используется закон Вант – Гоффа.
Мочевина – не электролит Þ используем формулу
π = сRT
с = п/V; п = m/M Þ c = m/(M·V) Þ π = mRT /(M·V) отсюда М = mRT/(π·V)
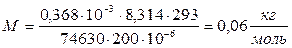
|
| m = 0,368 г V = 200cм3 t = 20°C π = 74630 Па R = 8,314 Дж/(моль×К) | 0,368×10-3 кг 200×10-6 м3 293 К |
Вычислить давление пара раствора, содержащего 8 г нафталина С10Н8 в 100 г бензола при 20°С. Давление пара бензола при данной Т равно 9,99×105 Па.
| Рб -? | Cu | Задача на 1 закон Рауля Рб = Рб° · Хб; Хб = пб/(пб + пн) пб = mб/Мб Мб = 78 × 10-3 кг/моль пн = mн/Мн Мн = 128×10-3 кг/моль |
| mн = 8 г mб = 100 г t = 20°C Pб° = 9,99×105 Па | 8 × 10-3 кг 100 × 10-3 кг |
пн = 8 × 10-3/(128 × 10-3) = 0,062 моль
пб = 100 × 10-3/(78×10-3)= 1,282 моль
Хб = 1,282/(1,282+0,062) = 0,954
Рб = 9,99×105 × 0,954 = 9,529 × 105 Па
Давление пара диэтилового эфира (С2Н5)2О при 20°С равно 58920 Па, а давление пара раствора, содержащего 12,4 г бензойной кислоты в 100 г эфира 54790 Па.
Вычислить молярную массу бензойной кислоты в эфире.
| MК -? | Cu | Для решения задачи используем 1 закон Рауля. Найти ХЭФ найдём и МК Р эф = Р ЭФ °× Х ЭФ. Х ЭФ = Р ЭФ /Р ЭФ °; Х ЭФ = 54790/58920 = 0,93 Х ЭФ = п ЭФ /(m ЭФ + m К ). Необходимо найти п К; так как п К = m К /M К |
| PЭФ° = 58920 Па РЭФ = 54790 Па t = 20°C mК = 12,4 г mЭФ = 100 г MЭФ = 74 × 10-3 кг/моль | 12,4 × 10-3 кг 100 × 10-3 кг |
m ЭФ + m К = n ЭФ /х ЭФ; п К = (п ЭФ /х ЭФ ) - п ЭФ.
п ЭФ = m ЭФ /M ЭФ = 100×10-3/74×10-3 = 1,35
п К = (1,35/0,93) – 1,35 = 1,45 – 1,35 = 0,1 Þ М К= 12,4×10-3/0,1 = 124×10-3 кг/моль
При решении задач на 1 закон Рауля необходимо понять, что для растворов электролитов перед концентрацией или мольной долей используется i = 1 + a(K - 1 ). А также при решении задач можно использовать первую и вторую формулы закона Рауля.
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 4071; Нарушение авторских прав?; Мы поможем в написании вашей работы!