
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вязкость растворов ВМС
|
|
|
|
Термодинамика процесса набухания и растворения ВМС.
Процесс набухания и растворения полимера является самопроизвольным, ∆ G < 0. Рассмотрим влияние энтальпийного и энтропийного факторов на обе стадии самопроизвольного процесса
∆G = ∆H - T∆S
На первой стадии, стадии набухания, энтропия изменяется незначительно,поэтому преобладает энтальпийный фактор. Энтальпия должна уменьшаться.
Энтальпия набухания складывается из двух энтальпий:
∆H наб. = ∆Hкр.+ ∆Hсольв.
∆Hкр.- энтальпия разрушения связей между макромолекулами, процесс эндотермический, ∆H кр > 0.
∆Hсольв – энтальпия сольватации макромолекул. Этот процесс экзотермический, как и любой процесс образования связей. ∆Hсольв. < 0.
Как правило ∆Hсольв.> ∆Hкр., поскольку связи между макромолекулами непрочные, поэтому, процесс набухания экзотермичен.
На стадии растворения преобладает энтропийный фактор. При переходе
Т → Ж система переходит в неупорядоченное состояние, энтропия возрастает, ∆S > 0. Энтальпия при этом остается постоянной, поэтому энергия Гиббса уменьшается за счет энтропийного фактора.
Растворы ВМС имеют более высокую вязкость, чем растворы, низкомолекулярных соединений или золей при одинаковой массовой доле растворенного вещества.
Вязкость (η) – это мера сопротивления среды движению. Это внутреннее трение между слоями движущейся среды.
Высокая вязкость растворов ВМС объясняется большими размерами макромолекул и их анизотропией, т.е. неодинаковостью их свойств по разным направлениям. Макромолекулы пронизывают разные слои движущейся жидкости и увеличивают сопротивление движению, т.е вязкость жидкости (Рис 5.4а)
Зависимость вязкости растворов ВМС от температуры, концентрации, давления, не подчиняется общим закономерностям, характерным для низкомолекулярных жидкостей и их растворов.
Эти отклонения называют аномалиями вязкости растворов ВМС.
1)Обычно с повышением температуры вязкость низкомолекулярных жидкостей уменьшается. А для ВМС характер изменения вязкости с изменением температуры зависит от структуры макромолекул. Для растворов разветвленных полимеров вязкость с ростом температуры уменьшается т.к увеличивается их движение и уменьшается возможность структурирования.
Для линейных полимеров вязкость раствора с ростом температуры возрастает, т.к возрастает интенсивность движения фрагментов молекул.
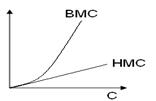
2. Вязкость растворов ВМС уменьшается с увеличением давления, в то время как на вязкость растворов низкомолекулярных соединений (НМС) оно не влияет (рис. 5.3).
|

Рис.5.3 Влияние давления на вязкость растворов ВМС и НМС
Это объясняется тем, что с увеличением давления расположение макромолекул становится более упорядоченным вдоль потока и уменьшается их сопротивление движению среды (рис. 5.4 б).
 | |||||||
 | |||||||
 | |||||||
 | |||||||





 а) б)
а) б)
Рис.5.4 Изменение расположения макромолекул в текущем растворе при увеличении давления
|
|
Макромолекулы не связаны между собой только в разбавленных растворах. При повышении концентрации образуются межмолекулярные связи по местам, не защищенным сольватной оболочкой. Образование таких пространственных сшитых структур повышает вязкость раствора. При увеличении внешнего давления структуры разрушаются, растворитель освобождается и вязкость уменьшается.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 5096; Нарушение авторских прав?; Мы поможем в написании вашей работы!