
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Потенциометрическое титрование
Измерительный стеклянный электрод.
Стекло шарика изготовлено из ион-селективного стекла (литий – барий – силикатное стекло). Это стекло чувствительно к ионам H+ (концентрация H+ внутреннего раствора постоянна). Между внутренней и наружной поверхностью возникает мембранный потенциал, величина которого зависит от концентрации H+, то есть от величины pH наружного раствора. Обычно шкала потенциометра сразу откалибрована в единицах pH.
Перед измерением pH растворов с помощью стеклянных электродов прибор калибруют с помощью буферных растворов с точным значение pH.
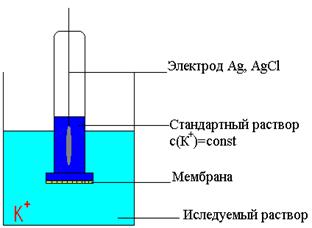 3) Для измерения концентрации других ионов используют ион-селективные электроды, мембрана которых чувствительны только к данному виду ионов.
3) Для измерения концентрации других ионов используют ион-селективные электроды, мембрана которых чувствительны только к данному виду ионов.
Рис.6.6 Ионселективный электрод
Приборы, которые используют для измерения концентраций других ионов, называют иономерами.
Метод потенциометрии используют:
а) для определения pH растворов;
б) для определения концентрации ионов;
в) для потенциометрического титрования – определения точки эквивалентности в титриметрическом анализе.
Это титриметрический метод анализа, в котором точка эквивалентности определяется с помощью прибора по изменению величины рН в ходе титрования анализируемого раствора.
Потенциометрическое титрование осуществляют следующим образом:
Определённый объём анализируемого раствора наливают в стаканчик, опускают в раствор электроды и добавляют из бюретки титрант определёнными порциями, например по 0,2 мл. После каждого добавления и перемешивания раствора измеряют и записывают величину ЭДС или рН. Затем строят кривые потенциометрического титрования.
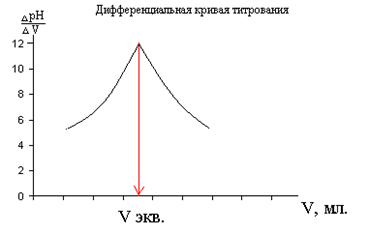
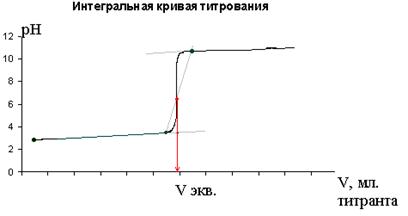
Рис.6.7. Определение точки эквивалентности при потенциометрическом титровании.
Достоинства и возможности потенциометрического титрования.
– Метод позволяет определять содержание сильной и слабой кислот в их смеси (два скачка титрования);
– Позволяют определять константу кислотности (Ка);
– Проводить анализ окрашенных и мутных растворов;
- автоматизировать аналитические определения.
Заключение
После ознакомления со свойствами коллоидных систем, становятся более понятными механизмы явлений, которые осуществляются в коллоидных системах живого организма.
С адсорбции начинаются любые процессы на многочисленных поверхностях раздела фаз в организме: мембранах, нервных и мышечных волокнах, стенках сосудов, кишечника и т.д.
1. Мембранное пищеварение на поверхности слизистой оболочки кишечника, в результате которого происходит гидролитическое расщепление белков, жиров и углеводов, начинается с адсорбции. Слизистая оболочка кишечника имеет многочисленные складки, ворсинки и микроворсинки, увеличивающие поверхность примерно в 500 раз. На поверхности микроворсинок адсорбируются пищеварительные ферменты и пищеварительные субстраты, только потом происходит процесс пищеварения
2. Детоксикация в организме токсичных продуктов пищеварения растительными волокнами (клетчаткой) основан на явлении адсорбции. Как известно, клетчатка (целлюлоза) не усваивается организмом человека из-за отсутствия соответствующих ферментов. Но она является незаменимым компонентом пищи, т.к. адсорбирует токсичные продукты пищеварения, продукты гниения в толстом кишечнике и выводит их из организма.
3. Адсорбция является первоначальным этапом фагоцитоза – обезвреживания бактерий путем переноса их в клетку макрофага.
4. В основе взаимодействия ферментов с субстратами в ходе биохимических реакций лежит процесс хемосорбции.
5. Иммунное взаимодействие антигенов с соответствующими антителами с образованием комплекса «АГ – АТ» также является процессом хемосорбции.
6. Действие некоторых гормонов также осуществляется через стадию адсорбции. Например, некоторые гормоны (адреналин, пептидные) не проникают в клетку, однако активируют ферменты-протеинкиназы, находящиеся внутри клетки. Молекула гормона хемосорбируется на специфическом рецепторе с наружной стороны мембраны, вызывая конформационную перестройку ферментного белка мембраны - аденилатциклазы, который из неактивной формы переходит в активную. В результате этого с внутренней стороны мембраны начинается синтез циклонуклеотида – ц-АМФ из АТФ, а образовавшийся ц-АМФ активирует протеинкиназы.
7. Некоторые белки плазмы крови, обладающие дифильной структурой, являются поверхностно-активными веществами (ПАВ) и обеспечивают постоянное поверхностное натяжение плазмы - около 46·10-3 Дж/м2. Изменение поверхностного натяжения плазмы может вызвать патологическое состояние. Например, при анафилактическом шоке поверхностное натяжение плазмы резко снижается, что приводит к нарушению процесса свертывания крови и проницаемости сосудов.
8. При адсорбции ПАВ на поверхности некоторых клеток может нарушаться и подавляться их жизнедеятельность. На этом основано использование ПАВ в качестве дезинфицирующих средств – детергентов. Наибольшее применение для обработки операционного поля и рук медперсонала находят катионные детергенты (соли четвертичных аминов) – церигель, дегмицид, хлоргексидин, роккал. Своею головкой – катионом они легко адсорбируются на отрицательно заряженной поверхности микроогранизмов и лишают их жизнедеятельности.
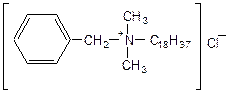 Обычное мыло (стеарат натрия) является анионным ПАВ. Поэтому после мытья рук мылом их следует тщательно ополоснуть водой перед обработкой катионным ПАВ во избежание нейтрализации его заряда.
Обычное мыло (стеарат натрия) является анионным ПАВ. Поэтому после мытья рук мылом их следует тщательно ополоснуть водой перед обработкой катионным ПАВ во избежание нейтрализации его заряда.
Роккал
Коллоидные и микрогетерогенные системы широко представлены в живых организмах. Такой сложной системой является кровь. Её очистка от низкомолекулярных продуктов метаболизма происходит в почечных нефронах по принципу ультрафильтрации с градиентом давления около 2,5 кПа.
1. При заболеваниях почек и острых отравлениях для детоксикации организма используется аппарат «искусственная почка», работающий по принципу диализа. Кровь больного пропускают через систему мембран, изготовленных из синтетического полисульфонового волокна, а в качестве «чистого» растворителя используют изотонический раствор NaCl. Очищенная кровь поступает обратно в организм.
2. При острых отравлениях используют также перитониальный диализ. При этой процедуре в брюшную полость вводится около 2л теплого гипертонического раствора. Роль естественной полупроницаемой мембраны играет брюшина с площадью поверхности около 2м2. Через 20 – 30 минут экспозиции диализный раствор вместе с перешедшими в него примесями удаляют.
4. Коагуляция лежит в основе сложного ферментативного процесса свертывания крови, благодаря которому уменьшаются кровопотери при повреждениях тканей. С другой стороны, свёртывание приводит к образованию тромбов в кровеносных сосудах. Удивительно, но природа предусмотрела одновременное присутствие в крови и антикоагулянта – гепарина.
5. Возможность коагуляции биологических коллоидных систем следует учитывать при инъекции лекарств-электролитов в кровь или мышечную ткань. Электролит следует вводить медленно, чтобы он успевал уноситься с током крови, благодаря чему не достигается пороговая концентрация и не наступает коагуляция.
6. При нарушении коллоидной защиты (белки крови) может происходить коагуляция коллоидных растворов фосфата кальция и холестерина в крови, приводящая к отложению их на внутренней поверхности кровеносных сосудов.
Ответы к тестовым заданиям
Адсорбция
1) 2 8) 2 15) 3
2) 2 9) 3 16) 3
3) 2 10) 2 17) 2
4) 2 11) 2 18) 2
5) 2 12) 1 19) 1,4
6) 3 13) 2 20) 4,5
7) 3 14) 2 21) 1
Коллоидные системы
1) 4 5)6 10) 2
2) А 1,2 6) 4 11) 1,6
Б 3,4 7) 1,4 12) 2
3) 5 8) 4 13) 4
4) 2 9) 4
Растворы коллоидных ПАВ
1) А2, Б4 4) Б 7) 3
В 5 5) 2 8) 1
2) 3 6) 4 9) 2
3) 1
Микрогетерогенные системы
1) 4 9) 3 18) 1
2) 3 10) 3 19) 2
3) 3 11) 2 20) 3
4) 4 12) 1 21) 1
5) 2 13) 1 22) 4
6) 3 14) 3 23) 3
7) 2 15) 1 24) 3
8) А 1,2,3 16) 3 25) 2
Б 4 17) 2 26) 2
Растворы высокомолекулярных соединений
1) 2 10) А 6 16) А 3
2) 3 Б 1 Б 2
3) 1 11) 3 17) 3
4) 2 12) 2 18) 6
5) 2 13) 2 19) 2
6) 2 14) 2,4 20) 3
7) 3 15) А3 21) 3
8) 1 Б 5
9) 3
Список литературы.
1. Общая химия. Биофизическая химия. Химия биогенных элементов. Под ред. Ю. А. Ершова. – М. Высш. школа, 2005.
2. Слесарев В. И. Химия. Основы химии живого. – С. – Пб. Химиздат, 2000.
3. Зимон А. Д. Коллоидная химия. – М., «Агар», 2001.
4. Пузаков С.А., Попков В.А., Филлипов А.А. Сборник задач и упражнений по общей химии. М.; Высшая школа, 2004.
Приложение.
|
|
Дата добавления: 2014-11-20; Просмотров: 975; Нарушение авторских прав?; Мы поможем в написании вашей работы!