
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнение состояния идеального газа
|
|
|
|
Давление смеси газов равно сумме парциальных давлений
При одинаковых давлениях (Р) и температурах (Т) в равных объемах (V) любого газа содержится одинаковое число молекул.
Закон Дальтона (для смеси газов)
Рсм=Р1+Р2+... +РК (7-4)
Парциальное давление - давление, которое оказывал бы данный компонент газа, если бы он один занимал весь объем, предоставленный смеси.
Наиболее простой моделью является модель идеального газа. Это газ, состоящий из точечных материальных частиц с конечной массой, силами взаимодействия между которыми можно пренебречь, и которые сталкиваются между собой по законам соударения упругих шаров. Следовательно, молекулы идеального газа обладают только кинетической энергией, поскольку потенциальной энергией взаимодействия молекул можно пренебречь. Молекулы движутся непрерывно и беспорядочно, следовательно, в среднем скорости молекул газа в разных направлениях одинаковы. Тот факт, что частицы точечные, позволяет считать, что газ занимает весь предоставленный ему объём, то есть, любая молекула в любой момент времени может находиться в любом месте предоставленного объёма.
Уравнение состояния идеального газа или уравнение Менделеева - Клапейрона является обобщением законов идеального газа, открытых экспериментально до создания МКТ.
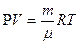 (7-5)
(7-5)
R = 8,3 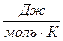 - молярная газовая постоянная или универсальная газовая постоянная.
- молярная газовая постоянная или универсальная газовая постоянная.
Уравнение состояния газа часто удобно использовать в записи, предложенной Клапейроном, если количество вещества не изменяется 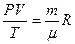 или
или
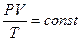 (7-6)
(7-6)
Уравнение (7-6) часто называют обобщённым газовым законом.
|
|
|
|
|
Дата добавления: 2014-12-10; Просмотров: 373; Нарушение авторских прав?; Мы поможем в написании вашей работы!