
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Принцип соответствия. Энергия покоя материального тела
|
|
|
|
При́нцип соотве́тствия — в методологии науки утверждение, что любая новая научная теория при наличии старой, хорошо проверенной теории находится с ней не в полном противоречии, а даёт те же следствия в некотором предельном приближении (частном случае).
В специальной теории относительности в пределе малых скоростей 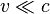 получаются те же следствия, что и в классической механике. Так, преобразования Лоренца переходят в преобразования Галилея, время течёт одинаково во всех системах отсчёта, кинетическая энергия становится равной
получаются те же следствия, что и в классической механике. Так, преобразования Лоренца переходят в преобразования Галилея, время течёт одинаково во всех системах отсчёта, кинетическая энергия становится равной 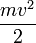 и т.д.
и т.д.
Общая теория относительности даёт те же результаты, что и классическая теория тяготения Ньютона при малых скоростях 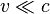 и при малых значениях гравитационного потенциала
и при малых значениях гравитационного потенциала  .
.
Любой массе (движущейся m или покоящейся m0) соответствует определенное значение энергии. Если тело находится в состоянии покоя, то его энергия покоя

Энергия покоя является внутренней энергией тела, которая складывается из кинетических энергий всех частиц, потенциальной энергии их взаимодействия и суммы энергий покоя всех частиц.
20. Уравнение состояния идеального газа (Клапейрона-Менделеева). Изопроцессы и их графическое изображение.
Уравнение состояния идеального газа — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
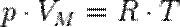 ,
,
где
-
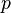 — давление,
— давление, -
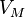 — молярный объём,
— молярный объём, -
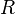 — универсальная газовая постоянная
— универсальная газовая постоянная -
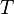 — абсолютная температура, К.
— абсолютная температура, К.
Так как  , где
, где  — количество вещества, а
— количество вещества, а  , где
, где 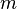 — масса,
— масса, 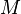 — молярная масса, уравнение состояния можно записать:
— молярная масса, уравнение состояния можно записать:
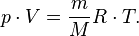
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
Уравнение, выведенное Клапейроном, содержало некую неуниверсальную газовую постоянную  , значение которой необходимо было измерять для каждого газа:
, значение которой необходимо было измерять для каждого газа:
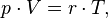
Менделеев же обнаружил, что  прямо пропорциональна
прямо пропорциональна  , коэффициент пропорциональности
, коэффициент пропорциональности 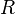 он назвал универсальной газовой постоянной.
он назвал универсальной газовой постоянной.
Изопроцессы — термодинамические процессы, во время которых количество вещества и ещё одна из физических величин — параметров состояния: давление, объём или температура — остаются неизменными. Так, неизменному давлению соответствует изобарный процесс, объёму — изохорный, температуре — изотермический, энтропии — изоэнтропийный (например, обратимый адиабатический процесс). Линии, изображающие данные процессы на какой-либо термодинамической диаграмме, называются изобара, изохора, изотерма и адиабата соответственно. Изопроцессы являются частными случаями политропного процесса.
Изохорный процесс (от греч. хора — занимаемое место) — процесс изменения состояния термодинамической системы при постоянном объёме ( ). Для идеальных газов изохорический процесс описывается законом Шарля: для данной массы газа при постоянном объёме, давление прямо пропорционально температуре:
). Для идеальных газов изохорический процесс описывается законом Шарля: для данной массы газа при постоянном объёме, давление прямо пропорционально температуре:

Линия, изображающая изохорный процесс на диаграмме, называется изохорой.
Изотермический процесс (от греч. «термос» — тёплый, горячий) — процесс изменения состояния термодинамической системы при постоянной температуре ( )(
)(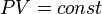 ). Изотермический процесс описывается законом Бойля — Мариотта:
). Изотермический процесс описывается законом Бойля — Мариотта:
При постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV = const.
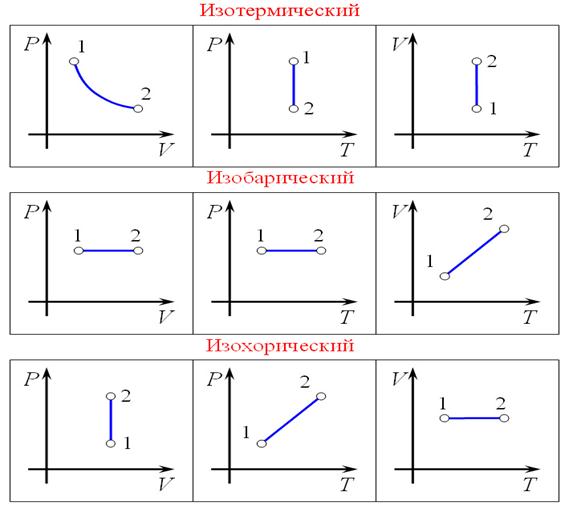
Изоэнтропийный процесс — процесс изменения состояния термодинамической системы при постоянной энтропии (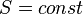 ). Изоэнтропийным является, например, обратимый адиабатический процесс: в таком процессе не происходит теплообмена с окружающей средой. Идеальный газ в таком процессе описывается следующим уравнением:
). Изоэнтропийным является, например, обратимый адиабатический процесс: в таком процессе не происходит теплообмена с окружающей средой. Идеальный газ в таком процессе описывается следующим уравнением:
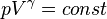
где 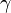 — показатель адиабаты, определяемый типом газа.
— показатель адиабаты, определяемый типом газа.
21. Основные положения МКТ. Вывод уравнения состояния идеального газа.
Основные положения МКТ базируются на ряде опытных данных и наблюдений (диффузия, броуновское движение).
1. Все вещества состоят из атомов или молекул.
2. Атомы всех веществ находятся в беспрестанном хаотическом движении.
3. Атомы (или молекулы) всех веществ взаимодействуют между собой.
Диффузия - явление проникновения молекул одного вещества между молекулами другого при их соприкосновении.
Броуновское движение – хаотическое движение взвешенных в жидкости или газе частиц.
Молекула - мельчайшая частица вещества, обладающая всеми его химическими свойствами.
Уравнение состояния идеального газа (иногда уравнение Клапейрона или уравнение Менделеева — Клапейрона) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
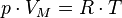 ,
,
где
-
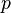 — давление,
— давление, -
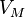 — молярный объём,
— молярный объём, -
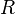 — универсальная газовая постоянная
— универсальная газовая постоянная -
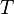 — абсолютная температура, К.
— абсолютная температура, К.
Так как  , где
, где  — количество вещества, а
— количество вещества, а  , где
, где 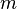 — масса,
— масса, 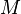 — молярная масса, уравнение состояния можно записать:
— молярная масса, уравнение состояния можно записать:
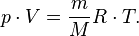
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
Уравнение, выведенное Клапейроном, содержало некую неуниверсальную газовую постоянную  , значение которой необходимо было измерять для каждого газа:
, значение которой необходимо было измерять для каждого газа:
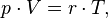
Менделеев же обнаружил, что  прямо пропорциональна
прямо пропорциональна  , коэффициент пропорциональности
, коэффициент пропорциональности 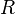 он назвал универсальной газовой постоянной.
он назвал универсальной газовой постоянной.
В случае постоянной массы газа уравнение можно записать в виде:

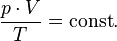
Последнее уравнение называют объединённым газовым законом. Из него получаются законы Бойля — Мариотта, Шарля и Гей-Люссака:
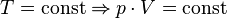 — закон Бойля — Мариотта.
— закон Бойля — Мариотта.
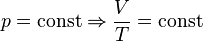 — Закон Гей-Люссака.
— Закон Гей-Люссака.
 — закон Шарля (второй закон Гей-Люссака, 1808 г.)
— закон Шарля (второй закон Гей-Люссака, 1808 г.)
А в форме пропорции 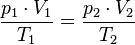 этот закон удобен для расчёта перевода газа из одного состояния в другое.
этот закон удобен для расчёта перевода газа из одного состояния в другое.
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 870; Нарушение авторских прав?; Мы поможем в написании вашей работы!