
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема 12. Электрохимические процессы. Электролиз
|
|
|
|
12-1. Электролизом называется окислительно-восстановительная реакция,
а) при осуществлении которой возникает электрический ток
б) протекающая в растворе при пропускании электрического тока
в) протекающая на электродах при пропускании электрического тока
г) при осуществлении которой в растворе образуются катионы и анионы
12-2. Катод при электролизе
| а) заряжен положительно | в) не имеет заряда |
| б) заряжен отрицательно | г) изменяет знак заряда во время электролиза |
12-3. Анод при электролизе
| а) заряжен положительно | в) не имеет заряда |
| б) заряжен отрицательно | г) изменяет знак заряда во время электролиза |
12-4. Процесс... протекает на катоде при электролизе.
| а) восстановления | в) нейтрализации |
| б) окисления | г) перезарядки |
12-5. Процесс... протекает на аноде при электролизе.
| а) восстановления | в) нейтрализации |
| б) окисления | г) перезарядки |
12-6. Масса вещества, выделяющегося на электроде при электролизе, находится по формуле:
а) 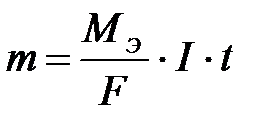
| в) 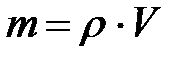
|
б) 
| г) 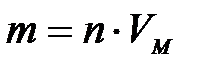
|
12-7. Наиболее вероятный процесс на катоде при электролизе
а) окисление частиц с наименьшим потенциалом
б) восстановление частиц с наименьшим потенциалом
в) окисление частиц с наибольшим потенциалом
г) восстановление частиц с наибольшим потенциалом
12-8. Наиболее вероятный процесс на аноде при электролизе
а) восстановление частиц с наибольшим потенциалом
б) восстановление частиц с наименьшим потенциалом
в) окисление частиц с наибольшим потенциалом
г) окисление частиц с наименьшим потенциалом
12-9. Только молекулы воды восстанавливаются на катоде при электролизе водных растворов, если
а) 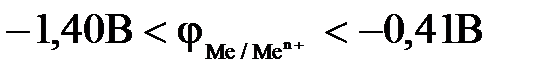
| в) 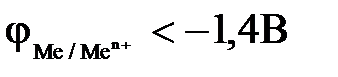
|
б) 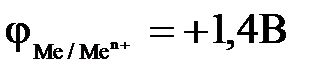
| г) 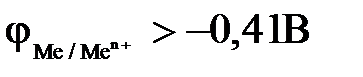
|
12-10. Ионы металла восстанавливаются на катоде при электролизе водных растворов, если
а) 
| в) 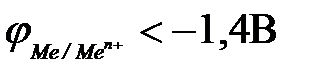
|
б) 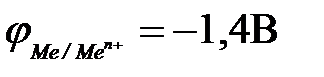
| г) 
|
12-11. Инертный анод при электролизе
| а) цинковый | в) медный |
| б) платиновый | г) хромовый |
12-12. Инертный анод при электролизе
| а) графитовый | в) серебряный |
| б) натриевый | г) никелевый |
12-13. Активный анод при электролизе
| а) графитовый | в) серебряный |
| б) платиновый | г) полиэтиленовый |
12-14. Процесс окисления ___ протекает на графитовом аноде при электролизе водных растворов кислородсодержащих солей.
| а) материала анода | в) кислородсодержащих анионов |
| б) бескислородных анионов | г) молекул воды |
12-15. Процесс окисления ___ протекает на графитовом аноде при электролизе водных растворов бескислородных солей.
| а) материала анода | в) кислородсодержащих анионов |
| б) бескислородных анионов | г) молекул воды |
12-16. Последовательность восстановления катионов металла на катоде:
а) Zn2+ (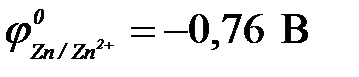 ) )
| в) Cu2+ ( ) )
|
б) Hg2+ (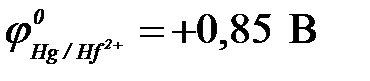 ) )
| г) Au+ ( ) )
|
12-17. Процесс ___ протекает на медном аноде при электролизе раствора CuCl2.
| а) Cu2+ + 2e– = Cu0 | в) Cu0 – 2e– = Cu2+ |
| б) 2H+ + 2e– = H20 | г) Cl2 + 2e– = 2Cl– |
12-18. Восстанавливаться на катоде при электролизе растворов будут ионы
| а) Cu2+ | б) Bi3+ | в) Cl– | г) OH– | д) Ag+ |
12-19. Процесс ___ будет происходить на катоде при электролизе водного раствора Na2SO4 ( ).
).
| а) Na+ + e – = Na0 | в) 2H2O – 4e– = O20+4H+ |
| б) 2H2O + 2e– = H20 + 2OH– | г) 2SO42– – 2e– = S2O82 |
12-20. Последовательность восстановления катионов металла на катоде
а) Cu2+ ( ) )
| в) Pb2+ (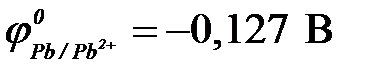 ) )
|
б) Ag+ (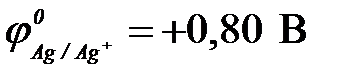 ) )
| г) Ni2+ ( ) )
|
12-21. Процесс ___ протекает на катоде при электролизе раствора NiCl2 (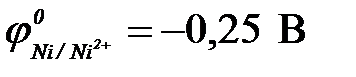 ).
).
| а) Ni2+ + 2e– = Ni0 | в) 2H2O – 4e– = O20 + 4H+ |
| б) 2H2O + 2e– = H20 + 2OH– | г) Ni2+ + 2e– = Ni0 и 2H2O + 2e– = H20 + 2OH– |
12-22. Процесс ___ будет протекать на катоде при электролизе раствора ZnSO4 (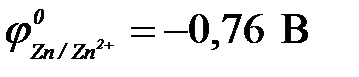 ).
).
| а) Zn2+ + 2e– = Zn0 | в) 2H2O + 2e– = H20 + 2OH– |
| б) 2H2O – 4e– = O20 + 4H+ | г) Zn2+ + 2e– = Zn0 и 2H2O + 2e– = H20 + 2OH– |
12-23. Кислород выделяется на аноде при ___ воды.
| а) окислении | б) восстановлении | в) замещении |
12-24. Продуктами электролиза водного раствора хлорида цинка (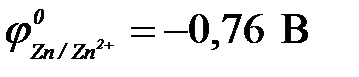 ) с инертными электродами будут
) с инертными электродами будут
| а) цинк и хлор | в) цинк, хлор, водород и гидроксид цинка |
| б) цинк, хлор и кислород | г) гидроксид цинка и хлор |
12-25. Ионы OH– образуются у электрода при электролизе водного раствора соли. Этот электрод называется
| а) катод | в) анод |
| б) металл | г) щелочной электрод |
12-26. Продуктами электролиза с графитовыми электродами водного раствора сульфата меди ( ) будут
) будут
| а) медь | г) медь, кислород и серная кислота |
| б) медь и водород | д) медь, водород, кислород и серная кислота |
| в) медь, водород и кислород |
12-27. Ионы Н+ образуются у электрода при электролизе водного раствора соли. Этот электрод –
| а) катод | в) анод |
| б) металл | г) щелочной электрод |
12-28. Практическая и теоретическая массы вещества, выделившегося на катоде, составляют 48 и 80 г соответственно. Выход по току (в %) равен ___.
_*_ _*_ _*_
12-29. Продуктами, выделяющимися на электродах при электролизе водного раствора хлорида калия, являются
| а) H2 и Cl2 | б) K и Cl2 | в) K и O2 | г) H2 и O2 |
12-30. Уравнение процесса, протекающего на аноде при электролизе водного раствора CaCl2 с графитовыми электродами, имеет вид
| а) Ca+2 + 2e = Ca0 | в) 2Cl– – 2e = Cl2 |
| б) 4OH– –4e = O2 + 2H2O | г) 2H2O – 4e = O2 + 4H+ |
12-31. Уравнение процесса, протекающего на аноде при электролизе водного раствора бромида калия с инертными электродами, имеет вид
| а) 2Br– – 2e = Br2 | в) 2H2O + 2e = H2 + 2OH– |
| б) 4OH– – 4e = O2 + 4H+ | г) 2H2O –4e = O2 + 4H+ |
12-32. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора сульфата меди, являются
| а) Cu и SO2 | б) Cu и O2 | в) H2 и O2 | г) Cu и H2 |
12-33. Уравнение процесса, протекающего на катоде при электролизе водного раствора нитрата серебра с инертными электродами, имеет вид
| а) 2H2O + 2e = H2 + 2OH– | в) 2H+ + 2e = H2 |
| б) Ag+ + e = Ag | г) 2NO3– –2e = 2NO2 + O2 |
12-34. Уравнение процесса, протекающего на катоде при электролизе водного раствора бромида меди, имеет вид
| а) Cu2+ + 2e =Cu0 | в) 2H+ + 2e = H2 |
| б) 2H2O + 2e = H2 + 2OH– | г) 2Br– – 2e = Br2 |
12-35. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора бромида меди, являются
| а) Cu(OH)2 и Br2 | в) Cu и O2 |
| б) H2 и O2 | г) Cu и Br2 |
12-36. Уравнение процесса, протекающего на инертном аноде при электролизе водного раствора хлорида натрия, имеет вид
| а) 2Cl– – 2e = Cl2 | в) O2 + 2H2O + 4e = 4OH– |
| б) 2H2O – 4e = O2 + 4H+ | г) 4OH– – 4e = 4OH |
12-37. Уравнение процесса, протекающего на аноде при электролизе водного раствора йодида калия, имеет вид
| а) 2H2O – 4e = O2 + 4H+ | в) O2 + 2H2O + 4e = 4OH– |
| б) 4OH– – 4e = 4OH | г) 2I– – 2e = I2 |
12-38. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора серной кислоты, являются
| а) H2 и SO2 | в) O2 и SO2 |
| б) H2 и O2 | г) H2 и S |
12-39. Уравнение процесса, протекающего на катоде при электролизе водного раствора йодида калия, имеет вид
| а) K+ + e = K0 | в) O2 + 2H2O + 4e = 4OH– |
| б) 2H2O + 2e = H2 + 2OH– | г) 2H2O – 4e = O2 + 4H+ |
12-40. Продуктами электролиза на инертных электродах при электролизе водного раствора нитрата серебра, являются
| а) Ag и O2 | б) H2 и O2 | в) Ag и NO2 | г) H2 и NO2 |
12-41. Металлом, который можно получить электролизом водного раствора его соли, является
| а) K | б) Na | в) Cu | г) Al |
12-42. Массу вещества, выделившегося или разложившегося в результате электролиза, можно вычислить, используя закон
| а) Вант-Гоффа | в) Фарадея |
| б) Гесса | г) Аррениуса |
12-43. Металлом, который нельзя получить электролизом водного раствора его соли, является
| а) Ag | б) Ni | в) Cu | г) Na |
12-44. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора сульфата натрия, являются
| а) H2 и S | в) H2 и O2 |
| б) Na и O2 | г) Na и SO2 |
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 1422; Нарушение авторских прав?; Мы поможем в написании вашей работы!