
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Розв’язування
|
|
|
|
Приклад розв'язку задачі
Методичні вказівки до розв'язування задачі
Перед розв'язуванням задачі необхідно вивчити відповідний теоретичний матеріал), знаючи фізичну суть параметрів пожежної небезпеки, які підлягають розрахунку.
Уважно прочитати умову задачі і переписати її в зошит. Виписати в стовпчик дані для свого варіанту. Відомі величини підкреслити, під рискою записати, що вимагається визначити. Посередині рядка під умовою задачі записати «Розв’язування», а потім по пунктам послідовно розв’язувати задачу.
Під час розв'язування необхідно показати весь хід розв'язку і математичні перетворення. Проміжні і кінцеві величини, які отриманні під час розв'язування, повинні супроводжуватись одиницями вимірювання. В кінці розв'язку задачі необхідно проаналізувати отриманні результати, щоб виключити нереальні величини, які підлягають визначенню.
Обчислення необхідно проводити до сотих долів числа з розрахунком тепловмісту - до цілого числа.
Під час розв'язування задачі на ЕВМ прикласти програму і роздруківку розв'язку.
Дано:
Г.Р. – етилацетат Vn = 200м3
СНзСООС2Н5 – рідина S випаровування = 3м2
Рн = 104000 Па
tu = 270 С = 300К
a =1,5
G = 1,6 г/м2 . с
Визначити: Vп, Vпг, % склад П.Г., Qн, tгор, Снас, Сст, Рвиб, НКМПП, ВКМПП, НТМПП, ВТМПП, tcп, tвип.
1. Розрахуємо об’єм повітря, який необхідний для згорання 1кг етилацетату:
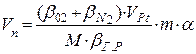 |
де: β02, βN2, βгр – кількість або число кіломолів О2, N2 і горючої речовини за рівнянням реакції горіння етилацетату;
Vpt – об’єм кіломоля будь – якого газу при заданих умовах;
М – молекулярна маса горючої речовини;
m – маса горючого (розрахунок ведеться на 1кг).
Ця формула отримана із аналізу рівняння реакції горіння.
1.1 Складемо рівняння реакції горіння етилацетату на повітрі:
СН3СООС2Н5 + 5О2 + 5 . 3,76N2 = 4CO2 + 4Н2О + 5 . 3,76N2
Звідси β02 = 5;
βN2 = 5 . 3,76
1.2 Визначаємо об’єм газу при заданих умовах
 |
1.3 Визначаємо масу кіломоля етилацетату
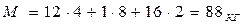 | |||
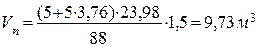 |
1.4
2. Розрахуємо об’єм і процентний склад продуктів горіння 1кг етилацетату:
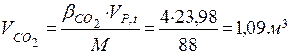 | |||
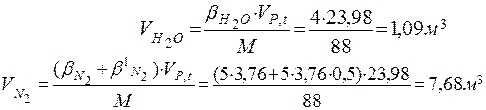 |
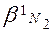 - кількість кіломолів азоту, що знаходяться в надлишку повітря:
- кількість кіломолів азоту, що знаходяться в надлишку повітря:
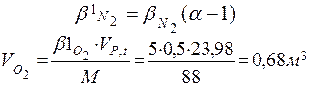 |
β1о2  - кількість кіломолей надлишкового кисню
- кількість кіломолей надлишкового кисню
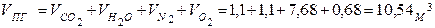 |



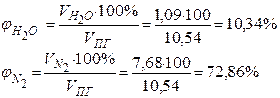 | |||
 |
3. Розрахуємо нижчу теплоту згорання етилацетату за формулою Д.І. Мендєлєєва:
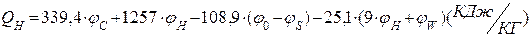 |
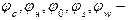 де: відсотковий вміст відповідно карбону, гідрогену, оксигену, сульфуру та вологи горючої речовини.
де: відсотковий вміст відповідно карбону, гідрогену, оксигену, сульфуру та вологи горючої речовини.
3.1 Розрахуємо відсотковий вміст етилацетату, вважаючи молекулярну масу за 100%.
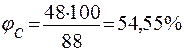 | |||
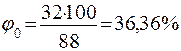 | |||
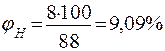 |
Тоді
 | |||
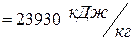 |
4. Розрахуємо температуру горіння етилацетату:
4.1.Визначаємо середній тепловміст одного м3 продуктів горіння
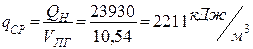 |
4.2 Враховуючи, що продукти горіння в основному (на 72,86%) складаються із азоту, приймаємо tГОР = 15000 С
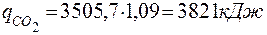 | |||||
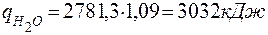 | |||||
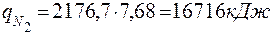 | |||||
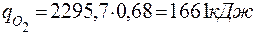 |
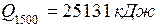
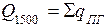 ;
;
4.3 Так як тепловміст продуктів горіння не може перевищувати тепловиділення (Qн), а Q1500 > Qн, приймаємо tГОР = 14000С і розрахунок повторюємо
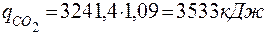 | ||||
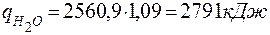 | ||||
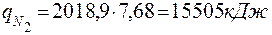 | ||||
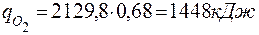 |
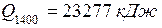
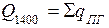 ;
;
4.4 Дійсну температуру горіння знаходимо інтерполяцією, приймаючи тепловміст продуктів горіння у вибраному інтервалі від 14000 С до 15000 С постійною


5. Визначаємо густину пари етилацетату по відношенню до густини повітря:
 |
М – молекулярна маса етилацетату
Mn = 29 – середня маса кіломоля повітря;
тобто пари етилацетату в 3,03 рази важчі за повітря.
6. Розрахуємо концентрацію насиченої пари
6.1 За таблицею або номограмою знаходимо тиск насиченої пари етилацетату при 300 К. Він дорівнює приблизно 1425 Па.
 6.2. Концентрація парів в % за об’ємом складає:
6.2. Концентрація парів в % за об’ємом складає:
6.3.Переведемо об’ємну концентрацію в масову:
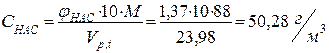 |
7. Розрахуємо стехіометричну концентрацію пари етилацетату в суміші з повітрям, вважаючи об’єм всієї суміші за 100%
7.1.у відсотках за об’ємом
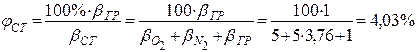 |
7.2. в грамах на м3

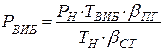 8. Розрахуємо тиск від часу вибуху парів етилацетату на стехіаметричній концентрації при tВИБ = tГОР
8. Розрахуємо тиск від часу вибуху парів етилацетату на стехіаметричній концентрації при tВИБ = tГОР
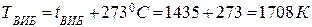 |
де:
 | ||
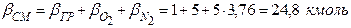 |
βст = βгр + βо2 + βN2 = 1+5+5 ∙ 3,76 = 24,8 кмоль
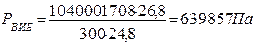 |
9. Розрахуємо концентраційні межі поширення полум’я етилацетату
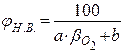 9.1. В об’ємних відсотках:
9.1. В об’ємних відсотках:
де: а і b – табличні дані.
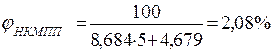 | |||
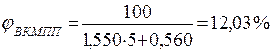 |
9.2. В грамах на м3:
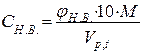 | ||||
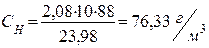 | ||||
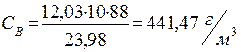 |
10. Розрахуємо температурні межі поширення полум’я речовини
10.1. Визначаємо тиск пари на нижній та верхній концентраційних межах поширення полум’я:
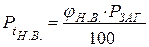

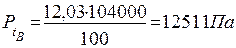
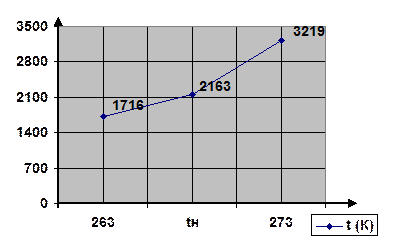
10.2. За таблицею тиску насиченої пари визначаємо температурні межі поширення полум’я етилацетату за значеннями PtH і PtB PtH = 2163 Па
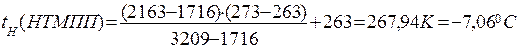
Ptв = 12511 Па
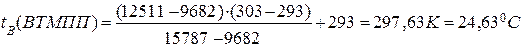
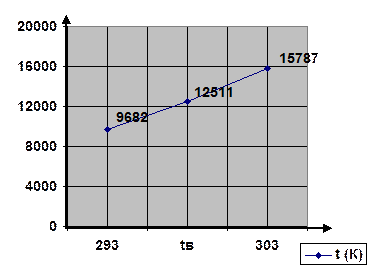
 Примітка: Під час розрахунку НТМПП (або ВТМПП) дві температури з різницею в t 10К вибрані так, щоб при одній із них табличне значення тиску насиченої пари етилацетату було більше за розрахункове РtН при іншій – менше за розрахункове РtН. ТМПП, яку визначають повинна бути у вибраному температурному інтервалі.
Примітка: Під час розрахунку НТМПП (або ВТМПП) дві температури з різницею в t 10К вибрані так, щоб при одній із них табличне значення тиску насиченої пари етилацетату було більше за розрахункове РtН при іншій – менше за розрахункове РtН. ТМПП, яку визначають повинна бути у вибраному температурному інтервалі.
11. Розрахуємо температуру спалаху етилацетату.
11.1. З таблицею 2 знаходимо температуру кипіння етилацетату
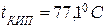 |
11.2. Знаходимо коефіцієнт горючості, виходячи із складу горючої речовини:
K= 4 “С” + 4 “S” + “Н” – 2 “О” – 2 “Cl” – 3 “F” – 5 “Br” + “N”
де: “С”, “S”, “Н”, “О”, “СІ”, “F”, “Br”, “N” – кількість атомів елементів в молекулі горючої речовини.
В етилацетаті: 4 атома С, 8 атомів Н, 2 атома О
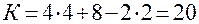
11.3. Знаходимо температуру спалаху за формулою Елея:
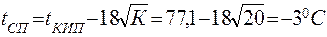 |
Отже, етилацетат відноситься до ЛЗР 2 розряду (постійно небезпечні)
12. Знаходимо час утворення НКМПП парів етилацетату
12.1 Визначаємо масу етилацетату, яку потрібно випаровувати, щоб в приміщенні об’ємом Vп = 200м3 створилась концентрація парів, рівна НКМПП.
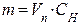 | 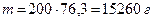 | ||
12.2.Визначаємо час випаровування із формули швидкості випаровування:
 |
з умови задачі S = 3м2;
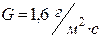 | |||
 |
ВИСНОВОК: для етилацетату при заданих tH = 270С, Рн = 104000 Па,
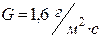 a = 1,5,
a = 1,5,
визначені наступні показники пожежної небезпеки:
1. 
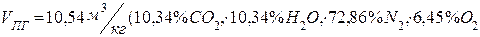 2.
2.
3.  QH = 23930
QH = 23930
4. tГОР = 1435,220С
5. d = 3,03
6. jНАС = 1,37%, СНАС = 50,28 
7. jСТ = 4,08%, ССТ = 147,8 
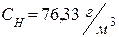 8. РВИБ = 639857 Па
8. РВИБ = 639857 Па
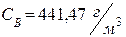 9. jН (НКМПП) = 2,08%,
9. jН (НКМПП) = 2,08%,
jВ (ВКМПП) = 12,03%,
10. tН (НТМПП) = -7,060С
tВ (ВТМПП) = 24,60С
11. tСПАЛ = -30С (ЛЗР 2 розряду)
12. tВИП = 53 хв (при Vп = 200м3, SВИП = 3м2)
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 707; Нарушение авторских прав?; Мы поможем в написании вашей работы!