
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Экспериментальная часть. Дополнительная литература
|
|
|
|
Дополнительная литература
14.2.1. Березин И. В., Савин Ю.В. Основы биохимии. – М.: Изд-во МГУ, 1990. – С. 166 – 210.
14.2.2. Биохимия. Учебник для ВУЗов под ред. Е. С. Северина. – М.: ГЭОТАР-МЕД, 2003. – С. 417 – 432.
14.2.3. Кейтс М. Техника липидологии. – М.: Мир, 1975. – 430 с.
14.2.4.Бергельсон Л., Дятловицкая Э. В., Молотковский Ю. Г. и др. Препаративная биохимия липидов. – М.: Наука, 1981. – 260 с.
14.2.5. Липосомы в биологических системах. Под ред. Г. Грегориадиса и А. Аллисона. – М.: Медицина, 1983. – 384 с.
14.2.6. Введение в биомембранологию. Под ред. А. А. Болдырева. – М.: Изд-во МГУ, 1990. – 208 с.
Уже сказано, что преобладание углеводородных групп в веществах класса липидов сильно ограничивает их растворимость в воде и разнообразие, характерных для них качественных реакций. Поэтому работу с липидами проводят под тягой, извлекая их из образцов экстракцией, с помощью органических растворителей и их смесей: гексана, метиленхлорида, хлороформа, метанола и др. Посуда для работы с ними, должна быть не только чистой, но градуированной, оснащенной притертыми пробками и абсолютно сухой.
В курсе органической химии изучались реакции выявления карбоксильных групп и двойных связей ВЖК, соответственно с помощью титрования щелочами и галогенпроизводными. Наличие и количество фосфатных групп в фосфо- и сфинголипидах, устанавливают по реакции с молибденовокислым аммонием (см. Занятие 12). Поэтому рассмотрим подробней, лишь работу со стеролами, распространенными у всех эукариот. Как и другие липиды, стеролы, не растворимы в воде, но взаимодействуют с нею (1:100 молекул), образуя стойкие непрозрачные эмульсии.
14.3.1. Качественные реакции со стеролами выполняют в вытяжном шкафу, соблюдая правила работы с органикой и концентрированными кислотами.
1) Принцип пробы Сальковского. Под действием концентрированной серной кислоты, ХС дегидратируется в холестерилен, имеющий красную окраску. Его дальнейшая конденсация в бихолестандиен вызывает флуоресценцию в зелёной области спектра, позволяя обнаружить микроколичества (10-7 – 10-9 М/л), например стероидных гормонов в биожидкостях.
Ход работы: 1. Внести в чистую сухую пробирку 0,1-0,2 мл хлороформного экстракта мозга крыс.
2.Осторожно по каплям, добавить такой же объем концентрированной серной кислоты. Перемешать и зарегистрировать окраску.
2) Принцип реакции Либермана – Бурхарда – тот же, что и у предыдущей. Однако, в присутствии уксусного ангидрида, бихолестандиен образует сульфопроизводное зеленого цвета. Эта реакция менее чувствительна (10-4 – 10-6 М/л) и применяется для колориметрических методов определения ХС.
Ход работы: 1. В пробирку с 0,1-0,2 мл хлороформного экстракта мозга крыс добавить 3-5 капель уксусного ангидрида и 2-3 капли концентрированной серной кислоты. Содержимое перемешать и через 5 мин, зарегистрировать развитие окраски.
3) Принцип качественной реакции Петтенкофера на желчные кислоты: В присутствии концентрированной серной кислоты, из фруктозы и ее производных возникает гидроксиметилфурфурол, дающий с желчными кислотами пурпурную окраску.
Ход работы: 1. На дно сухой чашки Петри или часового, но не предметного стекла, нанести одну каплю желчи и каплю 20 % раствора сахарозы.
2. Хорошо перемешать их стеклянной палочкой.
3. Не сдвигая с места чашки/стекла, нанести рядом 3 капли концентрированной серной кислоты.
4. Наблюдать через 1-3 мин., в месте контакта капель, развитие красной окраски, при стоянии переходящей в красно-фиолетовую.
14.3.2. Метод определения общего холестерола в биожидкостях, с помощью тест-набора реагентов «Новохол» (ЗАО «Вектор-Бест»)
Меры предосторожности: При работе с кровью людей, считать ее потенциально инфицированной, а потому быть не только в халате, но, желательно, и в одноразовых перчатках.
Реактивы:
1. Калибровочный раствор холестерола - 4,65 ммоль/л
2. Рабочий раствор – смесь лиофильно высушенных Е и реагентов в 0,01 м растворе фосфатного буфера.
Принцип метода (см. схему на рис. 14.6):
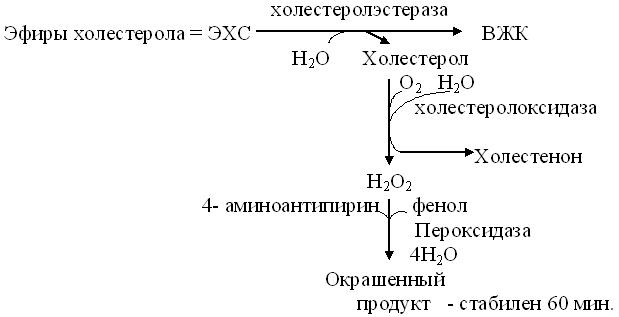
Рис. 14.6. Схема последовательности ферментных реакций метода
Ход работы: 1. В соответствии с таблицей разлить в 2 пробирки:

* - В связи с необходимостью экономии калибровочного раствора холестерола, пробу 2 (калибратор) на группу студентов, выполняет лишь одна рабочая пара.
2. Содержимое пробирок тщательно перемешать и выдержать 10 мин в термостате при 37 С.
3. Против рабочего раствора, в кювете толщиной 10 мм со вкладышем, фотометрировать при λ 490 нм – зеленом светофильтре абсорбцию опытной и калибровочной проб.
Расчет концентрации холестерола в пробе вести по формуле:
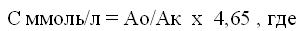
С – концентрация холестерола;
Ао – абсорбция исследуемой пробы;
Ак – абсорбция калибровочной пробы.
Нормальная концентрация холестерола в сыворотке крови – не более 5,2 ммоль/л.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 532; Нарушение авторских прав?; Мы поможем в написании вашей работы!