
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Экспериментальная часть. Дополнительная литература
|
|
|
|
Дополнительная литература
Потребность животных в аминокислотах
(По Р. Марри и др., 1993, с изменениями)
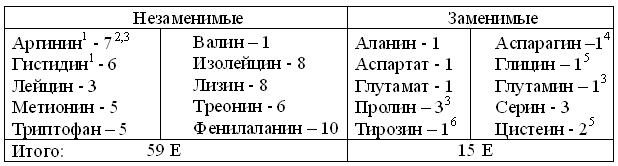
1 – Фактически, эти аминокислоты синтезируются, но со скоростью, недостаточной для обеспечения роста организмов.
2 – Цифры против аминокислот – число ферментов, нужных для их биосинтеза.
3-6 – Синтез аминокислот, соответственно из глутамата, аспартата, серина и фенилаланина.
Таким образом, основными источниками аминокислот для клеток консументов служат: 1) переваривание пищевого белка в ЖКТ; 2) внутриклеточный протеолиз, в т.ч. и убиквитинзависимый; 3) биосинтез заменимых аминокислот из кетокислот и аммиака, источником которого опять-таки, служат аминокислоты пищевых и тканевых белков. С другой стороны, клетки потребляют аминокислоты, прежде всего для: 1. Синтеза белков и пептидов, в т.ч. секреторных. 2. Синтеза заменимых аминокислот и 3. Биосинтеза небелковых азотсодержащих соединений: пуриновых и пиримидиновых оснований, гема и других кофакторов, аминоспиртов, аминосахаров, и ряда других молекул, в т.ч. с функциями гормонов и медиаторов.
16.2.1. Игнатов В. В. Биологическая фиксация азота и азотфиксаторы. //Соросовский образовательный журнал, 1998. – № 9. – С. 28 – 33.
16.2.2. Проворов Н. А. Происхождение и эволюция бобово-ризо-биального симбиоза // Ж. Общ. Биол., 2001. – Т. 62. – С. 472 – 495.
16.2.3. http://www.ksu.ru/conf/botan200/s181.rtf
Собирательным термином небелковые соединения азота обозначают все низкомолекулярные азотсодержащие вещества, остающиеся в центрифугате или фильтрате после осаждения белков из биопробы. Синоним этого понятия в клинической биохимии – «остаточный азот крови», количество которого служит критерием а зотвыделительной функции почек (табл. 16.3). Ряд компонентов остаточного азота: мочевина, креатинин, билирубин имеют самостоятельное диагностическое значение, в связи, с чем определяются с помощью стандартных тест-наборов реактивов.
Таблица 16.3
Компоненты остаточного азота крови

16.3.1. Определение количества мочевины в биожидкостях с помощью тест-набора фирмы Lachema (Чехия)
Мочевина – конечный продукт азотистого обмена у части беспозвоночных, многих позвоночных и большинства млекопитающих. Ее нормальная концентрация в плазме крови указана в таблице 16.3 и зависит от состава и количества пищи, интенсивности распада белков и др. азотистых соединений, обезвреживающей функции печени и азотовыделительной функции почек. Т.о., этот диагностический показатель имеет большое значение для экспериментальных и клинических лабораторий.
Одним из лучших по специфичности, чувствительности и воспроизводимости, является фотометрический метод определения мочевины с диацетилмонооксимом. Он основан на том, что в сильнокислой среде, присутствии ионов трехвалентного железа и тиосемикарбазида, мочевина образует с диацетилмонооксимом комплекс красного цвета, интенсивность окраски которого зависит от ее количества. Внимание!!! Тиосемикарбазид токсичен! При попадании раствора на кожу или в глаза - обильно промыть пораженное место водой. При попадании внутрь - сразу выпить не менее 0,5 л воды и вызвать рвоту. Оказывая первую помощь, пользоваться инструкциями ИОТ-001-05, ИОТ-002-КГУ-06 и немедленно поставить в известность лаборанта и преподавателя!
Ход анализа: 1. В соответствии с п. 3.3.1, с помощью полуавтоматического дозатора, соответственно таблице внести в 3 пробирки следующие растворы:
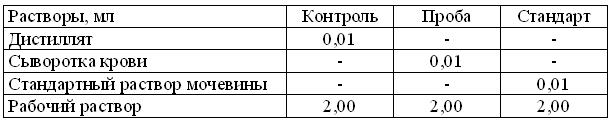
2. Содержимое пробирок перемешать, прикрыть горлышки колпачками из алюминиевой фольги и, выдержать на кипящей водяной бане точно 10 мин!
3. Тут же, хорошо охладить пробирки под краном и, не позже чем через 15 мин., измерить абсорбцию растворов на ФЭКе, при длине волны 540 нм (зеленый светофильтр), в кювете толщиной 10 мм.
4. По формуле: Мочевина, ммоль/л = 16,65 х Аопыта/А стандарта, рассчитать ее концентрацию в исследуемой сыворотке
16.3.2. Определение концентрации креатинина вбиожидкостях с помощью тест-набора фирмы Lahema (Чехия)
Креатинин – ангидрид креатина, содержащийся в крови, мозге и особенно в мышцах, как в форме транспортного макроэрга - креатинфосфата, так и в свободном состоянии. Следы креатина есть в нормальной моче, но в мышцах, он неферментативно и необратимо распадается до креатинина. Эндогенный креатинин экскретируется в почках клубочковой фильтрацией и секрецией в микротрубочках, со скоростью ~ на 20 % больше клиренса инулина.
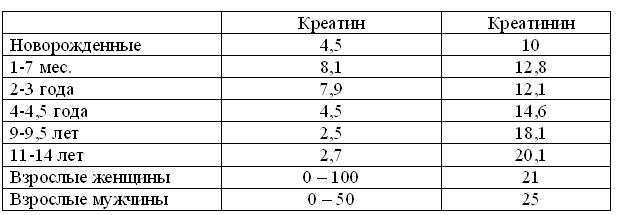
Его суточная экскреция удивительно пропорциональна массе мускулатуры (табл. 16.4) и составляет в моче женщин – 53-97 мкмоль/л и 61-115 мкмоль/л у мужчин.
Таблица 16.4
Возрастные нормы содержания (мг/кг) в суточной моче
(по Murray R.K. et al., 1990)
Обмен этих соединений азота связан с аминокислотой глицином и незаменимыми для консументов, аргинином и метионином (рис. 16.2).
Принцип метода: В щелочной среде креатинин взаимодействует с пикриновой кислотой, давая оранжево-красную окраску (реакция Jaffe), которую измеряют фотометрически. Метод малоспецифичен, т.к. восстановители типа глюкозы, вещества с активной метиленовой группой, кетокислоты, мочевина, мочевая кислота и пигменты: билирубин, Hb – могут завышать результаты. Поэтому определение ведут после осаждения белков биожидкостей.
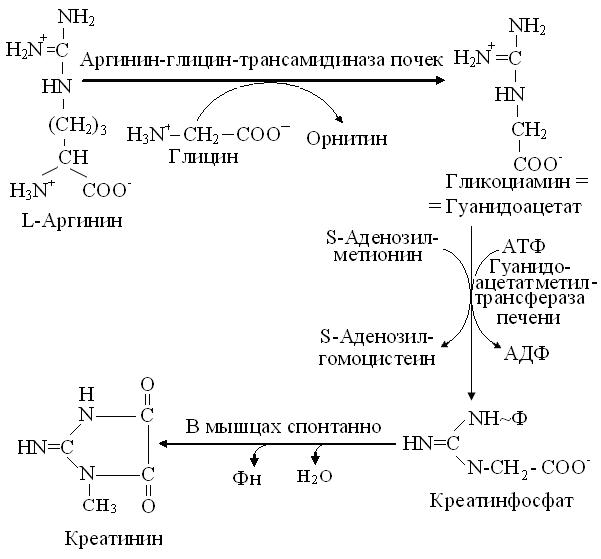
Рис. 16.2. Схема обмена креатина и креатинина
Ход работы: 1. В соответствии с таблицей, внести в 3 пронумерованных центрифужных пробирки:
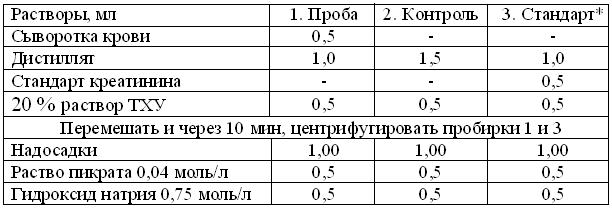
* - В связи с необходимостью экономии стандартного раствора креатинина, пробу 3 – Стандарт, с концентрацией креатинина 177 мкмоль/л и добавкой СА, на группу студентов, выполняет лишь одна рабочая пара.
2. Растворы перемешать и точно через 20 мин фотометрировать при λ 490 нм, в кювете толщиной 10 мм против контроля, абсорбцию пробы и стандарта.
3. По формуле: Креатинин, мкмоль/л = 177 х А опыта/А стандарта,
рассчитать концентрацию креатинина в исследуемой сыворотке.
Нормальное содержание креатинина в плазме крови здоровых людей: 0,7-1,5 мг/дл или 60-132 мкмоль/л. Оно может повышаться при приеме ряда лекарств и острых и хронических воспалительных болезнях почек.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 593; Нарушение авторских прав?; Мы поможем в написании вашей работы!