
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кислотно-основные свойства комплексных соединений
|
|
|
|
При координации молекул воды ионами металла диссоциация воды усиливается, при этом протоны выталкиваются из внутренней сферы аквакомплексов и образуются гидроксокомплексы, а раствор приобретает кислые свойства. Например, в растворах солей алюминия протекают реакции:
[Al(H2O)6]3++ H2O = [Al(H2O)5OH]2+ + H3O+.
По таким схемам происходит гидролиз солей металлов, дающих слабые основания.
Аммиак в водном растворе обладает основными свойствами:
NH3.H2O + H2O = NH4+ + OH- + H2O.
В случае координации аммиака ионами металла в небольшой степени происходит диссоциация его молекулы по кислотному типу:
[Pt(NH3)6]4+ +H2O = [Pt(NH3)5NH2]3+ +H3O+.
Интенсивность кислотных и основных свойств комплексных соединений зависит от размера, заряда и поляризационных свойств центрального иона, от величины заряда комплексного иона, от устойчивости комплекса в растворе, от строения комплекса и характера взаимного влияния координированных групп.
Чем выше заряд центрального иона, тем сильнее выражены кислотные свойства комплекса, а основные слабее. Так, ион [Cr(H2O)6]3+ способен проявлять более сильные кислотные свойства, чем ион [Zn(H2O)6]2+. Ион [Co(NH3)6]3+, содержащий Co3+, почти нейтрален, а ион [Pt(NH3)5Cl]3+, содержащий Pt4+, имеет сильные кислотные свойства. Чем выше заряд комплексного катиона, тем сильнее отталкивается протон и сильнее кислотные свойства. Ион [Cr(Н2О)6]3+ проявляет более сильные кислотные свойства, чем ион [Cr(H2O)4Cl2]+, а ион [Co(NH3)5(H2O)]3+ - более сильные кислотные свойства, чем ион [Co(NH3)4(NO2)(H2O)]2+.
Основные свойства комплексного катиона при увеличении его заряда, наоборот, ослабевают.[Pt(NH3)5OH]3+ проявляет более слабые основные свойства, чем ион [Co(NH3)5OH]2+.
Пример 1. Составьте координационную формулу комплексной соли состава Co(NO3)3 Cl 4NH3, если в растворе этой соли не обнаружены ионы кобальта, нитрата и аммиака. Весь хлор, содержащийся в составе этой соли, образует хлорид серебра при взаимодействии с раствором нитрата серебра. Измерения электрической проводимости показывают, что молекула соли диссоциирует на два иона.
Решение
Так как ионы кобальта и NO3-, а также аммиак не обнаружены в растворе они образуют внутреннюю сферу комплексного соединения. Два иона на которые диссоциирует комплексная соль представляют собой комплексный ион [Co(NH3)4(NO3)2]+ и ион Cl-. Координационная формула соли:
[Co(NH3)4(NO3)2]Cl. Координационное число кобальта равно 6. Степень окисления кобальта (x) равна: x + 0 +(-1)2 = +1 x = +3
Пример 2 Определите тип гибридизации центрального атома в комплексном ионе [Cr(CN)6]3- 
Решение
Cr3+ имеет две свободные 3d –, одну 4s –и три 4р – орбитали, которые они предоставляют для электронных пар лигандов, при этом осуществляется d2sp3- гибридизация.
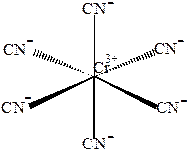
Пример 3 Составьте энергетическую диаграмму образования связей в октаэдрическом комплексе [FeF6]3-,укажите тип гибридизации орбиталей центрального атома.
Решение
Fe+III =[18Ar]3d54s04p04d0 (акцептор). F- - донор. 6 σ–связей.
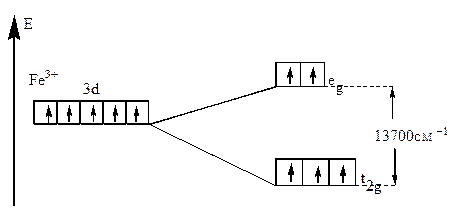
Комплекс высокоспиновый, парамагнитный, лиганд слабого поля - гибридизация sp3d2. Комплекс бесцветный.
Пример 4 Составьте энергетическую диаграмму образования связей в октаэдрическом комплексе
[Fe(CN)6]3-. Укажите тип гибридизации орбиталей центрального атома.
Решение Fe+III =[18Ar]3d54s04p04d0 (акцептор). CN- - донор. 6 σ–связей.
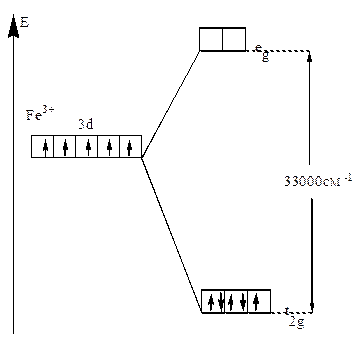
Комплекс низкоспиновый, лиганд сильного поля – гибридизация d2sp3.Комплекс окрашенный.
Пример 5. Определите окраску комплексного иона [Cr(H2O)6]3+, если энергия расщепления
энергетических уровней равна 209,5 кДж/моль.
Решение:
При переходе электронов с t2g – подуровня на eg - подуровень в октаэдрических комплексах поглощается квант света, энергия которого равна энергии расщепления: Δ = hν,
где h- постоянная Планка, h = 6,6 ∙10-34 Дж∙ с, а ν - частота колебаний света в максимуме поглощения. ν = с/ λ, где λ – длина волны максимума поглощения, а с- скорость света
(с = 3,0 109м/с). Энергия электронного перехода Е = Δ/Na.
Тогда: λ = h∙c∙ Na/ Δ = 6,63 ∙10-34 Дж∙ с∙ 3,0∙ 108 м/с ∙ 6,02∙1023 моль-1 ∙109 нм/м / 209500 Дж =571 нм.
Согласно таблице 2 книги «Комплексные соединения» этой длине волны соответствует цвет поглощаемого излучения желто-зеленый, а наблюдаемый (дополнительный) цвет-фиолетовый.
Пример 6. Определите число неспаренных электронов в низкоспиновом комплексе [Fe(CN)6]3+ по следующим экспериментальным данным: молярная магнитная восприимчивость χм = 0,0012.
Решение:

 По величине молярной магнитной восприимчивости вычисляем величину магнитного момента:
По величине молярной магнитной восприимчивости вычисляем величину магнитного момента:
___ ___
μ = 2,84 √ χмТ = 2,84 √ 0,0012·298 = 1,7. магнетонов Бора. Такая величина соответствует одному неспаренному электрону.
Пример 7. Рассчитайте, выпадет ли при 250С осадок сульфида серебра (I), если смешать равные объемы 0,001 М раствора K[Ag(CN)2], содержащего KCN с концентрацией 0,124 моль/л и раствор Na2S с концентрацией 0,004 моль/л. Общая константа устойчивости комплекса равна β2 =1,6 · 107.
ПР(Ag2S) = 7,2 · 10-50.
Решение: Ag + + 2CN- = [Ag(CN)2]-
β2 = [Ag(CN)2]- / [Ag+] ∙ [CN-], Отсюда: [Ag+] = [Ag(CN)2]- / β2 ∙ [CN-]2
Поскольку смешали равные объемы двух растворов, концентрации компонентов уменьшаются в 2 раза. Итак: [Ag+] = 5 ∙10-4 / 1,6 ∙107∙ 0,062 = 5,04 ∙ 10-10
[S2-] = 0,002 моль/л. Произведение [Ag+]2 [S2-] равно:(5,04 ∙10-10) 2 ∙ 0,002 = 5,08 ∙10-23.
Так как 5,08 ∙10-23 > ПР(Ag2S) = 7,2 ∙10-50 осадок выпадет.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 1300; Нарушение авторских прав?; Мы поможем в написании вашей работы!