
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Техника измерения ИК спектра
|
|
|
|
Энергия деформационных колебаний значительно меньше, чем энергия валентных колебаний, поэтому деформационные колебания наблюдаются при больших длинах волн (низких волновых числах).
Установлено, что частота валентных колебаний связана с прочностью соответствующих связей. Чем связь прочнее, тем выше частота колебаний. Так как тройные связи прочнее двойных, а двойные прочнее ординарных, то их частоты закономерно уменьшаются в рядах связей углерод-углерод, углерод-кислород, углерод-азот.
| n C-C | » 1000 см-1 | n С-О | » 1100 см-1 | nC-N | » 1100 см-1 | ||
| n C=C | » 1600 см-1 | n С=О | » 1700 см-1 | nC=N | » 1650 см-1 | ||
| n CºC | » 2200 см-1 | nCºN | » 2250 см-1 |
Если в образовании ординарной связи участвует протон (связи С-Н, О-Н или N-Н), то вследствие его небольшого размера валентные колебания происходят при гораздо большей частоте (2,7—3,8 мкм, 3700— 2640 см-1). Связь О-Н поглощает свет с длиной волны около 2,8 мкм (3570 см-1), а связь О-D при 3,8 мкм (2630 см-1), в этом случае прочность связей почти одинакова, однако масса одного из атомов удвоена.
Частота валентного колебания n связана с массами двух атомов (m1 и m2, г), скоростью света с и силовой постоянной связи F, дин/см следующим образом:
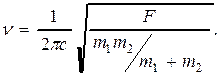
Силовая постоянная F является характеристикой конкретной связи, она зависит, прежде всего от природы атомов, образующих данную связь, а также от кратности связи. Ординарные, двойные и тройные связи имеют силовые постоянные, приблизительно равные 5, 10 и 15×105 дин/см соответственно.
Коэффициент мольной экстинкции в инфракрасной спектроскопии принимает значения от 0 до 2000.Его величина пропорциональна квадрату изменения дипольного момента молекулы, вызываемого данным колебанием.
Наиболее интенсивными в спектре являются пики, отвечающие валентным колебаниям.
| Для получения ИК спектров образец помещают на пути одного из лучей двухлучевого инфракрасного спектрофотометра и измеряют зависимость относительной интенсивности проходящего (а следовательно, и поглощаемого) света от длины волны (или волнового числа). |  Рис. 4. ИК спектрометр FTIR-8400S
фирмы “Shimadzu”
Рис. 4. ИК спектрометр FTIR-8400S
фирмы “Shimadzu”
|
Обычно источником инфракрасного излучения служит штифт Нернста, представляющий собой стержень из сплава окислов циркония, иттрия и эрбия, нагреваемый до 1500 °С. Для получения монохроматического света используют призмы или дифракционные решетки. Последние обладают более высокой разрешающей способностью. Стекло и кварц сильно поглощают во всей области инфракрасного спектра. Поэтому их нельзя использовать для изготовления кювет или призм. Для этих целей обычно применяют галогениды металлов (например, хлористый натрий, бромистый калий). Выпускаемые в настоящее время спектрофотометры снимают полный спектр (2,5 - 25 мкм, 4000 - 400 см-1) в течение нескольких минут.
Можно снимать спектры твердых, жидких или газообразных образцов, а также их растворов. Образец должен быть сухим, так как вода сильно поглощает свет с длиной волны 2,7 мкм (3710 см см-1) и около 6,25 мкм (~1630 см-1). Эти полосы накладываются на спектр исследуемого соединения, затрудняя его интерпретацию.
Для снятия спектра твердого соединения его часто прессуют в таблетку, предварительно добавив галогенид какого-либо щелочного металла. Приблизительно 1 мг вещества и 100 - 200 мг галогенида щелочного металла (обычно бромистого калия) смешивают и тщательно растирают, высушивают, прессуют при нагревании и высоком давлении (не менее 1800 атм). При этом в идеальном случае получается небольшой прозрачный диск примерно 10 мм в диаметре и толщиной 1 - 2 мм, фактически представляющий собой твердый раствор вещества в бромистом калии. Поскольку бромистый калий не поглощает излучение в области 2,5 - 15 мкм, то приготовленная таким образом таблетка позволяет снимать полный спектр образца. Для записи спектров твердых веществ можно использовать также тонкую пленку вещества, которая образуется при испарении его раствора, предварительно нанесенного на пластинку из галогенида щелочного металла. Вещества с низкой температурой плавления можно расплавить на солевой пластинке и снимать спектр застывшей пленки. Кроме того, для получения спектров твердых веществ широко используют их суспензии в вазелиновом масле. Для этого около 5 мг вещества тщательно растирают в агатовой ступке с одной-двумя каплями вазелинового масла, представляющего собой смесь жидких предельных углеводородов, имеющих достаточно большое число углеродных атомов в цепи (С12-С22). После чего образовавшуюся пасту помещают между двумя пластинками (шайбами) бромистого калия и снимают спектр. Вазелиновое масло имеет мало собственных полос поглощения: 3,3 - 3,5 мкм (3030 - 2860 см-1, валентные колебания С-Н), а также 6,8 мкм и 7,3 мкм (1460 см-1 и 1374 см-1, деформационные колебания С-Н) (рис. 5). Однако очевидно, что при использовании суспензии в вазелиновом масле получить данные о поглощении вещества в области указанных частот нельзя.
Полный спектр жидкого вещества, свободный от эффектов растворения, можно получить, исследуя его жидкую пленку. Для этого небольшую каплю жидкости помещают на пластинку (шайбу) из бромистого калия (диаметром около 25 мм и толщиной 5 мм), второй пластинкой из бромистого калия накрывают каплю, пластинки сжимают и снимают спектр.
При съемке спектров газообразных веществ пользуются кюветами длиной от нескольких сантиметров до нескольких метров. Для этого кюветы, представляющие собой стеклянные цилиндрические сосуды с торцами из бромистого калия, заполняют исследуемым веществом.
Часто бывает необходимо снять спектр вещества в растворе. Так как для всех растворителей характерны собственные линии поглощения по меньшей мере в нескольких областях спектра, то для компенсации этих поглощений на пути второго луча устанавливают кювету с растворителем. Чаще всего для снятия спектров в растворе используют кюветы толщиной 0,1 мм. В этом случае, работая с 10 %-ми растворами (20 мг вещества примерно в 0,2 мл растворителя), обычно удается получить удовлетворительные результаты.
Удобными для спектральных целей растворителями являются жидкости, в спектрах которых имеется как можно меньше полос поглощения. В инфракрасной спектроскопии чаще всего используют четыреххлористый углерод и хлороформ, спектры которых представлены нарис. 6, 7.
При использовании одинаковых кювет концентрация растворителя в компенсационной кювете всегда выше, чем в кювете с раствором. В спектре это отражается таким образом, что в области сильного поглощения растворителя пропускание всегда составляет примерно 100 %. При использовании кювет толщиной 0,1 мм и 0,5 мм эффект разности поглощения в двух кюветах не столь ярко выражен. Область спектра, исключаемая растворителем, определяется из спектра чистого растворителя, измеренного при толщине слоя 0,025 мм. Например, для СС14 исключается область 11,9 - 14,3 мкм (834 - 700 см-1). Хлороформ имеет больше полос поглощения, чем четыреххлористый углерод, но он также находит широкое применение, так как лучше растворяет органические соединения.
Вода имеет интенсивные полосы поглощения в ряде областей спектра. Кроме того, она растворяет материалы, из которых обычно изготавливаются кюветы. Поэтому ее редко применяют как растворитель, причем в этом случае применяют кюветы из нерастворимых в воде материалов, пропускающих инфракрасный свет (например, из хлористого серебра).
Часто существует необходимость снять спектр соединения в различных агрегатных состояниях или при различных концентрациях растворов. Так, в твердой фазе или концентрированном растворе ассоциация молекул значительна. В то же время в очень разбавленных растворах или газовой фазе влияние ассоциации сведено к минимуму. Это дает возможность исследовать водородные связи в веществе. Например, в спектрах поглощения растворов спиртов свободные (неассоциированные) гидроксильные группы ОН характеризуются узкими полосами переменной интенсивности при 2,77 мкм (3610 см-1). В спектрах же спиртов, снятых в виде жидкой пленки, полоса поглощения гидроксильной группы уширена и смещена к 3,03 мкм (3300 см-1) за счет образования водородных связей. Относительные интенсивности этих полос поглощения изменяются при разбавлении раствора инертным растворителем.
Аналогичные закономерности наблюдаются в ИК спектрах фенолов и карбоновых кислот (водородные связи О-Н…О-Н), а также первичных и вторичных аминов (водородные связи N-Н…N-Н).
В общем случае водородные связи обычно уменьшают частоты валентных колебаний и увеличивают частоты деформационных колебаний.
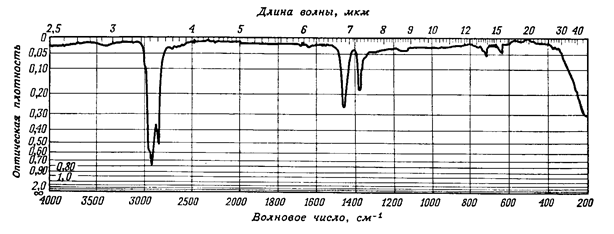 |
Рис. 5. ИК спектр вазелинового масла
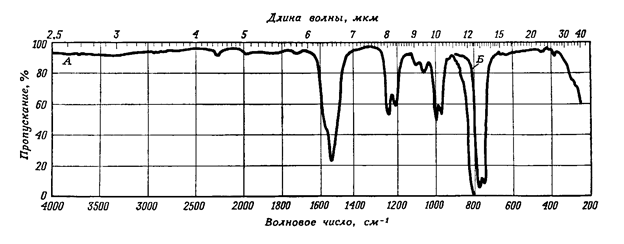 |
Рис. 6. ИК спектр хлороформа (кривая А записана при большем
усилении, чем кривая Б)
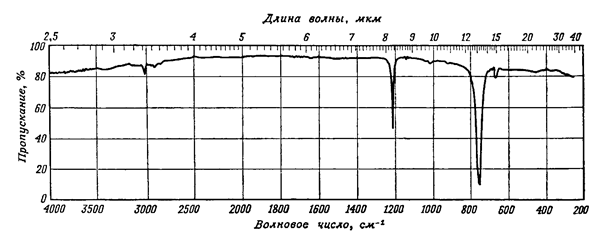 |
Рис. 7. ИК спектр четыреххлористого углерода
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 3255; Нарушение авторских прав?; Мы поможем в написании вашей работы!