
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакции с участием водородного атома ОН - группы
|
|
|
|
Химические свойства
Устойчив к действию окислителей
При обычных условиях не обесцвечивает раствор КMnO4 и Br2 - воду.
3. Реакции замещения (электрофильное)
катализатор поляризует молекулу
1) Нитрование [смесь НNO3(к) и H2SO4(к)]
С6Н6 + НNO3 ® С6Н5NO2 + H2O
2) Галогенирование tо, kat FeCl3 (FeBr3), AlCl3
С6Н6 + Br2 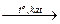 С6Н5Br + HBr
С6Н5Br + HBr
Предельные одноатомные спирты
СnH2n+1ОН или R-OH
Органические вещества, молекулы которых содержат функциональную гидроксильную группу – ОН, соединенную с углеводородным радикалом.
Номенклатура название алкана + ол
СН3-СН2-ОН этанол (этиловый спирт)
а) с активными металлами
2R-OH + 2Na → 2R-ONa + H2↑
б) с органическими кислотами (этерификации)
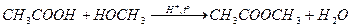
сложный эфир
2. Реакции с участием ОН-группы и Н-атома соседнего
или ближайшего углерода
а) окисление (KMnO4, K2Cr2O7 + H2SO4, O2 + kat)
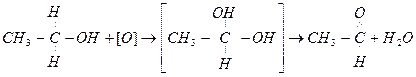
б) дегидратация
(То > 140oC) (То < 140oC)

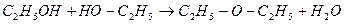
диэтиловый эфир
Предельные многоатомные спирты содержат в молекуле несколько гидроксильных групп.
Таблица 6.5. Предельные многоатомные спирты
| Простейшие | двух | Трехатомных | |||
| Представители | 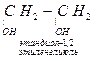
| спиртов | 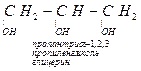
| ||
Простые эфиры
Простые эфиры – органические соединения состава R-O-R’, где R и R’ – одинаковые или различные углеводородные радикалы.
Номенклатура: Углеводородные радикалы +«эфир». Если R одинаковы, то приставка ди-, если разные – начинать название с простейшего.
СН3-О-С2Н5 С2Н5-О-С2Н5
метилэтиловый эфир диэтиловый эфир
Химические свойства -менее реакционоспособны, чем спирты.
Не разлагаются ни водой, ни щелочами.
Характерная реакция – с йодоводородной кислотой (конц.)
С2Н5-О-С2Н5 + НJ → С2Н5J + С2Н5OH
Фенолы
Фенолы – гидроксильные производные ароматических углеводородов, в молекулах которых функциональные группы связаны с бензольным ядром.
 С6Н5ОН фенол
С6Н5ОН фенол
С6Н5× – радикал «фенил»
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 688; Нарушение авторских прав?; Мы поможем в написании вашей работы!