
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет стандартного потенциала полуреакции, получаемой сочетанием полуреакции окисления (восстановления) и реакции протонирования
|
|
|
|
Окисленная и восстановленная форма часто являются слабыми основаниями или кислотами, поэтому наряду с реакцией окисления - восстановления протекают реакции протонирования и депротонирования. Пусть окисленная форма участвует в кислотно-основной реакции. Тогда полуреакцию
НОх + ne ↔ Red + Н+
можно представить сочетанием реакций нротонирования и восстановления
Ох + Н+ ↔ НОх
Ох + ne ↔ Red
Равновесие первой реакции характеризуется константой кислотности НОх:

Выразим а Ox из константы кислотности
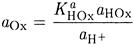
и подставим в уравнение Нернста для полуреакции Ох + ne ↔ Red

Если активности всех участников реакции равны единице, последнее слагаемое равно нулю и
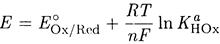
Оба слагаемых являются константами; их сумма и есть стандартный потенциал полуреакции
НОх + ne ↔ Red + Н+
Итак,
 (5-8)
(5-8)
Аналогичным образом можно вывести выражение для расчета стандартного потенциала полуреакции, в которой протонируется восстановленная форма
 (5-9)
(5-9)
И, наконец, если протонируется и окисленная, и восстановленная формы, то
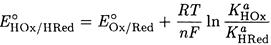 (5-10)
(5-10)
ПРИМЕР 8. Рассчитайте стандартный потенциал полуреакции
HNO2 + Н+ + е ↔ NО + Н2O
из величин Е°(NO2-/NO) = 1.202 В и K a (HNO2) = 6.2·10-4
Решение. Протонируется окисленная форма, поэтому используем формулу (5-8)
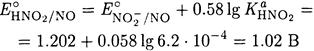
ПРИМЕР 9. Рассчитайте стандартный потенциал полуреакции
H2AsO4- + 2е + 3Н+ ↔ HAsO2 + 2Н2О
из величин Е°(HAsO42-/AsO2-) = 0.609 В, K a (HAsO3) = 1.15·10-7 и K a (HAsO2) = 5.0·10-10.
Решение. Протонируется и окисленная, и восстановленная формы, поэтому используем формулу (5-10)
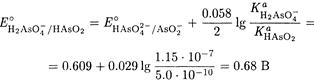
|
|
|
|
|
Дата добавления: 2015-01-03; Просмотров: 2029; Нарушение авторских прав?; Мы поможем в написании вашей работы!