
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
И восстановителей
|
|
|
|
Вычисление молярных масс эквивалентов окислителей
При вычисления молярных масс эквивалентов окислителей и восстановителей исходят из числа электронов, которые присоединяет или отдает в данной реакции один моль вещества. Для нахождения молярной массы эквивалента окислителя (восстановителя) нужно его молярную массу разделить на число принятых (отданных) электронов в данной полуреакции.
Например, в реакции окисления сульфата железа (II) перманганатом калия в кислой среде:
2 KMnO4 + 10 FeSO4 + 8 H2SO4 = 2 MnSO4 + 5 Fe2(SO4)3 + K2SO4 + 8 H2O
1 êMnO4- + 8 H+ + 5 e ® Mn2+ + 4 H2O
5 ê Fe2+ - e à Fe3+
ион MnO4- как окислитель принимает пять электронов, а ион Fe2+ как восстановитель отдает один электрон. Поэтому для расчета молярных масс эквивалентов окислителя и восстановителя их молярные массы следует разделить на пять и на один, соответственно.
MЭ(KMnO4) = 
МЭ(FeSO4) = 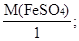 MЭ(Fe2+) = M(Fe2+) = 55,85 г/моль
MЭ(Fe2+) = M(Fe2+) = 55,85 г/моль
В реакции окисления сульфита натрия перманганатом калия в нейтральной среде:
2 KMnO4 + 3 Na2SO3 + H2O = 2 MnO2 + 3 Na2SO4 + 2 KOH
2 êMnO4- + 2 H2O + 3 e à MnO2 + 4 OH-
3 êSO32- + 2 OH- + 2 e à SO42- + H2O
ион MnO4- принимает только три электрона, а ион восстановителя SO32- отдает два электрона, следовательно:
MЭ(KMnO4) = 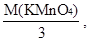 MЭ(Na2SO3) =
MЭ(Na2SO3) = 
Из приведенных примеров видно, что молярные массы эквивалентов окислителей и восстановителей зависят от условий проведения реакций и определяются исходя из соответствующих полуреакций.
|
|
|
|
|
Дата добавления: 2015-01-03; Просмотров: 566; Нарушение авторских прав?; Мы поможем в написании вашей работы!