
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Жесткости воды
|
|
|
|
ОПРЕДЕЛЕНИЕ БИКАРБОНАТНОЙ (ВРЕМЕННОЙ)
Определение жесткости воды имеет большое практическое значение и очень широко применяется в технике и промышленности.
Жесткость воды возникает в результате растворения в ней солей кальция и магния. В зависимости от состава солей различают временную (бикарбонатную) и постоянную жесткость. Жесткость воды выражается числом миллимолей растворимых солей кальция и магния в 1 литре воды (ммоль/л).
Бикарбонатная (временная) жесткость обусловлена присутствием в воде бикарбонатов кальция и магния: Ca(HCO3)2 и Mg(HCO3)2. Она почти полностью устраняется при кипячении воды, так как растворимые бикарбонаты при этом разлагаются с образованием нерастворимых карбонатов кальция и магния и гидроксокарбонатов магния:
Сa(HCO3)2 ® ¯CaCO3 + CO2 + H2O
Mg(HCO3)2 ® ¯MgCO3 + CO2 + H2O
2 Mg(HCO3)2 ® ¯(MgOH)2CO3 + 3 CO2 + H2O
Постоянная жесткость воды обусловлена присутствием в ней преимущественно сульфатов и хлоридов кальция и магния и при кипячении не устраняется.
Сумма величин временной и постоянной жесткости составляет общую жесткость воды: Жобщ.(Н2О) = Жвр. + Жпост.
Существуют различные способы определения жесткости воды: определение временной жесткости с помощью метода нейтрализации; комплексонометрический метод определения общей жесткости.
Бикарбонатная жесткость воды определяется титрованием воды раствором соляной кислоты в присутствии метилового оранжевого, так как рН в точке эквивалентности находится в области перехода окраски этого индикатора.
Сa(HCO3)2 + 2 HCl ® CaCl2 + 2 H2CO3
Mg(HCO3)2 + 2 HCl ® MgCl2 + 2 H2CO3
До начала титрования рН раствора бикарбонатов кальция и магния больше 7 за счет гидролиза солей с участием аниона слабой кислоты. В точке эквивалентности раствор имеет слабокислую реакцию, обусловленную диссоциацией слабой угольной кислоты:
Н2СО3 D НСО3- + Н+
Порядок выполнения работы
1. Отберите в коническую колбу пипеткой 100 мл исследуемой водопроводной воды или 10 мл приготовленной жесткой воды и добавьте 2-3 капли метилоранжа.
2. Оттитруйте воду рабочим раствором HCl до оранжевой окраски индикатора. Титрование повторите до получения сходящихся результатов. Результаты титрования запишите в таблицу (см. образец в лаб. раб 1).
3.Вычислите молярную концентрацию эквивалента солей Ca2+ и Mg2+ в воде:
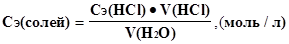
4. Вычислите временную жесткость воды:
Жвр.(Н2О) = СЭ(солей) · 1000,(ммоль/л)
5. Вычислите относительную ошибку определения Жвр.
Лабораторная работа № 3
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ЩЕЛОЧИ И СОДЫ В РАСТВОРЕ ПРИ СОВМЕСТНОМ ИХ ПРИСУТСТВИИ
Как известно, щелочи поглощают из воздуха СО2, превращаясь в соответствующие карбонаты:
2 NaOH + CO2 ® Na2CO3 + H2O
Поэтому раствор щелочи всегда содержит примеси карбонатов. В некоторых случаях необходимо знать содержание щелочи и карбоната в растворе. В данной лабораторной работе в качестве примера рассмотрим определение содержания NaOH и Na2CO3 при совместном их присутствии.
Взаимодействие смеси NaOH и Na2CO3 с сильной кислотой можно рассматривать как три процесса:
NaOH + HCl ® NaCl + H2O (I)
Na2CO3 + HCl ® NaHCO3 + NaCl (II)
NaHCO3 + HCl ® NaCl + CO2 + H2O (III)
Определение щелочи и соды при их совместном присутствии проводят с двумя индикаторами: фенолфталеином и метилоранжем. При титровании с фенолфталеином (V1) пройдут процессы I и II, точка эквивалентности будет находится в щелочной среде (из-за процесса гидролиза бикарбоната), т.е. с фенолфталеином оттитровывается вся щелочь и половина соды. Точка эквивалентности процесса III будет находится в кислой среде, поэтому он может быть проведен при титровании с метилоранжем. Эти определения ведут последовательно, не дополняя бюретку кислотой. Точка эквивалентности по метиловому оранжевому показывает конец титрования всей смеси (V2).
Количество кислоты, которое вступило в реакцию с ионом НСО3- равно (V2 - V1), следовательно:
V (HCl/CO32-) = 2(V2 - V1)
Количество кислоты, эквивалентное щелочи, равно:
V (HCl/NaOH) = V2 - 2(V2 - V1)
Порядок выполнения работы
1. Получите контрольную смесь NaOH и Na2CO3 в мерной колбе на 100 мл и добавьте дистиллированной воды до метки. Перемешайте раствор.
2. Ополосните и заполните бюретку приготовленной Вами соляной кислотой (не забудьте заполнить конец бюретки).
3. Ополосните пипетку контрольным раствором и отмерьте точный объем исследуемого раствора. Перенесите раствор в колбу для титрования. Добавьте 20-30 мл дистиллированной воды и 5-6 капель фенолфталеина.
4. Оттитруйте смесь соляной кислотой до исчезновения розовой окраски фенолфталеина. Запишите объем кислоты (V1).
5. В колбу для титрования добавьте 2-3 капли метилоранжа. Раствор окрасится в желтый цвет. Продолжите титрование (кислоту в бюретку не доливать) до оранжевой окраски раствора. Запишите объем кислоты (V2).
6. Титрование повторите несколько раз до получения сходящихся результатов.
7. Вычислите молярную концентрацию эквивалентов, титр и массу для соды и щелочи в отдельности по приведенным ранее формулам.
8. Рассчитайте относительную ошибку определения по каждому веществу.
|
|
|
|
|
Дата добавления: 2015-01-03; Просмотров: 1016; Нарушение авторских прав?; Мы поможем в написании вашей работы!