
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Види термодинамічних процесів
|
|
|
|
1. Політропним процесом називають такий термодинамічний процес, закономірностями якого узагальнюється велика група окремих термодинамічних змін стану робочих тіл (існують процеси, що не є політропними). Найпростіша теорія цих процесів стосується термодинамічних змін стану ідеальних ґазів.
2. Під політропним процесом розуміють такий термодинамічний процес ідеального ґазу, який описується рівнянням:
pvn = const, (3.1)
де n – стала величина – показник політропи, значення якої визначає особливости даного процесу: – ∞ < n < +∞.
Частинні випадки політропних процесів:
а) n = 0 pv 0 = const, p = const, v/Т = const – ізобарний процес;
б) n = 1 pv 1 = const, pv = const, Т = const – ізотермний процес;
в) n = k (де k – показник адіабати) pv k = const – адіабатний процес, коли ззовні не підводиться тепло Q або не відводиться від системи Q = 0:
· pv k = const;
· pv=RT 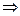 р=
р= 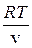
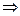
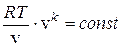 , Тvk – 1 = const";
, Тvk – 1 = const";
· pv=RT 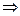 v=
v= 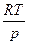 →pvk=const:
→pvk=const:  →
→
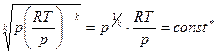 , Tp 1/к-1 = const"', k = Cp / Сv,
, Tp 1/к-1 = const"', k = Cp / Сv,
де Cp – ізобарна теплоємність; CV – ізохорна теплоємність.
Сумарне тепло складається із зовнішнього тепла Q і внутрішнього Qвн.:
QΣ = Q + Qвн. (3.2)
· Якщо Q = 0, Qвн. = 0, то QΣ = 0 і при цьому S = const, то такий адіабатний процес називають оборотнім і, разом з тим, оборотнім ізоентропним.
· Якщо Q = 0, Qвн. ≠ 0, то QΣ ≠ 0 і при цьому S ≠ const, то такий адіабатний процес носить назву необоротнього.
г) Якщо n → ± ∞ 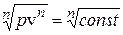 , p1/ n v = const';
, p1/ n v = const';
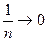 p0 v = v= const,
p0 v = v= const, 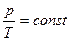 – ізохорний процес.
– ізохорний процес.
ґ) Якщо u=const, то процес ізодинамічний; для ідеального ґазу ізодинамічний процес є оборотнім і, разом з тим, оборотнім ізотермним тому, що для ідеального ґазу u = uК (T).
д) Якщо h=const, то процес ізоентальпний; для ідеального ґазу ізоентальпний процес є оборотнім і, разом з тим, оборотнім ізотермним тому, що для ідеального ґазу h = hК (T).
е) Для проміжних процесів показник політропи може набирати будь-яких значень в межах (– ∞, ∞).
Таким чином, політропний процес є узагальненим, а перераховані вище процеси є його частинними випадками.
3. Показник політропи має певний енергетичний смисл: продиференціюємо рівняння pvn = const, отримаємо
p nvn-1dv + vndp=0; vn-1(npdv + vdp)=0, звідки
npdv + vdp = 0.
Звідки
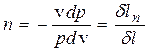 , (3.3)
, (3.3)
тобто величина показника політропи виражає собою відношення корисної роботи (роботи переміщення) до термодинамічної роботи в даному процесі.
|
|
|
|
|
Дата добавления: 2014-12-25; Просмотров: 876; Нарушение авторских прав?; Мы поможем в написании вашей работы!