
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Количественное определение
|
|
|
|
Фиолетовая окраска
Реакции подлинности
Количественное определение.
Растворите 80,0 мг препарата, осторожно перемешивая, в предварительно охлажденной до 20оС смеси серной кислоты (10 г) и 90 мл воды. Оттитровать 0,02 моль/л раствором калия перманганатом до слабо розового окрашивания.
1 мл 0,02 моль/лраствора калия перманганата эквивалентен 2,815 мг MgO2.
Хранение. В защищенном от света месте.
Гидроперит/ Hydroperit
OC(NH2)2.H2O2 Мr 94,07
Гидроперит представляет собой эквимолярную смесь мочевины и пероксида водорода. Содержание перекиси водорода составляет около 35 %. Применяется в виде таблеток (Тabulettae Нуdroperiti) по 1,5 г в упаковке по 6 штук. Одна таблетка гидроперита массой 1,5 г соответствует 15 мл 3% раствора пероксида водорода. При растворении таблетки в стакане воды получают 0,25% раствор пероксида водорода.
А. Реакции на пероксид водорода

Б. Мочевину в гидроперите определяют по биуретовой реакции:

Содержание пероксида водорода в таблетках гидроперита устанавливают методом йодометрического титрования (заместительное титрование):
2KI + H2O2 + H2SO4 ® I2 + K2SO4 + 2H2О
I2 + 2Nа2S2O3 ® 2 NaI + Na2S4O6
Титрант – 0,1 моль/л раствор натрия тиосульфата. Индикатор – крахмал. Титруют до исчезновения синего окрашивания.
Хранение. В сухом, защищенном от света месте, в хорошо закрытой таре при температуре не выше + 20 0С.
Тиосульфат натрия/ Natrii thiosulfas
Na2S2O3,5H2O Mr 248.2
Содержание действующего вещества составляет от 99.0 % до 101.0 % Na2S2O3,5H2O
Натрия тиосульфат– соль, образованная катионом натрия и анионом тиосерной кислоты:
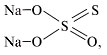
Сера в тиосульфат-ионе находится в разной степени окисления: (+4 и 0). Поэтому окислительно-восстановительные превращения тиосульфат-иона весьма разнообразны и используются в фармацевтическом анализе.
В водном растворе натрия тиосульфат гидролизуется по аниону:
S2O32- + H2O «HS2O3- + OH-
На воздухе препарат разлагается:
2Na2S2O3 + O2 (воздух) = 2Na2SO4 + 2S
Натрия тиосульфат применяют как антидот при отравлениях тяжелыми металлами и цианидами. Его применяют также в качестве десенсибилизирующего (предупреждающего или ослабляющего проявления аллергии), а также как противопаразитарное средство. При лечении чесотки втирают 60 % раствор в кожу туловища и конечностей и после высыхания смачивают 6 % раствором соляной кислоты (по прописи Демьяновича). Гибель чесоточного клеща и его яиц обусловлена акарицидным действием серы и сернистого ангидрида:
Na2S2O3 + 2НСI ® SO2 + S¯ + 2NaCl + H2O
|
|
|
|
|
Дата добавления: 2014-12-26; Просмотров: 4688; Нарушение авторских прав?; Мы поможем в написании вашей работы!