
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Природные a-аминокислоты
|
|
|
|
| Тривиальное название | Обозначение; (рН i) | Формула |
| Глицин | Gly; (6,0) | CH2(NH2)–COOH |
| Аланин | Ala; (6,0) | СН3–CH(NH2)–COOH |
| Валин* | Val; (6,0) | (СН3)2СН –CH(NH2)–COOH |
| Лейцин* | Leu; (6,0) | (СН3)2СН–СН2–CH(NH2)–COOH |
| Изолейцин* | Ile; (6,0) | СН3СН2(СН3)СН–CH(NH2)–COOH |
| Аспарагиновая кислота | Asp; (3,0) | НООС–СН2–CH(NH2)–COOH |
| Глютаминовая кислота | Glu; (3,2) | НООС–СН2СН2–CH(NH2)–COOH |
| Аспарагин | Asn; (5,4) | NH2ОС–СН2–CH(NH2)–COOH |
| Глютамин | Gln; (5,7) | NH2ОС–CH2CH2–CH(NH2)–COOH |
| Лизин* | Lys; (9,7) | NH2–(CH2)4–CH(NH2)–COOH |
| Аргинин* | Arg; (10,8) | 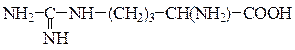
|
| Цистеин* | Cys; (5,0) | SH–CH2–CH(NH2)–COOH |
| Метионин* | Met; (5,7) | H3CS–CH2CH2–CH(NH2)–COOH |
| Серин | Ser; (5,7) | НО–CH2–CH(NH2)–COOH |
| Треонин* | Thr; (5,6) | CH3–CHOH–CH(NH2)–COOH |
| Фенилаланин* | Phe; (5,5) | С6Н5–СН2–CH(NH2)–COOH |
| Тирозин | Tyr; (5,7) | 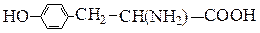
|
| Триптофан* | Trp; (5,9) | 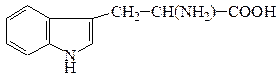
|
| Гистидин | His; (7,6) | 
|
| Пролин | Pro; (6,3) | 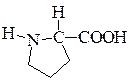
|
* Незаменимые аминокислоты.
Индивидуальные задания
Задача 34
Дайте определение понятию «основность» органического соединения. Расположите вещества А, Б и В (табл. 54) в порядке возрастания их основных свойств. Дайте необходимые пояснения. Приведите формулы и классификацию представленных в задании аминов (например, вторичный алифатическо-ароматический амин). Для наиболее слабого основания напишите уравнение солеобразования с H2SO4.
Таблица 54
| Вариант | А | Б | В |
| анилин | 2,4-диброманилин | метиламин | |
| метилфениламин | дифениламин | анилин | |
| пропиламин | диэтиламин | 2-метиланилин | |
| диметиламин | диметилфениламин | 4-хлоранилин | |
| втор- бутиламин | 4-метиланилин | 4-нитроанилин | |
| 2,4-динитроанилин | триэтиламин | 4-метиланилин | |
| 2-броманилин | метилпропиламин | N-этиланилин | |
| изобутиламин | 4-нитроанилин | анилин | |
| метилпропиламин | N,N-диэтиланилин | бутиламин | |
| дифениламин | 4-аминофенол | этиламин | |
| 2-аминобензойная кислота | 2-метиланилин | пропиламин | |
| метилпропиламин | трет- бутиламин | 3-броманилин | |
| N,N-диэтиланилин | триэтиламин | анилин | |
| пропилфениламин | втор- бутиламин | диметиламин | |
| трифениламин | метилфениламин | дифениламин | |
| 4-броманилин | пара- толуидин | бутан-2-амин | |
| триэтиламин | 3-иоданилин | бутиламин | |
| 2-аминофенол | трет- бутиламин | 3-броманилин | |
| 4-нитроанилин | орто- толуидин | дипропиламин | |
| анилин | изопропиламин | дифениламин | |
| N-пропиланилин | дипропиламин | этиламин | |
| трет- бутиламин | триэтиламин | анилин | |
| 2-хлоранилин | анилин | изобутиламин |
Окончание табл. 54
| Вариант | А | Б | В |
| 4-аминобензойная кислота | N-метиланилин | анилин | |
| 2-метиланилин | метилпропиламин | изобутиламин | |
| метилфениламин | дифениламин | диметиламин | |
| трифениламин | 2-аминофенол | 4-хлоранилин | |
| диметилэтиламин | 4-нитроанилин | анилин | |
| бутил втор- бутиламин | N,N-диэтиланилин | бутиламин | |
| N-пропиланилин | изопропиламин | диметиламин |
Задача 35
Напишите уравнения реакций соединений А и Б с соответствующими реагентами, указанными в табл. 55. Назовите, по возможности, конечные продукты реакций.
Таблица 55
| Вариант | Соединения | Реагенты |
| А) пропиламин Б) тирозин | А) CH3COCl; HNO2; H2O Б) T > Tпл; CuO; KOH | |
| А) 4-метиланилин Б) b-аланин | А) HNO2; С2Н5I; Br2, H2O Б) T > Tпл; NaHCO3; H2SO4 | |
| А) N,N-диметиланилин Б) глицин | А) HNO2; Br2, H2O; HCl Б) декарбоксилаза; СН3ОН, НÅ; T > Tпл | |
| А) дифениламин Б) 4-аминопентановая кислота | A) CH3COCl; H2SO4; СН3I Б) T > Tпл; HNO2; NaОH | |
| А) трет- бутиламин Б) валин | А) С2Н5I; HNO2; H2O Б) CuO; HCl; CH3COCl | |
| А) 2-хлоранилин Б) цистеин | А) Br2, H2O; С3Н7I; (CH3CO)2О Б) KOH; H2SO4; HNO2; | |
| А) диметиламин Б) 2-аминобензойная кислота | А) HNO2; С2Н5I; HCl Б) HNO3; HNO2 + b-нафтол; NaHCO3 | |
| А) N-пропиланилин Б) a-аланин | А) CH3COCl; HNO2; Br2, H2O Б) CuO; декарбоксилаза; H2SO4 | |
| А) 2-метиланилин Б) a-фенилаланин | А) HNO2 + b-нафтол; Br2, H2O; CH3COCl; Б) декарбоксилаза; HNO3; KOH | |
| А) бутиламин Б) триптофан | А) 2 С3Н7I; (CH3CO)2О; H2SO4 Б) 3 СН3I; СН3ОН, НÅ; NaHCO3 |
Продолжение табл. 55
| Вариант | Соединения | Реагенты |
| А) изопропиламин Б) глутаминовая кислота | А) HCl; HNO2; CH3COCl Б) a-декарбоксилаза; T > Tпл; PСl5 | |
| А) N-этиланилин Б) аспарагиновая кислота | А) HNO2; С2Н5I; Br2, H2O Б) 2СН3ОН, НÅ; (CH3CO)2О; b-декарбоксилаза | |
| А) метилэтиламин Б) 4-аминобензойная кислота | А) СН3I; HNO2; HCl Б) HNO2 + b-нафтол; HNO3; С3Н7ОН, НÅ | |
| А) 4-броманилин Б) лизин | А) HNO2 + b-нафтол; Br2, H2O; (CH3CO)2О Б) HNO2; NaОH; С2Н5I (изб.) | |
| А) втор- бутиламин Б) b-фенилаланин | А) HNO2; (CH3CO)2О; H2SO4 Б) T > Tпл; NH3, t, °C; HCl | |
| А) этиламин Б) тирозин | А) 3 СН3I; HNO2; H2O Б) HNO3; PСl5; CH3COCl | |
| А) N-пропиланилин Б) d-аминовалерьяновая кислота | А) HNO2; Br2, H2O; CH3COCl Б) T > Tпл; HNO2; NaHCO3 | |
| А) дипропиламин Б) 3-аминобензойная кислота | А) CH3COCl; HNO2; H2O Б) Br2, H2O; HNO2 + b-нафтол; NH3, t, °C | |
| А) пентан-2-амин Б) глицин | А) (CH3CO)2О; HNO2; 2 СН3I Б) С2Н5ОН, НÅ; декарбоксилаза; CuO | |
| А)2,4,6-трихлоранилин Б) изолейцин | А) HNO2 + b-нафтол; H2SO4; CH3COCl Б) CuO; T > Tпл; 3 С2Н5I | |
| А) 4-метиланилин Б) лейцин | А) HNO2 + b-нафтол; Br2, H2O; С2Н5I Б) HNO2; PСl5; T > Tпл | |
| А) дипропиламин Б) a-фенилаланин | А) HNO2; H2SO4; СН3I Б) CuO; HNO3; С4Н9ОН, НÅ | |
| А) N,N-диметиланилин Б) b-аланин | А) HNO2; Br2, H2O; HCl Б) T > Tпл; KOH; NH3, t, °C | |
| А) бутиламин Б) 4-аминобензойная кислота | А) 2 СН3I; HNO2; НСООН Б) HNO2 + фенол; HNO3; CH3CН2ОН, НÅ | |
| А) N-метиланилин Б) валин | А) HNO2; (CH3CO)2О; Br2, H2O Б)NaHCO3; CuO; 3 СН3I | |
| А) втор- бутиламин Б) триптофан | А) 2 С2Н5I; HNO2; СН3СООН Б) KOH; HCl; СН3ОН, НÅ |
Окончание табл. 55
| Вариант | Соединения | Реагенты |
| А) изобутиламин Б) b-фенилаланин | А) H2SO4; HNO2; CH3COCl Б) T > Tпл; PСl5; СН3I | |
| А) изопропиламин Б) аспарагиновая кислота | А) HNO2; НСООН; 3 СН3I Б) NH3, t °C; HNO2; a-декарбоксилаза | |
| А) N-пропиланилин Б) g-аминовалерьяновая кислота | А) HNO2; CH3COCl; HCl Б) T > Tпл; HNO2; NH3, t, °C | |
| А) дифениламин Б) a-аланин | А) HNO2; CH3COCl; H2SO4 Б) CuO; CH3CН2ОН, НÅ; HNO2 |
Задача 36
С помощью качественных реакций отличите между собой три вещества А, Б и В (табл. 56). Составьте план экспе-
римента в виде табл. 46. Запишите уравнения использованных реакций, опишите наблюдаемый результат.
Таблица 56
| Вариант | А | Б | В |
| 2-метиланилин | триптофан | цистеин | |
| 4-аминобензойная кислота | глицин | этандиамин | |
| a-аланин | анилин | d-аминовалерьяновая кислота | |
| N,N-диметиланилин | тирозин | бутиламин | |
| глутаминовая кислота | лейцин | N-пропиланилин | |
| 2-аминобензойная кислота | бутиламин | 4-метиланилин | |
| тирозин | анилин | b-аланин | |
| 2-метиланилин | a-фенилаланин | диэтиламин | |
| аспарагиновая кислота | глицин | 4-броманилин | |
| N-метиланилин | цистеин | валин | |
| a-фенилаланин | анилин | глицин | |
| N,N-диметиланилин | 4-метиланилин | 2-аминобензойная кислота | |
| 2-метиланилин | пропиламин | тирозин | |
| гексаметилендиамин | a-аланин | дипропиламин | |
| 4-аминобензойная кислота | a-фенилаланин | цистеин | |
| N-пропиланилин | анилин | 4-аминобензойная кислота |
Окончание табл. 56
| Вариант | А | Б | В |
| триптофан | 4-метиланилин | бутиламин | |
| N,N-диметиланилин | глицин | дифениламин | |
| дипропиламин | тирозин | цистеин | |
| изопропиламин | a-фенилаланин | 2-аминобензойная кислота | |
| N-метиланилин | цистеин | g-аминобутановая кислота | |
| 2-аминобензойная кислота | анилин | b-фенилаланин | |
| цистеин | 3-метиланилин | глицин | |
| диэтиламин | b-аланин | глутаминовая кислота | |
| N,N-диметиланилин | 2-метиланилин | 4-аминобензойная кислота | |
| лейцин | дифениламин | анилин | |
| 2-аминобензойная кислота | N-метиланилин | дипропиламин | |
| 4-броманилин | a-фенилаланин | 3-аминобензойная кислота | |
| a-аланин | пропиламин | дифениламин | |
| b-фенилаланин | 3-метиланилин | тирозин |
Задача 37
Установите строение соединения с молекулярной формулой А, которое соответствует приведенному в табл. 57 описанию. Обоснуйте выбор структурной формулы, сделав вывод по каждому из пунктов описания свойств. Напишите все упомянутые в условии уравнения реакций, назовите установленное вещество.
Таблица 57
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С8H11N | а) существует в виде энантиомеров; б) легко растворяется в HCl; в) алкилируется и ацилируется; г) с азотистой кислотой при 0-5 °С образует вещество состава С8Н10О, окисление которого хромовой смесью приводит к бензойной кислоте |
Продолжение табл. 57
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С3Н7NО2 | а) дает соли как с минеральными кислотами, так и со щелочами; б) при взаимодействии с PCl5 с последующим подщелачиванием образует вещество состава С3Н6ClNO; в) с нингидрином дает фиолетовое окрашивание; г) при нагревании до температуры выше Тпл превращается в вещество состава С6Н10N2О2 | |
| C5H13N | а) обладает оптической активностью; б) в водном растворе имеет рН > 7; в) ацилируется и алкилируется; г) с азотистой кислотой при 0-5 °С моментально выделяет азот с образованием спирта, который при дегидратации образует пент-2-ен | |
| С7Н7NО2 | а) проявляет амфотерные свойства; б) не образует комплекс синего цвета с CuO; в) при взаимодействии с азотистой кислотой образует соль диазония, которая при добавлении b-нафтола дает азокраситель красного цвета; г) с бромной водой образует дибромпроизводное; д) не способно к образованию внутримолекулярной водородной связи | |
| С4Н11N | а) легко растворяется в воде и кислотах; б) алкилируется, но не ацилируется; в) в сильнокислой среде не реагирует с азотистой кислотой; г) получается по реакции Гофмана из этиламина и иодметана | |
| С5Н11NО2 | а) образует соли с NaOH и с HCl; б) с этанолом в кислой среде образует вещество состава С7Н15NО2; в) при нагревании выше Тпл выделяет аммиак с образованием органического соединения, которое при жестком окислении дает смесь щавелевой кислоты и пропанона |
Продолжение табл. 57
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С7Н9N | а) обладает основными свойствами; б) алкилируется и ацилируется; в) при взаимодействии с азотистой кислотой образует соль диазония, которая при добавлении b-нафтола дает азокраситель красного цвета; г) с бромной водой дает белый осадок, молекулярная формула которого С7Н6Br3N | |
| С5Н11NО2 | а) может существовать в виде двух оптических изомеров (энантиомеров); б) образует соли с KOH и H2SO4; в) не дает биуретовую и нингидриновую реакции; г) в реакции с азотистой кислотой при 0-5 °С выделяется газ; д) при нагревании выше Тпл образует вещество состава С5Н9NO | |
| C8H11N | а) образует соли с минеральными кислотами; б) алкилируется; в) не способно ацилироваться по атому N; г) обесцвечивает бромную воду с образованием светлого осадка; д) в реакции с NaNO2 + HCl при 0-5 °С вначале образует вещество желто-оранжевого цвета, которое после нейтрализации Na2CO3 переходит в соединение состава C8H10N2O зеленого цвета | |
| С4Н7NО4 | а) образует соли с кислотами и щелочами; б) горячий водный раствор имеет рН < 4; в) в реакции с азотистой кислотой выделяет газ; г) при нагревании выше Тпл одновременно выделяет аммиак, воду и образует непредельную (фумаровую) кислоту и циклический дипептид (дикетопиперазин) | |
| С12Н11N | а) способно медленно растворяться в концентрированной H2SO4; б) алкилируется и ацилируется; в) с азотистой кислотой образует соединение состава С12Н10N2О |
Продолжение табл. 57
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| C9H11 NO3 | а) растворяется в растворах HCl, NaOH и NaHCO3; б) образует комплекс синего цвета с CuO; в) дает положительную ксантопротеиновую реакцию (HNO3); г) в реакции с азотистой кислотой при 0-5 °С выделяется газ; д) дает цветную реакцию с FeCl3 | |
| C7H9N | а) не обладает оптической активностью; б) растворяется в минеральных кислотах; в) алкилируется и ацилируется; г) с бромной водой дает светлый осадок трибромпроизводного; д) в реакции с азотистой кислотой реагирует по N-атому с образованием желтого вещества состава C7H8N2О | |
| С9Н11NО2 | а) образует соли с кислотами и основаниями; б) не дает цветную реакцию с нингидрином; в) дает положительную ксантопротеиновую реакцию (HNO3); г) в реакции с азотистой кислотой при 0-5 °С выделяется газ; д) при нагревании выше Тпл выделяет аммиак с образованием коричной кислоты | |
| C5H13N | а) не может существовать в виде энантиомеров; б) образует соли с кислотами; в) ацилируется и алкилируется; г) с азотистой кислотой при 0–5 °С моментально выделяет азот с образованием вторичного спирта | |
| С5Н11NО2 | а) не может существовать в виде энантиомеров; б) образует соли с NaHCO3 и HCl; в) не образует комплекс синего цвета с CuO; г) в реакции с азотистой кислотой при 0-5 °С выделяется газ; д) при нагревании выше Тпл образует вещество состава С5Н9NO |
Продолжение табл. 57
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| C9H13N | а) растворяется в минеральных кислотах; б) алкилируется и ацилируется; в) не реагирует с бромной водой; г) в реакции с азотистой кислотой при 0-5 °С образует соль диазония, которая при нагревании превращается в фенол с тривиальным названием «мезитол» | |
| C3H7NO2S | а) входит в состав белков; б) образует соли с KOH, H2SO4 и CuO; в) в реакции с азотистой кислотой при 0-5 °С выделяется газ; г) в реакции Фоля (NaOH, t, °С, затем (CH3COO)2Pb) образует черный осадок | |
| С8Н11N | а) дает соли с минеральными кислотами; б) не реагирует с бромной водой; в) с азотистой кислотой при 0-5 °С моментально выделяет азот с образованием первичного спирта. г) при жестком окислении KMnO4, H2SO4, t, °С образует терефталевую кислоту (1,4-бензолдикарбоновую) | |
| С6Н14N2O2 | а) существует в виде энантиомеров; б) имеет неразветвленный углеродный скелет; в) входит в состав белков; г) водный раствор имеет рН > 8; д) с азотистой кислотой при 0-5 °С моментально выделяет азот; е) в реакции с NaHCO3 выделяет СО2 | |
| С6Н16N2 | а) хорошо растворяется в органических и минеральных кислотах с образованием солей; б) водный раствор имеет рН > 9; в) дает два ряда алкильных и ацильных производных; г) с азотистой кислотой при 0-5 °С моментально выделяет азот с образованием двухатомного спирта, у которого ОН-группы связаны с первичными С-атомами; д) имеет неразветвленный углеродный скелет; е) используется в реакциях поликонденсации с двухосновными карбоновыми кислотами с целью получения синтетических волокон |
Продолжение табл. 57
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С3Н7NO3 | а) образует соли с кислотами и щелочами; б) дает фиолетовое окрашивание с нингидрином; в) с азотистой кислотой при 0-5 °С моментально выделяет азот с образованием глицериновой кислоты, которая при добавлении щелочного раствора Cu(OH)2 дает комплекс ярко-синего цвета | |
| С6Н8N2 | а) образует соли с минеральными кислотами; б) дает два ряда алкильных и ацильных производных; в) обесцвечивает бромную воду с образованием светлой мути; г) в реакции с азотистой кислотой при 0-5 °С образует соль диазония, которая при нагревании превращается в вещество состава С6Н6О2, дающее цветную реакцию с FeCl3; д) в веществе С6Н6О2 функциональные группы находятся в пара -положении друг относительно друга | |
| С4Н9NO3 | а) имеет четыре оптических изомера; б) входит в состав белков; в) имеет три функциональные группы, две из которых взаимодействуют с РСl5; г) с азотистой кислотой при 0-5 °С моментально выделяет азот с образованием вещества состава С4Н8О4, которое при добавлении щелочного раствора Cu(OH)2 дает комплекс ярко-синего цвета | |
| С10Н9N | а) растворяется в HCl; б) алкилируется и ацилируется; в) в реакции с азотистой кислотой при 0-5 °С образует соль диазония, которая при нагревании превращается в вещество состава С10Н8О, дающее с FeCl3 характерное зеленое окрашивание | |
| С6Н13NO2 | а) проявляет амфотерные свойства; б) может существовать в виде энантиомеров; в) не входит в состав белковых молекул; г) не дает биуретовую и нингидриновую реакции; д) при нагревании выше Тпл выделяет аммиак иобразует вещество состава С6Н10O2, которое при жестком окислении хромовой смесью превращается в щавелевую кислоту и бутан-2-он |
Окончание табл. 57
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С7Н9N | а) в водном растворе имеет рН > 8; б) с H2SO4 образует соль; в) алкилируется и ацилируется; г) с азотистой кислотой при 0-5 °С моментально выделяет азот; д) при жестком окислении хромовой смесью образует бензойную кислоту | |
| С6Н13NO2 | а) не может существовать в виде энантиомеров; б) содержит один четвертичный С-атом; в) образует соли с кислотами и основаниями; г) с азотистой кислотой при 0-5 °С моментально выделяет азот; д) при нагревании выше Тпл образует лактам состава С6Н11NO | |
| С5Н13N | а) в водном растворе имеет рН > 8; б) может существовать в виде энантиомеров; в) при алкилировании 2 моль СН3Cl образует четвертичную аммонийную соль | |
| С8Н9NO2 | а) образует соли с NaHCO3 и H2SO4; б) алкилируется и ацилируется; в) с азотистой кислотой при 0-5 °С моментально выделяет азот; г) при жестком окислении KMnO4, H2SO4, t, °С образует фталевую кислоту (1,2-бензолдикарбоновую) |
Задача 38
Из соответствующих природных аминокислот постройте формулу трипептида, указанного в табл. 58. Обозначьте пептидные связи, назовите образованный трипептид. Перечислите, какие качественные реакции и почему могут протекать для полученного трипептида.
Таблица 58
| Вариант | Пептид | Вариант | Пептид |
| Ala-Cys-Ser | Phe-Leu-Thr | ||
| Gly-Clu-Trp | Asp-Lys-Met | ||
| Tyr-Val-Lys | His-Ala-Cys |
Окончание табл. 58
| Вариант | Пептид | Вариант | Пептид |
| Trp-Ser-Glu | Ser-Phe-Asp | ||
| Gly-Tyr-Ile | Ile-Gly-Thr | ||
| Ile-Met-Ser | Leu-Ala-Glu | ||
| Val-Leu-Lys | Met-Tyr-Val | ||
| Leu-Glu-Ala | Lys-Ser-Val | ||
| Pro-Ala-Val | Trp-Cys-Phe | ||
| Gly-His-Thr | His-Leu-Gly | ||
| Ala-Phe-Ala | Glu-Gly-Ile | ||
| Tyr-Gln-Gly | Ser-Trp-Met | ||
| Lys-Cys-Asp | Pro-Cys-Ala | ||
| Val-His-Gly | Trp-Ala-Glu | ||
| Met-Trp-Ala | Val-His-Gly |

ЛИТЕРАТУРА
1. Кузьменок, Н. М. Органическая химия. Тесты, задачи, упражнения: учеб. пособие для студентов химико-технологических специальностей / Н. М. Кузьменок, Т. С. Селиверстова. – Минск: БГТУ, 2008. – 225 с.
2. Щербина, А. Э. Органическая химия. Задачи и упражнения: учеб. пособие для студентов химико-технологических специальностей / А. Э. Щербина, Л. Г. Матусевич, И. В. Сенько. – Минск: БГТУ, 2003. – 305 с.
3. Органическая химия. Реакционная способность основных классов органических соединений: учеб. пособие для студентов химико-технологических специальностей / А. Э. Щербина и [др.]. – Минск: БГТУ, 2000. – 615 с.
4. Органическая химия: учеб. для вузов: в 2 кн. / В. Л. Белобородов [и др.]; под общ. ред. Н. А. Тюкавкиной. – М.: Дрофа, 2002. – Кн. 1: Основной курс. – 640 с.
5. Грандберг, И. И. Органическая химия / И. И. Грандберг. – М.: Дрофа. 2001. – 672 с.
6. Потапов, В. М. Органическая химия / В. М. Потапов, С. Н. Татаринчик. – М.: Химия, 1989. – 448 с.
7. Травень, В. Ф. Органическая химия: учеб. для вузов: в 2 т. /
В. Ф. Травень. – М.: ИКЦ «Академкнига», 2006. – Т. 1. – 727 с.
8. Травень, В. Ф. Органическая химия: учеб. для вузов: в 2 т. /
В. Ф. Травень. – М.: ИКЦ «Академкнига», 2006. – Т. 2. – 582 с.
ОГЛАВЛЕНИЕ
| ПРЕДИСЛОВИЕ.......................................................................... 1. КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Классы органических соединений Рациональная номенклатура Углеводороды и углеводородные радикалы Основы рациональных названий и окончаний по систематической номенклатуре основных классов органических соединений Примеры названий по рациональной номенклатуре Систематическая номенклатура ИЮПАК Примеры названий органических соединений по систематической номенклатуре (ИЮПАК) Задача 1 Пример решения задачи 1 Задача 2 Пример решения задачи 2............................................................ 2. ХИМИЧЕСКАЯ СВЯЗЬ Задача 3 Пример решения задачи 3 Задача 4 Пример решения задачи 4........................................................... 3. ХИМИЧЕСКАЯ РЕАКЦИЯ Задача 5 Пример решения задачи 5 Задача 6 Пример решения задачи 6........................................................... 4. АЛКАНЫ Номенклатура алканов Способы получения алканов Химические свойства алканов Задача 7 Пример решения задачи 7 Задача 8 Пример решения задачи 8........................................................... 5. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ Номенклатура Способы получения алкенов Химические свойства алкенов Задача 9 Пример решения задачи 9 Задача 10 Пример решения задачи 10 Химические свойства алкадиенов Задача 11 Пример решения задачи 11 Задача 12 Пример решения задачи 12 Способы получения алкинов Химические свойства алкинов Задача 13 Пример решения задачи 13 Задача 14 Пример решения задачи 14 Задача 15 Пример решения задачи 15 Задача 16 Пример решения задачи 16......................................................... 6. АРЕНЫ Номенклатура и изомерия замещенных бензола Способы получения аренов Химические свойства аренов Задача 17 Пример решения задачи 17 Задача 18 Пример решения задачи 18 Задача 19 Пример решения задачи 19.......................................................... 7. ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ Номенклатура галогенопроизводных углеводородов Химические свойства галогенопроизводных углеводородов Задача 20 Пример решения задачи 20 Задача 21 Пример решения задачи 21.......................................................... 8. СПИРТЫ, ФЕНОЛЫ, ПРОСТЫЕ ЭФИРЫ Классификация и номенклатура спиртов Классификация и номенклатура фенолов Классификация и номенклатура простых эфиров Способы получения спиртов Способы получения фенолов Способы получения простых эфиров Кислотно-основные свойства спиртов и фенолов Основные химические свойства спиртов, фенолов и простых эфиров Задача 22 Пример решения задачи 22 Задача 23 Пример решения задачи 23 Задача 24 Пример решения задачи 24.......................................................... 9. АЛЬДЕГИДЫ И КЕТОНЫ Классификация и номенклатура Примеры номенклатуры альдегидов Примеры номенклатуры кетонов Способы получения карбонильных соединений Химические свойства карбонильных соединений Задача 25 Пример решения задачи 25 Задача 26 Пример решения задачи 26.......................................................... 10. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ Классификация и номенклатура Примеры номенклатуры карбоновых кислот Функциональные производные карбоновых кислот Примеры названий кислотных остатков Номенклатура функциональных производных кислот Примеры названий функциональных производных Способы получения карбоновых кислот Способы получения функциональных производных кислот Задача 27 Пример решения задачи 27 Задача 28 Пример решения задачи 28 Задача 29 Пример решения задачи 29 Задача 30 Пример решения задачи 30.......................................................... 11. УГЛЕВОДЫ Классификация углеводов Тривиальные названия моносахаридов Классификация моносахаридов Количество пространственных изомеров D- и L-ряды моносахаридов Построение формул Хеуорса Химические свойства моносахаридов Классификация и номенклатура дисахаридов Химические свойства дисахаридов Задача 31 Пример решения задачи 31 Задача 32 Пример решения задачи 32......................................................... 12. НИТРОСОЕДИНЕНИЯ Классификация и номенклатура нитросоединений Способы получения нитросоединений Химические свойства нитросоединений Задача 33 Пример решения задачи 33......................................................... 13. АМИНЫ, АМИНОКИСЛОТЫ И ПЕПТИДЫ Классификация и номенклатура аминов Основность аминов Химические свойства аминов Классификация и номенклатура аинокислот Природные аминокислоты Химические свойства аминокислот Задача 34 Пример решения задачи 34 Задача 35 Пример решения задачи 35 Задача 36 Пример решения задачи 36 Задача 37 Пример решения задачи 37 Задача 38 Пример решения задачи 38 КАЧЕСТВЕННЫЕ РЕАКЦИИ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Качественные реакции непредельных углеводородов Реакция с бромной водой алкенов, алкинов Реакция с реактивом Вагнера алкенов, алкадиенов, алкинов Реакции на концевую тройную связь Качественные реакции спиртов Реакция с активными металлами Растворение в концентрированных кислотах Качественная реакция на вицинальные полиолы Качественные реакции фенолов Реакция с FeCl3 Реакция с бромной водой Качественная реакция простых эфиров Качественные реакции альдегидов и кетонов Реакции окисления Реакция с натрий-гидросульфитом Иодоформная реакция Качественная реакция на карбоксильную группу Качественная реакция сложных эфиров Качественные реакции на амины Растворение алифатических аминов в воде Реакции аминов с азотистой кислотой Реакция ароматических аминов с бромной водой Качественные реакции на аминокислоты Биуретовая реакция Нингидриновая реакция Ксантопротеиновая реакция Реакция Фоля ЛИТЕРАТУРА.............................................................................. |
Учебное издание
Каток Ядвига Марьяновна
Толкач Ольга Ярославовна
|
|
|
|
|
Дата добавления: 2014-12-26; Просмотров: 1579; Нарушение авторских прав?; Мы поможем в написании вашей работы!