
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры названий кислотных остатков
|
|
|
|
Кислота
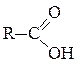
| Название ацильной группы
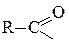
| Название ацилоксигруппы

|
| метановая, муравьиная (от лат. formic) |  метан оил,
форм ил *
метан оил,
форм ил *
|  метан оат,
форми ат *
метан оат,
форми ат *
|
| этановая, уксусная (от лат. acetic) |  этан оил,
ацет ил *
этан оил,
ацет ил *
|  этан оат,
ацет ат *
этан оат,
ацет ат *
|
Окончание табл. 42
| пропановая, пропионовая | 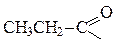 пропан оил,
пропион ил
пропан оил,
пропион ил
| 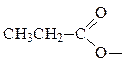 пропан оат,
пропион ат
пропан оат,
пропион ат
|
| бутановая, масляная (от лат. butyric) | 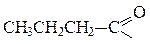 бутан оил,
бутир ил *
бутан оил,
бутир ил *
|  бутан оат,
бутир ат *
бутан оат,
бутир ат *
|
| пропеновая, акриловая | 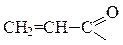 пропен оил,
акрило ил *
пропен оил,
акрило ил *
| 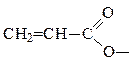 пропен оат,
акрил ат *
пропен оат,
акрил ат *
|
| этандиовая, щавелевая (от лат. oxalic) |  этан диоил,
оксал ил *
этан диоил,
оксал ил *
|  этан диоат,
оксал ат *
этан диоат,
оксал ат *
|
| бутандиовая, янтарная (от лат. succinic) | 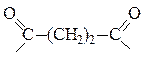 бутан диоил,
сукцин ил *
бутан диоил,
сукцин ил *
| 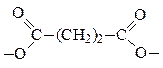 бутан диоат,
сукцин ат *
бутан диоат,
сукцин ат *
|
| бензойная |  бенз оил
бенз оил
| 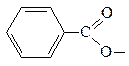 бенз оат
бенз оат
|
| 1,2-бензолдикарбоновая (фталевая) | 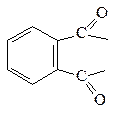 фтал оил
фтал оил
| 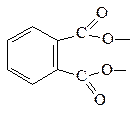 фтал ат * (фтал оат)
фтал ат * (фтал оат)
|
* Предпочтительное название кислотного остатка.
Функциональные производные кислот подобно кислотам могут быть алифатическими или ароматическими, насыщенными или ненасыщенными. Названия производных образуют из тривиальных или систематических названий соответствующих кислот. Допускается давать названия функциональным производным и описательным способом (табл. 43).
Название галогенангидрида образуется от названия карбоновой кислоты путем замены суффикса -овая кислота на суффикс -оилгалогенид.
Ангидриды называют согласно названиям соответствующих кислот с заменой слова кислота на ангидрид.
В названии сложного эфира сначала указывают алкильную группу, связанную с кислородом, затем название ацилоксигруппы, то есть заменяют суффикс в названии кислоты -овая кислота на суффикс -оат.
При составлении названия амида суффикс в названии кислоты -овая кислота заменяют на суффикс -амид. Назвать амид можно и от соответствующей ацильной группы заменой суффикса -оил (или -ил)на -амид. В случае моно- и дизамещенных амидов перед основным названием перечисляют алкильные группы, связанные с азотом с символом N- или N,N- соответственно.
Названия солей производят от соответствующих названий ацилоксигрупп, добавляя название металла (или другого катиона). Кислые соли дикарбоновых кислот называют аналогично нейтральным. Наличие иона водорода обозначают префиксом гидро- перед названием ацилоксигруппы.
К функциональным производным карбоновых кислот относятся и нитрилы, которые образуются в результате замещения карбоксильной группы СООН на группу нитрильную СºN.
Их названия формируют, добавляя суффикс -онитрил к названию родоначального углеводорода с тем же числом атомов
углерода (буква о вставляется между двумя согласными для благозвучия). Если кислота имеет тривиальное название, то название произведенного от нее нитрила образуют путем замены суффикса -оил (или -ил)ацильной группы на -онитрил. При наличии более старшей группы в молекуле группа СºN обозначается префиксом циано-.
Таблица 43
Примеры названий функциональных производных карбоновых кислот
Функциональное производное

| Х | Суффикс в названии | Пример | Название* | Название описательным способом |
| галогенангидриды | F, Cl, Br, I | -оилгалогенид | 


| ацетилхлорид, этаноилхлорид бензоилиодид оксалилдибромид, этандиоиодибромид | хлорангидрид уксусной (этановой) кислоты иодангидрид бензойной кислоты бромангидрид щавелевой (этандиовой) кислоты |
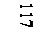 ангидриды ангидриды
| 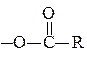
| -овый ангидрид | 
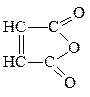
| пропановый или пропионовый ангидрид малеиновый ангидрид | ангидрид пропановой (пропионовой) кислоты ангидрид малеиновой кислоты |

Продолжение табл. 43
 Функциональное производное Функциональное производное

| Х | Суффикс в названии | Пример | Название* | Название описательным способом |
| сложные эфиры | – OR1 | -оат | 

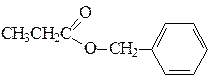
| изопропилформиат, изопропилметаноат диметилфталат, диметилфталоат бензилпропионат, бензилпропаноат | изопропиловый эфир муравьиной (метановой) кислоты диметиловый эфир фталевой кислоты бензиловый эфир пропионовой (пропановой) кислоты |
| амиды | – NH2 – NHR – NR2 | -амид | 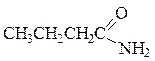
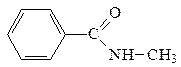

| бутанамид, бутирамид N-метилбензамид N,N-диметилформамид, N,N-диметилметанамид | амид бутановой кислоты N-метиламид бензойной кислоты N,N-диметиламид муравьиной (метановой) кислоты |

Окончание табл. 43
Функциональное производное

| Х | Суффикс в названии | Пример | Название* | Название описательным способом |
| соли | – OМет | -ат | 


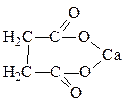
| пентаноат натрия, валерат натрия гидрооксалат калия, гидроэтандиоат калия акрилат аммония, пропеноат аммония сукцинат кальция, бутандиоат кальция | натриевая соль пентановой (валериановой) кислоты кислая калиевая соль щавелевой кислоты, монокалиевая соль этандиовой кислоты аммонийная соль акриловой (пропеновой) кислоты кальциевая соль янтарной (бутандиовой) кислоты |
| нитрилы | – CºN | -онитрил | 


| ацетонитрил, этанонитрил гексанонитрил бензонитрил | нитрил уксусной (этановой) кислоты нитрил гексановой кислоты нитрил бензойной кислоты |
 *Первым приведено более употребимое название функционального производного карбоновой кислоты.
*Первым приведено более употребимое название функционального производного карбоновой кислоты.
Индивидуальные задания
Задача 27
1. Дайте определение понятий «функциональные производные карбоновых кислот» и «замещенные карбоновые кислоты». Напишите уравнения реакций получения из кислоты А ее производных (табл. 44): а) бариевой соли; б) хлорангидрида; в) ангидрида; г) сложного эфира (реакцией этерификации с пропан-
1-олом); д) амида. Назовите полученные соединения.
2. Приведите уравнения реакций гидролиза в кислой и щелочной среде вещества Б. Сравните активность в реакциях ацилирования веществ А и Б, дайте необходимые пояснения.
Таблица 44
| Вариант | Кислота А | Вещество Б |
| пропановая | ацетилбромид | |
| фенилэтановая | бензамид | |
| муравьиная | этановый ангидрид | |
| бензойная | этилбензоат | |
| 4-бромбензойная | бензоилхлорид | |
| бутановая | метилбутират | |
| изовалериановая | N,N-диметилэтанамид | |
| пальмитиновая | метилстеарат | |
| уксусная | N-метилацетамид | |
| масляная | этилпропионат | |
| 4-нитробензойная | бутирилхлорид | |
| хлоруксусная | ацетилхлорид | |
| валериановая | пентанамид | |
| триметилуксусная | бензойный ангидрид | |
| диметилпропилуксусная | бутанамид | |
| 2-метилпропановая | этилбутаноат | |
| гексановая | N,N-диметилгексанамид | |
| бромуксусная | этаноилбромид | |
| нитроэтановая | метилэтаноат | |
| изомасляная | пропановый ангидрид | |
| 4-метилбензойная | бензамид |
Окончание табл. 44
| Вариант | Кислота А | Вещество Б |
| 3-хлорбензойная | метилбензоат | |
| пара -толуиловая | бензоилбромид | |
| метановая | N,N-диметилформамид | |
| 3,3-диметилбутановая | бензилпропиноат | |
| циклогексанкарбоновая | метилбензоат | |
| 4-метоксибензойная | бензамид | |
| 2-аминобензойная | бензоилбромид | |
| фторэтановая | фторэтанамид | |
| изобутилуксусная | бензилформиат |
Задача 28
Заполните схемы превращений, приведенные в табл. 45. Назовите промежуточные и конечные продукты.
Таблица 45
| Вариант | Схема превращений |

| |
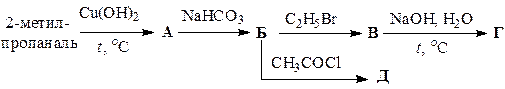
| |
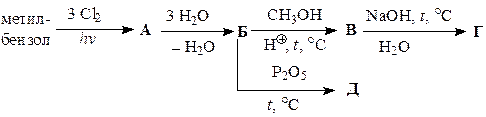
| |

|
Продолжение табл. 45
| Вариант | Схема превращений |

| |
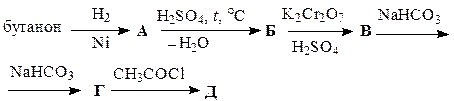
| |
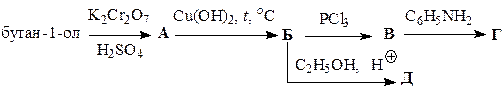
| |
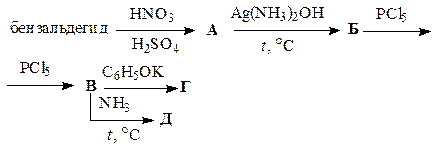
| |
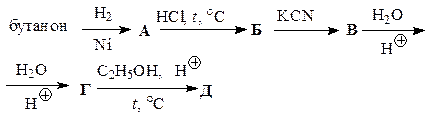
| |

| |
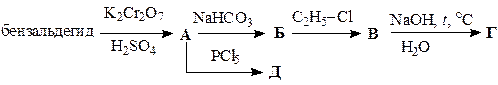
| |

|
Продолжение табл. 45
| Вариант | Схема превращений |
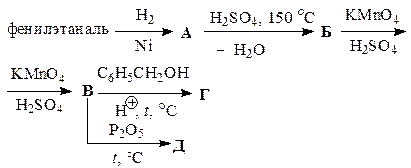
| |

| |
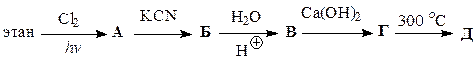
| |

| |

| |
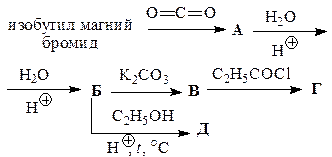
| |

|
Продолжение табл. 45
| Вариант | Схема превращений |

| |

| |
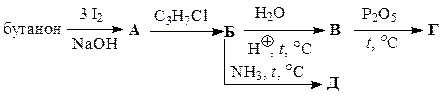
| |

| |

| |
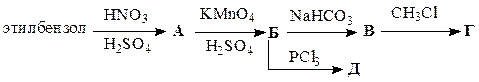
| |

| |

|
Окончание табл. 45
| Вариант | Схема превращений |

| |

| |
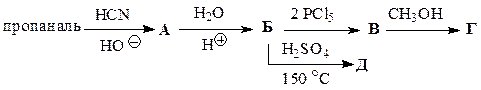
|
Задача 29
С помощью качественных реакций и проб различите между собой вещества А, Б и В (табл. 47). Составьте план эксперимента в виде приведенной ниже табл. 46. Запишите уравнения использованных реакций, опишите наблюдаемый результат.
Таблица 46
| Опыт | Реагент | Наблюдаемый результат и вывод | ||
| вещество А | вещество Б | вещество В | ||
| … | ||||
| Общий вывод | формула А | формула Б | формула В |
Таблица 47
| Вариант | А | Б | В |
| изопропилацетат | бутан-1,2-диол | пентан-3-он | |
| фенилуксусный альдегид | салициловая кислота | ацетилсалициловая кислота | |
| метилфенилкетон | этилбензоат | диизопропилкетон | |
| пара -крезол | пропан-1-ол | бутановая кислота | |
| муравьиная кислота | винная кислота | 4-хлорфенол | |
| трет бутиловый спирт | бензальдегид | бензойная кислота |
Окончание табл. 47
| Вариант | А | Б | В |
| пропан-1,2-диол | метилпропилкетон | бензилацетат | |
| бутан-2,3-диол | хлораль | уксусная кислота | |
| циклогексанол | циклогексанон | формальдегид | |
| 2-хлорфенол | этилформиат | бутаналь | |
| этилбутиловый эфир | гексан-3-он | изопентилацетат | |
| этилизобутилкетон | 2,2-диметилпропаналь | фталевая кислота | |
| бензиловый спирт | галловая кислота | пентан-2-он | |
| этандиол | этаналь | пропилбензоат | |
| диэтилкетон | глицерин | 3-метилбутан-2-ол | |
| бутилацетат | бутан-2-ол | бут-3-ен-1-ол | |
| 2,3-дигидроксипропаналь | пирокатехин | метилизобутилуксусный альдегид | |
| мета -крезол | 1,4-бензолдикарбоновая кислота | метилбензилкетон | |
| бутановая кислота | 2-нафтол | 2-метилбутан-1,2-диол | |
| щавелевая кислота | 4-изопропилбензальдегид | пропан-1,2-диол | |
| 3-метилгексан-2-он | бензилбензоат | 3-метилгексаналь | |
| коричная кислота | изопропилфенилкетон | терефталевая кислота | |
| 2-метилпентановая кислота | пентан-2-он | ксилит (пентан-1,2,3,4,5-пентаол) | |
| 4-гидроксибензойная кислота | метилбензоат | 4-бромбензойная кислота | |
| глицерин | 2,4-диметил-пентан-3-он | бензилпропиноат | |
| адипиновая кислота | этилбутират | трихлоруксусная кислота | |
| пентан-2,3-диол | щавелевая кислота | диметилкетон | |
| диизобутиловый эфир | изобутиловый спирт | диизобутилкетон | |
| 3,4-диметилгексаналь | глицерин | гексановая кислота | |
| 4-гидроксибензальдегид | галловая кислота | метилфенилкетон |
Задача 30
Установите строение соединения с молекулярной формулой А, которое соответствует приведенному в табл. 48 описанию. Обоснуйте выбор структурной формулы, сделав вывод по каждому из пунктов описания свойств. Назовите установленное вещество, напишите все упомянутые в условии уравнения реакций.
Таблица 48
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С4Н4О4 | а) выделяет СО2 при взаимодействии с NaHCO3; б) обесцвечивает бромную воду и реактив Вагнера; в) может существовать в виде цис-транс- изомеров, один из которых легко, а другой трудно растворим в воде; г) при нагревании до 200 °С образуется соединение состава С4Н2О3, которое не обладает кислотными свойствами и реагирует с водой | |
| С8Н10О | а) дает цветную реакцию с FеCl3; б) алкилируется метилбромидом в щелочной среде; в) при окислении продукта алкилирования образуется 4-метоксибензойная кислота | |
| С8Н8О3 | а) реагирует с NaHCO3 с выделением газа; б) образует сложные эфиры как с карбоновыми кислотами, так и со спиртами; в) не дает цветную реакцию с FеCl3; г) при жестком окислении превращается в 1,2-бензолдикарбоновую кислоту | |
| С4Н6О4 | а) проявляет кислотные свойства; б) с этанолом (в присутствии Н2SO4) образует производное состава С8Н14О4; в) при нагревании выделяет СО2 с образованием нового соединения С3Н6О2, которое также обладает кислотными свойствами | |
| С5Н10О2 | а) имеет рН< 4; б) реагирует с NaHCO3 с выделением газа; в) с фосфор-пентахлоридом образует вещество состава С5Н9OCl; г) при cплавлении со щелочью его натриевой соли образуется 2-метилпропан | |
| C8H6O3 | а) реагирует с карбонатами с выделением газа; б) дает реакцию «серебряного зеркала»; в) с этанолом в кислой среде образует соединение состава С14Н20О4; г) при окислении хромовой смесью образует 1,4-бензолдикарбоновую кислоту |
Продолжение табл. 48
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С8Н8О2 | а) образует оксим и гидразон; б) дает положительную иодоформную реакцию; в) дает цветную реакцию с FеCl3; г) функциональные группы в искомом соединении имеют согласованную ориентацию в SE-реакциях; д) не способно к образованию внутримолекулярной водородной связи | |
| С3Н4О3 | а) не дает реакцию «серебряного зеркала»; б) дает положительную иодоформную реакцию; в) образует оксим, гидразон, хлорангидрид; г) в реакции с натрий-гидрокарбонатом выделяет газ | |
| C8H8O3 | а) выделяет СО2 при взаимодействии с карбонатами; б) с этанолом образует вещество состава С9Н10О3; в) при нагревании с концентрированной НI образует салициловую кислоту | |
| С6Н12О3 | а) образует соль с СаСО3; б) при взаимодействии с РСl5 образует вещество состава C6H10Cl2; в) при нагревании с серной кислотой образует соединение, обладающее кислотными свойствами, состава С6Н10О2; г) соединение С6Н10О2 дает бурый осадок с реактивом Вагнера, а при окислении хромовой смесью образует метилэтилкетон и щавелевую кислоту | |
| С4Н6О6 | а) реагирует с NaHCO3 с выделением газа; б) вступает в реакцию этерификации с метанолом с образованием соединения состава С6Н10О6; в) в сильно щелочной среде образует комплекс темно-синего цвета с Сu(OH)2 | |
| C8H6O4 | а) не растворяется в воде, но растворяется в растворах NaOH и NaHCO3; б) при интенсивном нагревании образует соединение состава C8H4O3, которое не проявляет кислотные свойства; в) вещество C8H4O3 легче, чем искомое, вступает в реакции ацилирования с этанолом и метиламином |
Продолжение табл. 48
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С9Н12О | а) реагирует с металлическим натрием с выделением газа; б) при нагревании с водоотнимающим средством образует соединение состава С9Н10, которое обесцвечивает бромную воду, а при окислении KMnO4 + H2SO4 образует 1,4-бензолдикарбоновую кислоту; в) при дегидрировании (Cu, 630 °C) образует кетон | |
| С3Н8О2 | а) выделяет водород при взаимодействии с металлическим натрием; б) при взаимодействии с избытком РСl5 образует соединение состава C3H7СlO; в) при нагревании с концентрированной НI образует иодметан и вещество состава С2H6O2, которое растворяет Сu(OH)2 с образованием комплекса темно-синего цвета | |
| C8H8O3 | а) способно к образованию внутримолекулярной водородной связи; б) дает фиолетовое окрашивание при добавлении раствора FeCl3; в) обесцвечивает бромную воду с образованием светлого осадка; г) при кислотном гидролизе образует метанол и вещество состава C7H6O3, которое при добавлении раствора NaHCO3 выделяет углекислый газ | |
| С6Н12О2 | а) образует кристаллический осадок с натрий-гидросульфитом; б) реагирует с металлическим натрием без нагревания; в) при нагревании с Cu(ОН)2 образует красный осадок Cu2О; г) может быть получено реакцией альдольной конденсации пропаналя | |
| С6Н14О2 | а) молекула имеет симметричное строение; б) выделяет водород при взаимодействии с металлическим натрием; в) не образует комплекс темно-синего цвета с Сu(OH)2; г) при дегидратации образует алкадиен состава С6Н10, который при окислении KMnO4 в кислой среде образует 2 моль СО2 и 1 моль бутандиона |
Продолжение табл. 48
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С4Н8О2 | а) реагирует с металлическим натрием при комнатной температуре с выделением газа; б) при взаимодействии с PCl5 образует соединение состава С4Н7Cl3; в) дает положительную реакцию «серебряного зеркала»; г) окисление хромовой смесью приводит к образованию янтарной кислоты | |
| С9Н8О2 | а) сгорает с выделением сажи; б) с реактивом Вагнера образует бурый осадок MnO2; в) существует в виде цис-транс -изомеров; г) реагирует с натрий-гидрокарбонатом с выделением газа | |
| С5Н8О3 | а) выделяет СО2 при взаимодействии с NaНСО3; б) с метанолом в кислой среде образует соединение состава С6Н10О3; в) присоединяет молекулу HCN в щелочной среде; г) образует желтый осадок иодоформа при взаимо- действии с I2 + NaOH; д) имеет неразветвленный углеродный скелет | |
| С5Н8О2 | а) не проявляет кислотные свойства; б) обесцвечивает бромную воду; в) при гидролизе в водном растворе щелочи образует два органических продукта, один из которых метанол; г) легко вступает в реакцию полимеризации с образованием полимера, который используется для изготовления органического стекла | |
| С7Н8О2 | а) хорошо растворяется в NaOH; б) ацилируется уксусным ангидридом в щелочной среде; в) обесцвечивает бромную воду с образованием соединения состава С7Н5Br3О2; г) при нагревании с концентрированной HI образуется иодметан и вещество, которое с раствором FeCl3 дает цветную реакцию |
Продолжение табл. 48
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| C9H8O | а) обесцвечивает бромную воду; б) с NaHSO3 образует кристаллический осадок; в) дает реакцию «серебряного зеркала»; г) при окислении KMnO4 в кислой среде образует бензолдикарбоновую кислоту с согласованной ориентацией в SE-реакциях | |
| С10Н12О2 | а) не проявляет кислотные свойства; б) при гидролизе в кислой среде образует два органических соединения, одно из которых при взаимодействии с NaHCO3 выделяет углекислый газ; в) искомое вещество может быть получено ацилированием фенолята натрия хлорангидридом кислоты с разветвленным углеродным скелетом | |
| С6Н14О | а) растворяется в холодной концентрированной H2SO4 с образованием оксониевой соли; б) не взаимодействует с металлическим натрием при комнатной температуре, но при нагревании претерпевает расщепление с образованием двух органических продуктов; в) может быть получено по реакции Вильямсона из трет -бутилата натрия и алкилиодида | |
| С6Н12О3 (2 изомера) | а) образуют соли с СаСО3; б) в реакции с РCl5 образуют соединения состава С6Н10Cl2О; в) в результате внутримолекулярной дегидратации обоих изомеров получается одно и то же соединение состава С6Н10О2, которое образует бурый осадок при взаимодействии с реактивом Вагнера; г) вещество С6Н10О2 при жестком окислении хромовой смесью образует ацетон и малоновую кислоту | |
| С9Н8О3 | а) выделяет СО2 при взаимодействии с карбонатами; б) при гидролизе образует уксусную кислоту и соединение состава С7Н6О3, которое дает фиолетовое окрашивание с FeCl3 и образует осадок с бромной водой; в) искомое вещество широко используется в медицине |
Окончание табл. 48
| Вариант | Молекулярная формула соединения А | Описание свойств соединения А |
| С3Н6О3 | а) с C6H5NHNH2 образует фенилгидразон; б) в щелочной среде присоединяет HCN; в) дает реакцию «серебряного зеркала»; г) растворяет Cu(OH)2 с образованием раствора темно-синего цвета | |
| С8Н6О4 | а) не растворяется в воде, но растворяется в растворах NaOH и NaHCO3; б) с этанолом образует соединение состава С12Н14О4; в) вступает в реакцию поликонденсации с этандиолом с образованием полимера, который используется в производстве синтетического волокна лавсан | |
| С5H10О | а) с гидроксиламином образует оксим; б) не восстанавливает Сu(OH)2; в) присоединяет водород с образованием спирта, который при нагревании с водоотнимающим средством дает углеводород С5Н10; г) вещество С5Н10 при жестком окислении образует смесь этановой и пропановой кислот |
Пример решения и оформления задачи на установление строения неизвестного вещества.
Установить строение соединения состава С10Н10О, которое: а) обесцвечивает бромную воду и реактив Вагнера; б) может cуществовать в виде цис-транс-изомеров; в) образует осадок с NaHSO3; г) при нагревании восстанавливает Cu(OH)2 до Cu2O; д) при окислении хромовой смесью образует терефталевую кислоту.
| Экспериментальные данные | Выводы о строении |
| С10Н10О т. е. С n H2 n -10O | сильно ненасыщенное кислородсодержащее соединение (возможно содержит бензольное кольцо) |
| обесцвечивает бромную воду и реактив Вагнера | содержит алифатические кратные связи |
| Экспериментальные данные | Выводы о строении |
| может существовать в виде цис-транс -изомеров | содержит не концевую двойную связь |
| образует осадок с NaHSO3 | является альдегидом или метилкетоном |
| при нагревании восстанавливает Cu(OH)2 до Cu2O | содержит альдегидную группу, не связанную с бензольным кольцом |
| при окислении хромовой смесью образует терефталевую кислоту | содержит две боковые цепи, находящиеся по отношению друг к другу в пара -положении |
На основании выводов о строении устанавливаем, что искомое соединение имеет следующую структурную формулу:

3-(4-метилфенил)пропеналь
(пара -метилкоричный альдегид)
Уравнения реакций, подтверждающие строение искомого соединения:




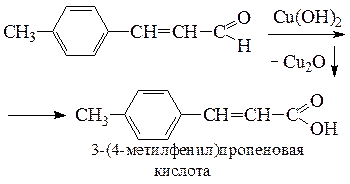


11. УГЛЕВОДЫ

Схема 3. Классификация углеводов
|
|
|
|
|
Дата добавления: 2014-12-26; Просмотров: 5355; Нарушение авторских прав?; Мы поможем в написании вашей работы!