
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основное уравнение МКТ идеального газа
|
|
|
|
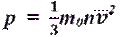 основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда.
основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда.
Это же уравнение в другой записи:

ВЫВОД
Число ударов молекул о стенку при условии, что скорости частиц одинаковы и равновероятно распределены по шести направлениям: вперед - назад, налево - направо, вверх – вниз:


При ударе одной частицы о стенку, частица передает стенке удвоенный импульс. Суммарный импульс, которые частицы передают стенке:
 ,
,
где 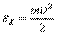 — средняя кинетическая энергия поступательного движения одной молекулы.
— средняя кинетическая энергия поступательного движения одной молекулы.
Давление газа равно импульсу, которые частицы при ударах передают стенке за единицу времени на единицу поверхности:
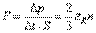 .
.
8. Теплоёмкость тела( СИ — Дж/К) — физическая величина, определяющая отношение бесконечно малого количества теплоты δ Q, полученного телом, к соответствующему приращению его температуры δ T: или (отношение кол-ва теплоты, поглощаемой телом при бесконечно малом изменении его темп-ры, к этому изменению.)

Уравнение Майера:
Qp=Δ⋅U+Ap
Qp=Cp⋅ΔT
ΔU=(i2)⋅R⋅ΔT
Ap=P⋅ΔV=R⋅ΔT
Cp⋅ΔT=(i2)⋅R⋅ΔT+R⋅ΔT=(i+22)⋅R⋅ΔT
Cp=(i+22)⋅R Qv=ΔU
Qv=Cv⋅ΔT
ΔU=(i2)⋅R⋅ΔT
Cv=(i2)⋅R
Cp=Cv+R
где  — универсальная газовая постоянная,
— универсальная газовая постоянная, 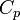 — молярная теплоемкость при постоянном давлении,
— молярная теплоемкость при постоянном давлении,  — молярная теплоемкость при постоянном объёме.
— молярная теплоемкость при постоянном объёме.
Применение первого начала термодинамики к изопроцессам:
Изохорный процесс (V=const)
Диаграмма этого процесса (изохора) в координатах р, V изображается прямой, параллельной оси ординат (рис. 1), где процесс 1—2 есть изохорное нагревание, а 1—3 — изохорное охлаждение. При изохорном процессе газ не совершает работы над внешними телами,т.е. 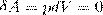
Из первого начала термодинамики (δQ=dU+δA) для изохорного процесса следует, что вся теплота, которая сообщается газу, идет на увеличение его внутренней энергии:

т.к. CV=dUm/dt,
Тогда для произвольной массы газа получим

Изобарный процесс (p=const).
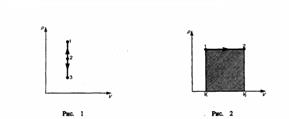
Диаграмма этого процесса (изобара) в координатах р, V изображается прямой, которая параллельна оси V. При изобарном процессе работа газа при увеличения объема от V1 до V2 равна

и равна площади заштрихованного прямоугольника (рис. 2). Если использовать уравнение Менделеева-Клапейрона для выбранных нами двух состояний, то
 и
и 
откуда

Тогда выражение для работы изобарного расширения примет вид

В изобарном процессе при сообщении газу массой m количества теплоты

его внутренняя энергия возрастает на величину (т.к. CV=dUm/dt)
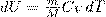
Изотермический процесс (T=const). Изотермический процесс описывается законом Бойля—Мариотта:
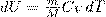
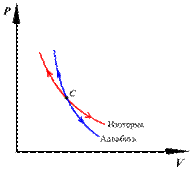
Диаграмма этого процесса (изотерма) в координатах р, V представляет собой гиперболу, которая расположена на диаграмме тем выше, чем выше температура, при которой происходит процесс.
Исходя из формул для работы газа и уравнения Менделеева-Клайперона найдем работу изотермического расширения газа:

Так как при Т=const внутренняя энергия идеального газа не изменяется:
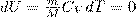
то из первого начала термодинамики (δQ=dU+δA) следует, что для изотермического процесса

т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил:
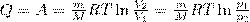
9. Адиабатный процесс — процесс, при котором отсутствует теплообмен между системой и окружающей средой.
Для определения уравнения адиабаты воспользуемся первым началом термодинамики, которое запишем в следующем виде dQ = dU + pdV.
Для идеального газа dU = CVdT, следовательно, dQ = CvdT + pdV, и если процесс адиабатический dQ = 0, то
 ,
,
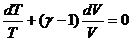 , где
, где 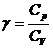 .
.
CV и Cp для идеального газа не зависят от температуры:

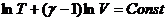 ,
,
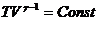 Поскольку
Поскольку  , то
, то  Уравнение Пуассона
Уравнение Пуассона
Работа газа при адиабатном процессе равна убыли внутренней энергии:
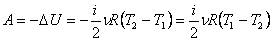 .
.
10. Закон Кулона -это закон взаимодействия двух неподвижных точечных зарядов.
Закон Кулона формулируется следующим образом: Сила электрического взаимодействия между двумя точечными зарядами в вакууме пропорциональна этим зарядам и обратно пропорциональна квадрату расстояния между ними. При взаимодействии одноименные заряды отталкиваются, разноименные притягиваются. Силы Кулона направлены по прямой, соединяющей заряды.



Единицы измерения заряда – Кулон (Кл) 1 Кл = 1 А*с
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 506; Нарушение авторских прав?; Мы поможем в написании вашей работы!