
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Механизмы нарушения синаптической передачи нейротоксикантами. Формы токсического процесса. 2 страница
|
|
|
|
Действие:
- прямое (ингибирование арсинами SH-групп структурных белков и ферментов; действие капсаицина на ионные каналы возбудимой мембраны и т.д.), приводящее к нарушению метаболизма в нервных волокнах и их возбуждению;
- опосредованное активацией процессов образования в покровных тканях брадикинина, простогландинов, серотонина и других биологически активных веществ, которые вторично возбуждают окончания ноцицептивных волокон.
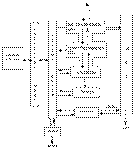 Сигналы, воспринимаемые чувствительными нейронами, передаются на нервные окончания желатинозной субстанции и чувствительного ядра спинного мозга (кожа), а также тройничного нерва (глаза, носоглотка, дыхательные пути) - первичных центров обработки информации, поступающей с периферии. Отсюда сигналы по нервным связям иррадиируют в вегетативные и двигательные ядра среднего и продолговатого отделов мозга. Возбуждение последних приводит к замыканию нервных цепей, ответственных за формирование безусловных рефлексов, лежащих в основе клиники поражения раздражающими веществами: блефароспазма, слезотечения, ринореи, саливации, (ядра лицевого и глазодвигательного нервов), чихания, кашля (ядра солитарного тракта), замедления сердечной деятельности, частоты дыхания, рефлекса Геринга - Бреейра (ядра блуждающего нерва, дыхательный и сосудодвигательный центр). Иррадиация нервного возбуждения из таламуса в структуры лимбики и экстрапирамидки при тяжелом поражении веществами лежит в основе двигательных и психических нарушений, наблюдаемых при поражении раздражающими ОВ. По таламокортикальному пути сигналы передаются в чувствительную зону коры головного мозга, где завершается интегративный процесс субъективного восприятия явлений, разыгрывающихся на периферии. Иррадиация возбуждения в коре приводит к потенцированию всех видов реакций структур головного мозга на поток импульсации, провоцируемой раздражением химическими веществами нервных окончаний.
Сигналы, воспринимаемые чувствительными нейронами, передаются на нервные окончания желатинозной субстанции и чувствительного ядра спинного мозга (кожа), а также тройничного нерва (глаза, носоглотка, дыхательные пути) - первичных центров обработки информации, поступающей с периферии. Отсюда сигналы по нервным связям иррадиируют в вегетативные и двигательные ядра среднего и продолговатого отделов мозга. Возбуждение последних приводит к замыканию нервных цепей, ответственных за формирование безусловных рефлексов, лежащих в основе клиники поражения раздражающими веществами: блефароспазма, слезотечения, ринореи, саливации, (ядра лицевого и глазодвигательного нервов), чихания, кашля (ядра солитарного тракта), замедления сердечной деятельности, частоты дыхания, рефлекса Геринга - Бреейра (ядра блуждающего нерва, дыхательный и сосудодвигательный центр). Иррадиация нервного возбуждения из таламуса в структуры лимбики и экстрапирамидки при тяжелом поражении веществами лежит в основе двигательных и психических нарушений, наблюдаемых при поражении раздражающими ОВ. По таламокортикальному пути сигналы передаются в чувствительную зону коры головного мозга, где завершается интегративный процесс субъективного восприятия явлений, разыгрывающихся на периферии. Иррадиация возбуждения в коре приводит к потенцированию всех видов реакций структур головного мозга на поток импульсации, провоцируемой раздражением химическими веществами нервных окончаний.
В мозге имеется система, подавляющее такое восприятие. Она представлена рецепторными структурами, локализующимися на мембранах нейронов, участвующих в передаче болевых сигналов в ЦНС, и чувствительными к морфину и его аналогам. Эндогенными агонистами этих рецепторов является целая группа нейропептидов, обозначаемая как "опиопептины" (иногда используют термин "эндорфины" - эндогенные морфины). К этим веществам в частности относятся: мет-энкефалин, лей-энкефалин (пентапептиды), бета-эндорфин и т.д. К сожалению, активация этих рецепторов сопровождается не только анальгезией, но и эйфорическим эффектом, повышением тонуса и ригидностью скелетной мускулатуры, угнетением дыхания, развитием физической зависимости от морфина и его аналогов.
NB! (вопросы с 8 по 13)
Клеточный уровень:
- обратимые структурно-функциональными изменениями клетки (изменение формы, сродства к красителям, подвижности и т.д.);
- преждевременная гибель клетки (некроз, апоптоз);
- мутации (генотоксичность).
Орган или система органов:
- функциональные реакции (спазм гортани, кратковременное падение артериального давления, учащение дыхания, усиление диуреза, лейкоцитоз и т.д.);
- заболевание органа;
- неопластические процессами.
Целостный организм:
- болезни химической этиологии (интоксикации, отравления);
- транзиторные токсические реакции
- аллобиоз (аллергия, иммуносупрессия, повышенная утомляемость и т.д.);
- специальные токсические процессы (действие дополнительных веществ; в определенный период жизнедеятельности организма и т.д.) и характеризующимися продолжительным скрытым периодом (канцерогенез, эмбриотоксичность, нарушение репродуктивных функций и т.д.).
Экотоксическое:
- рост заболеваемости, смертности, числа врожденных дефектов развития, уменьшением рождаемости;
- нарушение демографических характеристик популяции (соотношение возрастов, полов и т.д.);
- падение средней продолжительности жизни членов популяции, их культурной деградацией.
9. Пульмонотоксическое действие: определение, классификация по преимущественной локализации поражения, общие механизмы, формы токсического процесса (на уровне органов и систем, целостного организма).
Пульмонотоксичность - это свойство химических веществ, действуя на организм немеханическим путем вызывать структурно-функциональные нарушения со стороны органов дыхания. Вещества, порог чувствительности к которым органов дыхания существенно ниже, чем других органов и систем, и клиника поражения которыми характеризуется нарушениями со стороны, прежде всего, органов дыхания, условно можно отнести к группе пульмонотоксикантов.
Основные формы патологии дыхательной системы химической этиологии:
Острые ингаляционные поражения (по локализации поражения)
- Верхние дыхательные пути
Кашель, секреция слизи, бронхоспазм, умеренный отек дыхательных путей - защитные реакции на вредные воздействия.
При интенсивных воздействиях такие транзиторные токсические реакции перерастают в тяжелые патологические состояния.
- Глубокие дыхательные пути
Повреждение альвеолярного эпителия, эндотелия альвеолярных капилляров, альвеолярных макрофагов. Повреждение паренхимы легких приводит к развитию диффузной бронхиолярной обструкции вследствие отека, инфильтрации стенки бронхиол воспалительными клетками, а также выходу жидкости в просвет альвеол (отек легких). Повреждение макрофагов приводит к суперинфецированию и развитию химической пневмонии.
У некоторых может развиться состояние повышенной чувствительности к токсикантам, проявляющаяся синдромом реактивной дисфункции дыхательных путей (СРДП).
- Паренхима легких
Острые химические пневмонии, Отек легких, Острая дыхательная недостаточность
Хронические патологические процессы химической этиологии
Диффузный интерстициальный фиброз, Облитерирующий бронхиолит, Гигантоклеточные пневмонии, Канцерогенез
Аллергические и гиперреактивные заболевания легких
Профессиональная астма; синдром реактивной дисфункции дыхательных путей; экзогенный аллергический альвеолит; пневмокониоз;
фиброз, гранулематоз легких, вызываемый металлами, способными оказывать сенсибилизирующее действие.
Сайт депонирования ингалируемых газов определяется степенью их растворимости в тонком слое жидкости, выстилающей слизистую дыхательных путей и альвеолярный эпителий. Хорошо растворимые в воде вещества, например аммиак, диоксид серы преимущественно фиксируются верхним отделом дыхательных путей. По этой причине основной токсический эффект этих ксенобиотиков реализуется в верхних дыхательных путях, а ниже лежащие отделы поражаются лишь при очень высоких концентрациях. Напротив, плохо растворимые в воде вещества, такие как фосген, оксиды азота преимущественно поражают глубокие отделы лёгких. То есть, чем менее растворим газ в воде, тем выше его потенциал в плане поражения паренхимы легких. Водорастворимые вещества достигают глубоких отделов легких при дыхании через рот, что наблюдается при физической нагрузке, либо когда человек находится в бессознательном состоянии. В обоих случаях степень поражения паренхимы лёгких токсикантами, при прочих равных условиях, увеличивается. На депонирование частиц в лёгких оказывают влияние различные факторы. Среди них: анатомические особенности дыхательной системы (см. выше), характеристика аэрозоля, характер дыхания. Решающим фактором является размер частиц. Частицы диаметром более 50 мкм практически не проникают в дыхательные пути, до 10 мкм - оседают преимущественно в носоглотке (более 80%), 0,5 - 3 мкм - преимущественно в глубоких дыхательных путях и альвеолах (около 80%). Более мелкие частицы, как правило, не задерживаются в лёгких (минимальная задержка отмечается при диаметре частиц 0,25 - 0,30 мкм). Высокодисперсные аэрозоли (диаметр частиц менее 0,1 мкм) ведут себя практически как газы. Клиренс частиц оказывается определяющим в токсических эффектах ингалируемых агентов. Под клиренсом в данном случае понимают элиминацию частиц из организма или перемещение их в другие органы после первичного депонирования в дыхательных путях. В целом, частицы, хорошо растворимых в воде веществ, и газы абсорбируются эпителиальным слоем и затем проникают в кровь. Клиренс нерастворимых веществ зависит от того, где абсорбированы частицы. Если максимум абсорбции осуществляется в носоглотке и крупных воздухоносных путях, эпителий которых имеет микроворсинки (см. выше), частицы удаляются с помощью восходящего мукоцилиарного тока в полость рта, откуда поступают в желудочно-кишечный тракт. На уровне альвеол, где цилиарный эпителий отсутствует, клиренс частиц осуществляется макрофагами. Эти клетки ответственны за удаление и нейтрализацию частиц, попадающих в дыхательные пути. Они захватывают аэрозоль, а затем мигрируют в лимфатическую систему или к верхним дыхательным путям. Вследствие этого любое вещество, влияющее на количество макрофагов в лёгких или их функциональную активность, изменяет чувствительность дыхательной системы к патогенным факторам. Этапы взаимодействия макрофагов с частицами, следующие: хемотаксис, адгезия частиц к фагоциту, фагоцитоз частиц, образование первичных лизосом, слияние их со вторичными лизосомами, разрушение частиц. Повреждение защитных механизмов легких возможно при повреждении токсикантом любого из этих этапов.
10. Общеядовитое действие: определение, классификация по преимущественным механизмам, формы токсического процесса (на уровне клетки, органов и систем, целостного организма).
Общеядовитые - токсичные вещества, способные специфически нарушать процессы биоэнергетики, вызывая острое энергетическое голодание организма.
- яды крови (гемолитики; яды гемоглобина – сернистый ангидрид, оксид углерода);
- тканевые яды (ингибиторы ферментов дыхательной цепи – цианиды, сероводород, нитрилы; разобщители окисления и фосфорилирования – динитрофенол; истощающие запасы субстратов для процессов биоокисления – этиленхлоргидрин); острое нарушение энергетического обмена (блокировка цикла трикарбоновых кислот, нарушение механизмов фосфорилирования и т.д.)
Токсический эффект общеядовитых:
- характерное проявление тяжелых интоксикаций - кома-отек мозга-гипоксические судороги, приводящие к остановке дыхания и сердечной деятельности;
- общий результат токсоэффекта - формирование острого энергетического дефицита;
- отсутствие цианоза, розовая окраска кожи и слизистых (для большинства токсикантов);
- одинаковая динамика развития интоксикации (острая, острейшая) для большинства токсикантов;
Механизмы действия:
- нарушение транспорта кислорода кровью;
- разрушение эритроцитов;
- изменение структуры и функции гемоглобина;
- нарушение способности тканей эффективно использовать кислород в процессе биологического окисления;
Процессы, запускающие патологические механизмы:
- блокада ферментов энергообмена;
- разобщение окислительного фосфорилирования;
- нарушение мембран митохондрий;
- активация свободно-радикального и перекисного окисления липидов в митохондриях, в эритроцитах;
11. Нейротоксическое действие: определение, классификация (по обратимости поражения, по механизмам действия, по эффектам), формы токсического процесса (на уровне целостного организма).
Нейротоксичность - это свойство химических веществ, действуя на организм немеханическим путем, вызывать нарушение структуры и/или функций нервной системы. В основе развивающегося токсического процесса может лежать повреждение любого структурного элемента нервной системы путем модификации пластического, энергетического обменов, нарушения генерации, проведения нервного импульса по возбудимым мембранам, передачи сигнала в синапсах. Нейротоксичность может быть проявлением прямого, и опосредованного повреждением других органов и систем, действия токсикантов на нервную систему. Нейротоксичность присуща большинству известных веществ. Поэтому практически любая острая интоксикация в той или иной степени сопровождается нарушениями функций нервной системы. Вещества, для которых порог чувствительности собственно нервной системы (отдельных её гистологических и анатомических образований) существенно ниже, чем других органов и систем, и в основе интоксикации которыми лежат нарушения моторных, сенсорных функции нервной системы, памяти, мышления, эмоций, поведения, условно относят к нейротоксикантам.
Классификация "избирательных" нейротоксикантов в соответствии с механизмами их действия
| 1. Токсиканты, разрушающие определенные нервные клетки ЦНС - 6-гидроксидофамин: дофаминергические нейроны - 5,6-дигидрокситриптамин: серотонинергические нейроны - капсаицин: нейроны, синтезирующие субстанцию Р - 3-ацетилпиридин: нейроны олив мозга |
2. Токсиканты, действующие на специфические рецепторы:
А. Антагонисты:
- курарин,  -бунгаротоксин, эрабутоксин: Н-холинорецепторы
- атропин, скополамин, хинуклединилбензилат: М-холинорецепторы
- ДЛК, псилоцибин: серотонинергические рецепторы
- бициклофосфаты, норборнан, пикротоксин, бикукуллин: ГАМК-рецепторы
- стрихнин: глициновые рецепторы
Б. Агонисты:
- никотин, анабазин: Н-холинорецепторы
- ФОС, карбаматы: М- и Н-холинорецепторы
- каиновая кислота и её аналоги: рецепторы глютамата -бунгаротоксин, эрабутоксин: Н-холинорецепторы
- атропин, скополамин, хинуклединилбензилат: М-холинорецепторы
- ДЛК, псилоцибин: серотонинергические рецепторы
- бициклофосфаты, норборнан, пикротоксин, бикукуллин: ГАМК-рецепторы
- стрихнин: глициновые рецепторы
Б. Агонисты:
- никотин, анабазин: Н-холинорецепторы
- ФОС, карбаматы: М- и Н-холинорецепторы
- каиновая кислота и её аналоги: рецепторы глютамата
|
| 3. Токсиканты, действующие на пресинаптические структуры: - ботулотоксин, кротоксин: Н-холинергические синапсы - резерпин: катехоламинергические синапсы |
| 4. Токсиканты, действующие на натриевые каналы: А. Блокаторы проницаемости: - тетродотоксин - сакситоксин Б. Активаторы проницаемости: - аконитин - вератридин - батрахотоксин - токсины скорпионов |
| 5. Токсины, действующие на калиевые каналы: А. Блокаторы проницаемости: - аминопиридин - новокаин и его аналоги Б. Активаторы проницаемости: - тетраэтиламмоний - пентилентетразол |
| 6. Токсиканты, нарушающие биоэнергетику мозга: - цианиды, сульфиды - фторуксусная кислота - динитрофенол |
| 7. Токсиканты, угнетающие аксональный транспорт: - колхицин - цитохалазин |
| 8. Токсиканты, блокирующие митозы - метилазоксиметанол-гликозид (циказин) |
Конвульсанты
- Конвульсанты, активирующие возбуждающие процессы в ЦНС
- Вещества, действующие на возбудимые мембраны и нарушающие механизмы ионного транспорта (Пентилентетразол (метразол), Оуабаин, Фторэтил (гексафтордиэтиловый эфир))
- Вещества, активирующие холинэргические структуры мозга (ФОС, Карбаматы)
- Вещества, активирующие глютаматэргические структуры мозга
- Конвульсанты, блокирующие тормозные процессы в ЦНС
- Конвульсанты, действующие на ГАМК-эргический синапс.
- Антагонисты ГАМК (Бикукуллин, Судорожные барбитураты, Пикротоксин, Тетраметилендисульфотетрамин (дисульфотетразаадаматнтан, ДСТА), Бициклические фосфорорганические соединения (БЦФ), Норборнан)
- Ингибиторы синтеза ГАМК (Вещества, блокирующие высвобождения ГАМК из нервных окончаний (Тетанотоксин))
- Конвульсанты, действующие на глицинергические синапсы (Стрихнин)
- Вещества, нарушающие процессы биоэнергетики в мозге (Фторорганические соединения)
Наркотики (Седативно-гипнотическй эффект)
Психодислептики
- Эйфориогены - тетрагидроканнабинол
Галлюциногены
- Диэтиламид лизергиновой кислоты (ДЛК)
- Делириогены (BZ, Фенциклидин)
Все вещества, нарушающие передачу нервных импульсов в холинергических и катехоламинергических синапсах периферического отдела нервной системы, вызывают рассматриваемые эффекты. Свойства большинства этих веществ хорошо известны из курса фармакологии. К числу наиболее токсичных из известных токсикантов относятся некоторые карбаматы (см. выше), нейротоксины, выделенные из яда змей, и ботулотоксин.
Яды змей, относящихся к семейству Elapidae (тигровая змея, тайпан, морские змеи), содержат нейротоксины, избирательно действующие на механизмы передачи нервного импульса в холинэргических нервно-мышечных синапсах (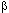 -бунгаротоксин, Кротоксин, Нотексин, Тайпоксин)
-бунгаротоксин, Кротоксин, Нотексин, Тайпоксин)
Все перечисленные в таблице токсины проявляют активность фосфолипаз А2, причем каталитический центр энзимов является функционально значимым для реализации их токсического действия. Интересно отметить, что большинство известных фосфолипаз А2, выделяемых из других источников (поджелудочной железы млекопитающих, пчелиного яда и т.д.), не смотря на высокую специфическую энзиматическую активность, не обладают нейротоксичностью.
Полагают, что нейротоксические фосфолипазы специфически связываются с определенными сайтами пресинаптической мембраны, а затем вызывают неспецифическое разрушение фосфоглицеридов мембраны вокруг сайта, инактивируя тем самым важные в функциональном плане структуры синапса. Опыты, выполненные на изолированных синаптосомах указывают, что одной из таких структур может являться система эффлюкса Са2+ в клетку и клеточные органеллы или каналы для других ионов, в частности К+. Полагают также, что для реализации токсического действия токсины должны попасть внутрь нервных терминалий с помощью механизма специфического эндоцитоза, где и вызывают повреждение синаптосом и митохондрий, нормальная функциональная активность которых необходима для экзоцитоза ацетилхолина. Поскольку нетоксичные фосфолипазы А2 неспецифически связываются с фосфоглицеридами любых, в том числе и несинаптических, биологических мембран, они не обладают свойствами нейротоксикантов.
Различные токсины, вероятно, связываются с различными сайтами пресинаптических структур. Так, одновременная инкубация биопрепарата с двумя нейротоксическими фосфолипазами А2 вызывает блок проведения импульса со значительно большей скоростью, чем с двойной дозой каждого из нейротоксинов в отдельности.
За исключением 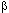 -бунгаротоксина рассматриваемые нейротоксины обладают также миотоксическим действием на скелетную мускулатуру млекопитающих. Внутримышечное введение веществ сопровождается острой некротической миопатией в области инъекции.
-бунгаротоксина рассматриваемые нейротоксины обладают также миотоксическим действием на скелетную мускулатуру млекопитающих. Внутримышечное введение веществ сопровождается острой некротической миопатией в области инъекции.
В настоящее время бунгаротоксин, кротоксин, тайпоксин широко используются в практике лабораторных исследований физиологии и биохимии синапсов.
13. Нервно-паралитическое действие: определение, классификация по механизмам токсического действия, формы токсического процесса.
| Активация процессов возбуждения | Угнетение процессов торможения |
| - прямая активация возбудимых мембран нервных клеток; - активация постсинаптических рецепторов возбуждающих нейромедиаторов; - увеличение количества возбуждающего нейромедиатора, высвобождающегося в синаптическую щель при прохождении нервного импульса; - пролонгация действия возбуждающего нейромедиатора в следствие угнетения механизмов разрушения или реаптейка; - повышение чувствительности постсинаптических рецепторов к возбуждающему нейромедиатору; - снижение потенциала покоя постсинаптических мембран клеток; | - блокада постсинаптических рецепторов тормозных нейромедиаторов; - уменьшение количества тормозного нейромедиатора, высвобождающегося в синаптическую щель при прохождении нервного импульса; - блок высвобождения тормозного нейромедиатора; - понижение чувствительности постсинаптических рецепторов к тормозному нейромедиатору; - сокращение продолжительности действия тормозного нейромедиатора в результате активации механизмов разрушения и реаптейка |
| Механизмы действия | Вещества |
| 1. Активация возбуждающих систем мозга: -прямое действие на возбудимые мембраны, изменение ионной проводимости; -селективный постсинаптический антагонизм с ГАМК -угнетение активности холинэстеразы и накопление ацетилхолина в синаптической щели -открытие Na+ каналов в результате прямого действия на возбудимые мембраны -стимуляция рецепторов возбуждающих аминокислот (глютамата, аспартата) -усиление проницаемости возбудимых мембран для Na+ путем вытеснения Са2+ с поверхности возбудимых мембран 2. Блокада тормозных систем мозга А. Угнетение ГАМК-рецепторов: -постсинаптический антагонизм с ГАМК путем действия на ГАМК-рецепторы -постсинаптический антагонизм с ГАМК в результате действия на барбитуровые рецепторы -усиление инфлюкса Ca2+ в нервные терминалии и активация выброса возбуждающих нейромедиаторов Б. Угнетение синтеза ГАМК или её высвобождения: -блокада высвобождения ГАМК из нервных окончаний -угнетение активности декарбоксилазы глютаминовой кислоты (ДГК), глютамилцистеинсинтетазы и цистатионазы -угнетение активности ДГК -усиление активности ГАМК-трансаминазы -нарушение метаболизма ГАМК в следствие угнетения активности пиридоксалькиназы В. Действие на глицинергические рецеапторы: -действие на глицин-зависимый ионофорный комплекс и нарушение проницаемости возбудимых мембран для Cl- 3. Нарушение энергетического обмена в мозге и в следствие этого механизмов ионного транспорта 4. Нарушение механизмов ионного транспорта: -угнетение активности Na+-K+-АТФазы | пентилентетразол и его аналоги антихолинэстеразные вещества фторэтил каиновая кислота, иботеновая кислота, N-метил-D-аспартат пикротоксин, бикукуллин, бициклофосфаты, норборнан судорожные барбитураты** тетанотоксин аллилглицин 3-меркаптопропионовая кислота гидразин, тиосемикарбазид и др. стрихнин, бруцин фторацетат, цианиды, сулфиды, динитрофенол и т.д. оуабаин |
14. Инкапаситанты: определение, классификация, основные формы токсического процесса. Медико-тактическая характеристика очагов поражения. Специфическая профилактика поражений. Принципы организации оказания неотложной помощи.
Инкапаситанты – вещества, временно выводящие из строя живую силу противника и не уничтожающие ее;
1) Ирританты (стерниты и лакриматоры) – на минуты или до суток;
2) Вещества калечущего действия (микстоксин Т2);
3) Дисрегуляторы (психотомиметики – 7-10 дней (симпатомиметики, гликолаты, фентанил и его наркопроизводные); физиканты (нейролептики, треморогены, эметики – рвотогенетики));
Общие действия:
- разница между LCt50 и ICt50, LD50 и ID50 в несколько порядков;
- эффективность малых доз;
- действие на ЦНС первично и не сопровождается соматическими изменениями;
- вызывает вегетативные расстройства;
- действие обратимо у психически здоровых людей;
Формы токсического процесса:
Ирританты:
Психотомиметики: извращают психические процессы, делают поведение людей неадекватным ситуации;
Физиканты: обездвиживающее действие;
Очаг: нестойкий (стойкий), несмертельный, быстрого действия.
Профилактика: противогаз, ЧСО ИПП, изъятие оружия у пораженных, успокоить их.
Помощь: галантамин (0,5%-2 мл), эзерин (0,05%-2 мл) – ингибиторы холинэстеразы, проникающие через ГЭБ, симптоматическое лечение – бета-адреноблокаторы (анаприлин), пирроксан, периферические антихолинэстеразы (прозерин), борьба с психомоторным возбуждением – трифтазин (0,2% - 1,0 мл), коррекция АД.
15. Гипоксия как лидирующий фактор токсического процесса. Характеристика гипоксий, формирующихся при интоксикации: классификация, общие механизмы. Принципы оказания помощи. Порядок проведения оксигенотерапии.
Гипоксия является одним из наиболее общих патогенетических факторов в процессах, нарушающих то или иное звено внешнего или внутреннего (тканевого) дыхания. Первичная причина гипоксии — абсолютный или относительный недостаток кислорода в клетках, что приводит к расстройству электрогенеза в возбудимых мембранах и разобщению окислительного фосфорилирования. При этом возникают вторичные изменения, которые характеризуются нарушением гемодинамики и микроциркуляции, потерями ферментов клетками, повреждением мембран лизосом с выходом аутолитических энзимов. Активация свободнорадикальных реакций приводит к окислению липидов мембран и дальнейшему нарушению их функции. В 1948 г. предложена Питерсом и Ван-Слайком классификация различных форм гипоксии по патогенетическому принципу:
1. Гипоксическая гипоксия: а) от понижения парциального давления кислорода во вдыхаемом воздухе; б) в результате затруднения поступления кислорода в кровь через дыхательные пути; в) вследствие расстройства дыхания.
2. Гемическая гипоксия: а) анемический тип; б) в результате инактивации гемоглобина (характеризуется уменьшением кислородной емкости крови).
3. Циркуляторная гипоксия: а) застойная форма; б) ишемическая форма.
4. Тканевая гипоксия, при которой нарушаются процессы потребления кислорода тканями в связи с подавлением функциональной активности различных дыхательных ферментов.
Наряду с указанным, И. Р. Петров и др. выделяют смешанную форму гипоксии. По течению гипоксию делят на молниеносную (например при вдыхании чистых инертных газов), острую и хроническую.
При снижении содержания кислорода в артериальной крови и в тканях включаются компенсаторные механизмы, направленные на устранение кислородной недостаточности. К ним относятся дыхательные, сердечно-сосудистые, кровяные и тканевые реакции, которые устраняют возникшее понижение рО2. При максимальном напряжении всех этих механизмов снабжение тканей кислородом может увеличиться в сравнении с нормой в 16—18 раз.
В развитии гипоксии различают две стадии компенсации и декомпенсации. В стадии декомпенсации кислородного голодания развиваются патологические изменения в важнейших системах и органах, наиболее чувствительных к недостатку кислорода. Так, при гипоксической гипоксии нарушение функции центральной нервной системы представляет непосредственную опасность для жизни человека. Как правило, вслед за изменениями в центральной нервной системе при острой гипоксии наблюдаются нарушения функций сердечно-сосудистой и дыхательной систем.
Изменение метаболизма при гипоксии характеризуется активацией анаэробного окисления, что приводит к нарушению кислотно-основного состояния, повышению содержания недоокис-ленных продуктов в крови и в моче (ацетоновые тела, молочная и пировиноградная кислоты, аминокислоты и т. д.). Эти изменения наступают в результате нарушения углеводного, белкового и жирового обменов.
При интоксикациях наблюдаются практически все типы кислородного голодания, которые могут проявляться в различных сочетаниях.
Так, гипоксическая гипоксия возникает при действии инертных газов, не оказывающих влияния на кровь (метан, азот); как следствие поражения дыхательных путей кислотами и щелочами, оксидами азота, удушающими ОВ и другими ядовитыми веществами, вызывающими отек легких; при действии ядовитых веществ, вызывающих угнетение функции дыхательного центра (например хлорированные углеводороды); при действии ядовитых веществ, вызывающих бронхоспазм (например ФОС и др.).
Гемическая гипоксия развивается как при уменьшении количества гемоглобина в результате действия гемолитических ядов (например мышьяковистый водород), так и при инактивации гемоглобина при отравлении оксидом углерода и метге-моглобинообразователями.
Циркуляторная гипоксия возникает при действии различных ядовитых веществ в результате нарушения сердечно-сосудистой деятельности (токсический шок, коллапс).
Тканевая гипоксия развивается вследствие паралича дыхательной функции клеток при отравлении цианидами, сероводородом и другими ядами.
Во всех случаях гипоксия сразу же начинает приобретать смешанный характер, так как при общих расстройствах функций организма страдают и другие звенья внешнего и внутреннего дыхания.
В случаях интоксикаций, протекающих с явлениями кислородного голодания, возникает необходимость в проведении рациональной терапии, направленной на ликвидацию гипоксии.
Лечебные мероприятия при гипоксии в основном сводятся к повышенной доставке кислорода тканям. Наиболее распространенным методом кислородной терапии является ингаляционный. Существующие методы ингаляции кислорода при нормальном барометрическом давлении, хотя и создают условия для относительно большего насыщения организма кислородом, не могут полностью устранить кислородное голодание при таких патологических состояниях, когда дефицит кислорода слишком велик. В этих случаях значительное преимущество имеет метод применения кислорода под давлением (оксигенобаротерапия). При этом появляется возможность резко увеличить содержание кислорода в организме п в значительной степени обеспечить его утилизацию независимо от количества активного гемоглобина.
Клинические и экспериментальные данные позволяют считать, что оксигенобаротерапия при различных отравлениях имеет неравнозначную ценность. Так, при кислородном голодании гемического типа (отравление СО, метгемоглобинообразователями) лечение кислородом под давлением дает положительные результаты даже без применения дополнительных средств помощи. При острых интоксикациях, приводящих к тканевой и циркуляторной гнпоксемии (отравление цианидами, ФОС), оксигенобаротерапию проводят с применением антидотов.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 1192; Нарушение авторских прав?; Мы поможем в написании вашей работы!