
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электронные эффекты в молекулах органических соединений
|
|
|
|
Электронные эффекты - смещение электронной плотности в молекуле,
ионе или радикале под влиянием заместителей.
Заместителем считается любой атом (кроме водорода) или группа атомов,
связанная с атомом углерода.
Различают индуктивный и мезомерный электронные эффекты заместителей.
Индуктивный эффект (I -эффeкт) - смещение электронной плотности по цепи
s-связей, обусловленное различиями в электроотрицательностях атомов.
Из-за слабой поляризуемости s-связей I -эффект быстро затухает с удалением от
заместителя и через 3-4 связи становится практически равным 0.
Индуктивный эффект называют отрицательным (- I), если заместитель уменьшает
электронную плотность на атоме углерода, с которым связан этот заместитель.
При этом заместитель приобретает частичный отрицательный заряд (d-), а атом
углерода - частичный положительный заряд (d+). Направление смещения
электронной плотности всех s-связей обозначается прямыми стрелками
(по линии связи) и символами частичных зарядов, индуцируемых заместителем:
H3C d+® Cl d- (- I -эффект атома хлора)
- I -эффект проявляют заместители, содержащие более электроотрицательные
атомы, чем атом углерода: -F, -Cl, -Br, -OH, -NH2, -NO2.
Индуктивный эффект называют положительным (+ I), если заместитель
увеличивает электронную плотность на атоме углерода, индуцируя на нем
частичный отрицательный заряд (d-), сам при этом приобретая заряд d+.
+ I -эффект проявляют атомы с низкой электроотрицательностью -Mg-, -Li;
алифатические углеводородные радикалы (-CH3, -C2H5).
Пример: H3C d- Li d+ (+ I -эффект атома лития)
Мезомерный эффект (М -эффект) - смещение электронной плотности по цепи
делокализованных (сопряженных) p-связей (см. раздел 4.10). Этот эффект
проявляют заместители, связанные с sp 2- или sp -гибридизованным атомом.
Благодаря подвижности p-электронов, М -эффект передается по цепи сопряжения
без затухания.
+ М -эффектом обладают заместители, повышающие электронную плотность в
сопряженной системе. К ним относятся группы, которые содержат атомы с
неподеленной парой электронов, способные к передаче этой пары электронов в
общую систему сопряжения. + М -эффект характерен для групп -OH и -NH2
(аним_6_4_1). 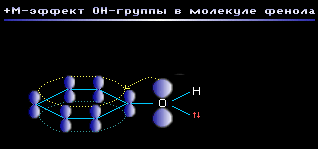
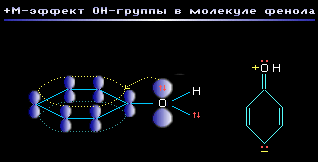
- М -эффект проявляют заместители с электроотрицательными атомами и
смещающие электронную плотность на себя. - М -эффект характерен для групп
-CH=O, -COOH, -NO2. Хотя эти группы имеют неподеленные электронные пары,
пространственное расположение орбиталей с этими электронами не позволяет
им вступать в систему сопряжения. Таким образом, в данном случае заместитель
может лишь оттягивать электроны из общей системы сопряжения за счет своей
более высокой электроотрицательности.
Для определения знака М-эффекта полезно строить атомно-орбитальные модели,
отражающие пространственную ориентацию орбиталей и возможности их
перекрывания (см. раздел 4.9). Так, если p-орбиталь кратной связи C=O и
sp 2-орбитали с неподеленными парами электронов атома кислорода
расположены перпендикулярно друг другу, то их перекрывание невозможно и
ни одна электронная пара кислорода не может передаваться в p-систему.
Следовательно, заместитель, содержащий группу C=O, проявляет не + М,
а - М -эффект (рис_6_4_1, 
аним_6_4_2). 
Направление смещения электронной плотности под влиянием М -эффекта
обозначается изогнутыми стрелками (рис_6_4_2).

27.Углеводы. Классификация.
Углеводы широко распространены в природе, они встречаются в свободной или связанной форме в любой растительной, животной, бактериальной клетке, они составляют три четверти биологического мира и примерно 60-80% калорийности пищевого рациона. Наиболее распространенный углевод - целлюлоза, структурный компонент деревьев и растений. Главный пищевой ингредиент - крахмал. Моносахариды встречаются в свободном виде в природе в небольших количествах; в основном они присутствуют как структурные единицы полисахаридов, входят в состав дисахаридов и олигосахаридов.
Выделяют простые углеводы, или сахара, включающие моносахариды и дисахариды, и сложные углеводы - полисахариды (крахмал, гликоген и некрахмальные полисахариды - клетчатка (целлюлоза и гемицеллюлоза, пектины).
Моносахариды содержат от 3 до 9 атомов углерода, наиболее распространены пентозы (5С) и гексозы (6С), а по функциональной группе альдозы и кетозы. Широко известные моносахариды - глюкоза, фруктоза, галактоза, рабиноза, арабиноза, ксилоза и Д-рибоза.
Глюкоза (виноградный сахар) в свободном виде содержится в ягодах и фруктах (в винограде - до 8%; в сливе, черешне - 5-6%; в меде - 36%). Из молекул глюкозы построены крахмал, гликоген, мальтоза; глюкоза является основной часть сахарозы, лактозы.
Фруктоза (плодовый сахар) содержится в чистом виде в пчелином меде (до 37%), винограде (7,7%), яблоках (5,5%); является основной частью сахарозы.
Галактоза - составная часть молочного сахара (лактозы), которая содержится в молоке млекопитающих, растительных тканях, семенах.
Арабиноза содержится в хвойных растениях, в свекловичном жоме, входит в пектиновые вещества, слизи, гумми (камеди), гемицеллюлозы.
Ксилоза (древесный сахар) содержится в хлопковой шелухе, кукурузных кочерыжках. Ксилоза входит в состав пентозанов. Соединяясь с фосфором, ксилоза переходит в активные соединения, играющие важную роль во взаимопревращениях сахаров.
В ряду моносахаридов особое место занимает D-рибоза. Почему природа всем сахарам предпочла рибозу - пока не ясно, но именно она служит универсальным компонентом главных биологически активных молекул, ответственных за передачу наследственной информации, - рибонуклеиновой (РНК) и дезоксирибонуклеиновой (ДНК) кислот; входит она и в состав АТФ и АДФ, с помощью которых в любом живом организме запасается и переносится химическая энергия. Замена в АТФ одного из фосфатных остатков на пиридиновый фрагмент приводит к образованию еще одного важного агента - НАД - вещества, принимающего непосредственное участие в протекании жизненно важных окислительно-восстановительных процессов. Еще один ключевой агент - рибулоза 1,5-дифосфат. Это соединение участвует в процессах ассимиляции углекислого газа растениями.
Полисахариды. Различают полисахариды (олигосахариды) I и II порядков (полиозы).
Олигосахариды. Это полисахариды I порядка, молекулы которых содержат от 2 до 10 остатков моносахаридов, соединенных гликозидными связями. В соответствии с этим различают дисахариды, трисахариды и т. д.
Дисахариды - сложные сахара, каждая молекула которых при гидролизе распадается на две молекулы моносахаридов. Дисахариды, наряду с полисахаридами, являются одним из основных источников углеводов в пище человека и животных. По строению дисахариды являются гликозидами, в которых две молекулы моносахаридов соединены гликозидной связью.
Среди дисахаридов особенно широко известны мальтоза, сахароза и лактоза. Мальтоза, являющаяся а-глюкопиранозил-(1,4)-а-глюкопиранозой, образуется в качестве промежуточного продукта при действии амилаз на крахмал (или гликоген).
Одним из наиболее распространенных дисахаридов является сахароза - обычный пищевой сахар. Молекула сахарозы состоит из одного остатка а-Э-глюкозы и одного остатка Р-Э-фруктозы.
В отличие от большинства дисахаридов, сахароза не имеет свободного полуацетального гидроксила и не обладает восстанавливающими свойствами.
Дисахарид лактоза содержится только в молоке и состоит из Р-Э-галактозы и Э-глюкозы.
Среди природных трисахаридов наиболее известна раффиноза (содержащая остатки фруктозы, глюкозы и галактозы). Она находится в значительных количествах в сахарной свекле и во многих других растениях, в частности в бобовых. В целом олигосахариды, присутствующие в растительных тканях, разнообразнее по своему составу, чем олигосахариды животных тканей.
Полисахариды II порядка разделяются на структурные и резервные. К первым относится целлюлоза, а к резервным - гликоген (у животных) и крахмал (у растений).
Крахмал представляет собой комплекс из линейной амилозы (10-30%) и разветвленного амилопектина (70-90%), построенных из остатков молекулы глюкозы (а-амилоза и амилопектин в линейных цепях а-1,4-связами, амилопектин в точках ветвления межцепочными а-1,6-связами), общая формула которых С6Н10О5п.
Хлеб, картофель, крупы и овощи - главный энергетический ресурс организма человека.
Гликоген - полисахарид, широко распространенный в тканях животных, близкий по своему строению амилопектину (сильно разветвленные цепочки через каждые 3-4 звена, общее количество гликозидных остатков 5-50 тыс.)
Целлюлоза (клетчатка) является распространенным растительным гомополисахаридом, выполняет роль опорного материала растений (скелет растений). Древесина наполовину состоит из клетчатки и связанного с нею лигнина, это биополимер линейного характера, содержащий 600-900 остатков глюкозы, соединенных Р-1,4-гликозидными связами.
Декстраны - гомополисахариды, построенные из остатков Э-глюкозы с доминирующим типом гликозидной связи. Декстран образуется из сахарозы и крахмала.
Пентозаны - целлюлозоподобные полисахариды, построенные из ксилозы, арабинозы и других пентоз. Богаты пентозанами скорлупа орехов, подсолнухов, кукурузные кочерыжки, солома, рожь.
Инулин - высокомолекулярный углевод, растворимый в воде. Содержится в клубнях земляной груши, георгинов, в корнях одуванчика, кок-сагыза, цикория, артишоках.
Пектиновые вещества, содержащиеся в растительных соках и плодах, представляют собой гетерополисахариды, построенные из остатков галактуроновой кислоты, соединенных а-(1,4)-гликозидными связями. Карбоксильные группы галактуроновой кислоты в той или иной степени этерифицированы метиловым спиртом. В зависимости от этого существует следующая классификация пектиновых веществ:
- протопектин - нерастворимое в воде соединение сложного химического состава (в протопектине длинная цепь полигалактуроновой кислоты связана с другими веществами: целлюлозой, арабаном, галактаном и другими полиозами, а также с белковыми веществами);
- пектиновые кислоты — это полигалактуроновые кислоты, в малой степени этерифицированные остатки метанола;
- пектин представляет собой почти полностью этерифицированную пектиновую кислоту.
Пектиновые вещества составляют основу фруктовых гелей. Пектины растворимы в воде, образуют коллоидные растворы. Протопектин нерастворим в воде, молекулярная масса 20-30 тыс. дальтон.
К гемицеллюлозам относятся разнообразные по химической структуре гетерополисахариды растений: глюкоманнаны, галактоманнаны и ксиланы, содержащие в боковых цепях арабинозу, глюкозу и т. д. В растениях гемицеллюлозы, как правило, сопутствуют целлюлозе и лигнину, причем ксиланы и глюкоманнаны прочно адсорбируются на поверхности целлюлозы.
Гемицеллюлозы, выделяемые из различных растений, отличаются по структуре. В деревьях и семенах они представлены линейными глюкоманнами, содержащими остатки - Э-маннозы и -Э-глюкозы, соединенных -(1,4)-гликозидными связями. В травах и древесине обнаружены гемицеллюлозы, цепи которых построены из остатков ксилопираноз, соединенных -(1,4)-гликозидными связями, причем в основной цепи имеются различные разветвления.
Гликозиды - продукты, получающиеся при элиминации воды. Только очень малые количества гликозидов встречаются в питании человека. Однако их значение часто зависит не от количества, а связано с физиологической ролью. Ряд природных гликозидов являются сильными пенообразователями и стабилизаторами, флавоноидные гликозиды могут придавать горький вкус и (или) определенный аромат и цвет пищевому продукту. S-гликозиды встречаются в природе в семенах горчицы и корня хрена. Они называются гликозинолаты. Аллилгликозинолат, наиболее известный из класса S-гликозидов, называется синигрин. Он придает определенный аромат пище, но есть работы, авторы которых полагают, что S-гликозиды и (или) продукты их распада могут быть отнесены к пищевым токсикантам.
Небольшое количество левоглюкозана образуется в условиях пиролиза при обжарке и выпечке мучных изделий и нагревании сахаров и сахарных сиропов при высокой температуре. Большие количества в пище нежелательны из-за горького вкуса.
Другой класс гликозидов, важных с точки зрения гигиены питания, - цианогенные гликозиды. Это соединения, которые образуют цианистый водород (HCN) при деградации in vivo; они достаточно широко представлены в природе (семена горького миндаля, маниок, сорго, косточки персиков, абрикосов и др.). Цианиды калия и натрия, образующиеся при деградации этих гликозидов, обычно детоксицируется превращениями в тиоцианат. Эта реакция включает С№-ион, SO-ион и фермент S-трансферузу. Однако, если путь детоксинации подавляется введением большого количества гликозида, может появиться токсичность. Были отмечены отравления как результат потребления маниока, горького миндаля; отравление крупного рогатого скота при потреблении незрелого проса или сорго.
Идеальная защита от цианидного отравления - исключить (или почти исключить) цианогенную пищу. Эти пищевые продукты должны храниться только очень короткое время. Надо принимать меры, чтобы не было «побитых» после уборки плодов. Плоды должны быть тщательно отобраны и затем хорошо промыты, чтобы удалить цианид.
28.Индуктивный эффект заместителей
Индуктивный эффект (I -эффект)
Известно, что полярная ковалентная связь образуется между атомами с различной электроотрицательностью. Наличие в молекуле полярной s-связи вызывает поляризацию ближайших двух–трех s-связей и ведет к возникновению частичных зарядов d+ (дельта плюс) или d- (дельта минус) на соседних атомах. Направление смещения электронной плотности всех s-связей обозначается прямыми стрелками (по линии связи) и символами частичных зарядов, индуцируемых заместителем:
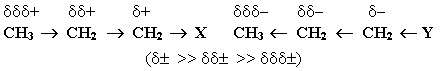
Таким образом, заместители (X или Y) вызывают поляризацию не только "своей", но и соседних связей. Такой вид передачи влияния атомов, приводящий к поляризации ковалентных связей и индуцированию зарядов на атомах, называется индуктивным (индукционным) электронным эффектом.
- Индуктивный эффект - смещение электронной плотности по цепи s-связей, которое обусловлено различиями в электроотрицательностях атомов.
Из-за слабой поляризуемости s-связей I -эффект быстро затухает с удалением от заместителя и через 3-4 связи становится практически равным 0.
Индуктивный эффект называют отрицательным (– I), если заместитель уменьшает электронную плотность на атоме углерода, с которым связан этот заместитель. При этом заместитель приобретает частичный отрицательный заряд (d-), а атом углерода - частичный положительный заряд (d+).
Например:

Индуктивный эффект называется положительным (+ I), если заместитель увеличивает электронную плотность на атоме углерода, индуцируя на нем частичный отрицательный заряд d-, сам при этом приобретая заряд d+.
Направление (знак) I -эффекта заместителя качественно оценивается путем сравнения со стандартом - атомом водорода, индуктивный эффект которого принят за 0.
- – I -эффект проявляют заместители, которые содержат более электроотрицательные атомы, чем атом углерода:
-F, -Cl, -Br, -OH, -NH2, -NO2, >C=O, -COOH и др.
- + I -эффект проявляют заместители, содержащие атомы с низкой электроотрицательностью:
-Mg-, -Li; алифатические углеводородные радикалы (-CH3, -C2H5) и т.п.
29.α-Аминокислоты.
Аминокислоты, органические кислоты, содержащие одну или несколько аминогрупп. В зависимости от природы кислотной функции аминокислоты подразделяют на аминокарбоновые, например H2N(CH2)5COOH, аминосульфоновые, например H2N(CH2)2SO3H, аминофосфоновые, например H2NCH[Р(О)(ОН)2]2, и аминоарсиновые, например H2NC6H4AsO3H2. Согласно правилам ИЮПАК, название аминокислоты производят от названия соответствующей кислоты; взаимное расположение в углеродной цепи карбоксильной и аминной групп обозначают обычно цифрами, в некоторых случаях - греческими буквами. Однако, как правило, пользуются тривиальными названиями аминокислоты.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 6532; Нарушение авторских прав?; Мы поможем в написании вашей работы!