
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Контрольні завдання. 601. Які хімічні властивості характерні для металів.
|
|
|
|
МЕТАЛИ
601. Які хімічні властивості характерні для металів? Чим вони зумовлюються?
602. Як змінюються металічні властивості елементів за періодами і групами періодичної системи Д.І.Менделєєва зі збільшенням порядкового номеру? Дати пояснення на прикладі елементів I групи головної підгрупи та елементів III періоду.
603. Які хімічні властивості проявляють метали в окисно-відновних реакціях? Чим зумовлені такі властивості?
604. Які сполуки утворюються при взаємодії металів з киснем, воднем, галогенами, сіркою, азотом, вуглецем, кремнієм? Дати назву цим сполукам і написати рівняння реакцій їх утворення на прикладі металу кальцію.
605. В яких випадках метали реагують з водними розчинами солей інших металів? Написати рівняння реакції взаємодії цинку з розчином сульфату міді.
606. Які метали взаємодіють з розбавленими соляною та сірчаною кислотами? Навести два приклади такої взаємодії.
607. Як активні метали реагують з водою? Навести два приклади такої взаємодії.
608. Які метали можуть взаємодіяти як з кислотами так, і з основами? Написати рівняння реакцій взаємодії такого металу з кислотою та лугом.
609. В якому стані метали зустрічаються в природі? Які метали зустрічаються в природі в самородному стані?
610. Чому такі активні метали як цинк та алюміній не реагують з водою? Як їх перевести в активний стан?
611. Чим зумовлені характерні фізичні властивості металів: електропровідність, теплопровідність і пластичність?
612. Чому метали застосовуються, в основному, не в чистому вигляді, а у вигляді сплавів?
613. У ванночку з водою опустили 1 г натрію. Написати рівняння реакції. Які речовини і в яких кількостях утворяться?
614. Чому мідь можна одержати електролізом розчину її солі, а натрій тільки електролізом розплаву його солі? Відповідь підтвердити рівняннями реакцій, що відбуваються на електродах.
615. Який з лужних металів є найбільш активним відновником? Чим це зумовлюється?
616. Як з хлориду калію можна одержати металічний калій, гідроксид калію? Написати відповіді рівняння реакцій.
617. Написати рівняння реакцій за допомогою яких можна здійснити наступні перетворення:
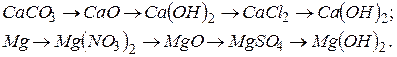
618. Як реагує алюміній з розбавленими та концентрованими сірчаною та азотною кислотами? Відповідь підтвердити відповідними рівняннями реакцій.
619. Які сполуки заліза можуть бути: а) тільки окисником, б) і окисником і відновником?
620. В яких кислотах розчиняється залізо? Написати відповідні рівняння реакцій.
НЕМЕТАЛИ
КОНТРОЛЬНІ ЗАВДАННЯ
621. На чому заснований поділ елементів періодичної системи на метали і неметали? Які елементи належать до неметалів? Де вони містяться в періодичній системі? Яку структуру має зовнішній електронний шар атомів неметалів?
622. Як змінюються неметалічні властивості елементів у періодах та групах? Показати на прикладах елементів 2-го та 3-го періодів та елементів головної підгрупи 7-ої групи. Як при цьому змінюється спорідненість до електрона та енергія іонізації?
623. Який ступінь окиснення можуть мати атоми неметалів у сполуках? Навести приклади. Які властивості виявляють сполуки неметалів – окисників чи відновників?
624. У вигляді яких молекул існують прості речовини неметали? Який агрегатний стан характерний для неметалів?
625. У чому полягають основні відмінності фізичних і хімічних властивостей металів та неметалів?
626. На прикладі 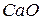 та
та 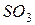 вказати, за якими властивостями оксиди металів відрізняються від оксидів неметалів. Написати відповідні рівняння реакцій.
вказати, за якими властивостями оксиди металів відрізняються від оксидів неметалів. Написати відповідні рівняння реакцій.
627. Які ступені окиснення може виявляти вуглець у своїх сполуках? Навести формули відповідних сполук. В яких реакціях виявляються відновні, а в яких окисні властивості вуглецю?
628. Які оксиди утворює вуглець? Як добувають вуглекислий газ у промисловості та в лабораторії? Навести відповідні рівняння реакцій.
629. Які молекули та іони знаходяться в розчині вуглекислого газу у воді? Скласти рівняння існуючої у цьому розчині рівноваги.
630. Які властивості характерні для вугільної кислоти? Які солі вона утворює? Яка розчинність солей вугільної кислоти? Скласти рівняння реакцій утворення карбонату та гідрокарбонату кальцію. Що відбувається з цими солями при нагріванні? Скласти відповідні рівняння реакцій.
631. Розчин карбонату натрію забарвлює лакмус в синій колір. Чому? Скласти молекулярне та іонне рівняння процесу, що відбувається при розчиненні карбонату натрію у воді.
632. Описати фізичні та хімічні властивості кремнію, вказавши його відношення до води, кислот та лугів. Скласти рівняння відповідних реакцій.
633. Порівняти неметалічні властивості кремнію та вуглецю. В яких реакціях кремній виявляє окисні, а в яких відновні властивості. Підтвердити рівняннями реакцій.
634. При пропусканні діоксиду вуглецю через вапняну воду (розчин  ) утворюється осад, який при подальшому пропусканні
) утворюється осад, який при подальшому пропусканні 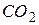 розчиняється. Дати пояснення цьому явищу. Скласти рівняння реакцій.
розчиняється. Дати пояснення цьому явищу. Скласти рівняння реакцій.
635. Який ступінь окиснення може виявляти кремній у своїх сполуках? Скласти рівняння реакцій, які треба провести для здійснення перетворень:
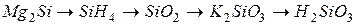
При якому з перетворень відбувається окисно-відновна реакція?
636. Вказати хімічний характер діоксиду кремнію. Як він відноситься до води, кислот, лугів? Як з діоксиду кремнію можна одержати: а) фторид кремнію; б) кремнієву кислоту? Скласти рівняння реакцій.
637. Чому водний розчин силікату натрію має лужне середовище? Скласти молекулярне та іонне рівняння реакції, що відбувається при розчиненні силікату натрію у воді. Яку технічну назву мають силікати натрію та калію? Де вони застосовуються?
638. Які вихідні речовини використовують для добування скла? Скласти рівняння реакцій, що відбуваються при утворенні скла.
639. Які кислоти відповідають діоксиду кремнію? У чому полягає особливість кремнієвих кислот порівняно з іншими кислотами? Як називаються солі кремнієвих кислот?.
640. З огляду на будову зовнішнього електронного шару охарактеризувати валентні можливості та ступені окиснення елементів VI групи головної підгрупи періодичної системи.
641. Записати рівняння реакцій, які відбуваються під час розчинення 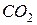 у воді. Які рівноваги встановлюються у цьому випадку? Як вплине збільшення тиску на зміщення рівноваги?
у воді. Які рівноваги встановлюються у цьому випадку? Як вплине збільшення тиску на зміщення рівноваги?
642. Карбонат кальцію розкладається при нагріванні на оксид кальцію і діоксид вуглецю. Яка маса природного вапняку, який містить 90% карбонату кальцію, необхідна для одержання 7,0 т негашеного вапна?
Відповідь: 13,9 т
643. Крізь розчин, що містить 7,4 г гідроксиду кальцію, пропустили 3,36 л діоксиду вуглецю, взятого за нормальних умов. Знайти загальну масу солей, що утворилися внаслідок реакції.
Відповідь: 13,1 г.
644. При розкладанні карбонату кальцію виділилось 11,2 л діоксиду вуглецю. Чому дорівнює маса гідроксиду калію, необхідна для зв’язування газу, що виділився, в карбонат?
645. Які сполуки називаються карбідами й силіцидами? Написати рівняння реакцій: а) карбіду алюмінію з водою; б) силіциду магнію з соляною кислотою. Чи є ці реакції окисно-відновними? Чому?
646. На підставі електронних рівнянь скласти рівняння реакції фосфору з азотною кислотою, враховуючи, що фосфор набуває найвищого ступеню окиснення, а азот ступеню окиснення +4.
647. Чому сірчиста кислота може виявляти як окисні, так і відновні властивості? На основі електронних рівнянь скласти рівняння реакцій 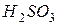 : а) з сірководнем; б) з хлором.
: а) з сірководнем; б) з хлором.
648. Як виявляє себе сірководень в окисно-відновних реакціях? Чому? Скласти електронні та молекулярні рівняння реакцій взаємодії розчину сірководню: а) з хлором; б) з киснем.
649. Чому азотиста кислота може виявляти як окисні, так і відновні властивості? На основі електронних рівнянь скласти рівняння реакцій 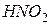 : а) з бромною водою; б) з
: а) з бромною водою; б) з 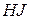 .
.
650. Які властивості в окисно-відновних реакціях виявляє сірчана кислота? Написати рівняння реакцій взаємодії розбавленої сірчаної кислоти з магнієм та концентрованої – з міддю. Вказати окисник і відновник.
651. В якій газоподібній сполуці азот виявляє свій найнижчий ступінь окиснення? Написати рівняння реакції одержання цієї сполуки при взаємодії хлориду амонію з гідроксидом калію. Де застосовується цей газ?
652. Як змінюються окисні властивості галогенів у підгрупі зверху вниз та відновні властивості їх негативно заряджених іонів? Чому? Скласти електронні і молекулярні рівняння реакцій: а) 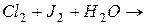 ; б)
; б) 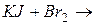 . Вказати окисник і відновник.
. Вказати окисник і відновник.
653. Як змінюються неметалічні властивості у підгрупі кисню від кисню до телуру? Чому? Чому кисень, як правило, виявляє валентність, що дорівнює 2, на відміну від своїх аналогів, які можуть виявляти валентність, що дорівнює 2, 4, 6?
654. Написати рівняння реакцій взаємодії металів різної активності з розбавленим та концентрованим розчинами сірчаної кислоти.
655. Яке застосування знаходить кремній? Скласти рівняння реакцій, які необхідно провести для здійснення наступних перетворень:
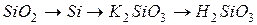
Рівняння окисно-відновних реакцій написати на основі електронних рівнянь.
656. Які з солей вугільної кислоти мають найбільше промислове застосування? Як одержати соду, виходячи з металічного натрію, соляної кислоти, мармуру та води? Чому в розчині соди лакмус набуває синього забарвлення? Відповідь підтвердити рівняннями відповідних реакцій.
657. Чим суттєво відрізняється дія розведеної азотної кислоти на метали від дії хлороводневої (соляної) та розведеної сірчаної кислот? Що є окисником у першому випадку, що – у двох інших? Навести приклади.
658. Що представляють собою силікати? Які виробництва відносяться до силікатної промисловості?
659. Які з солей кремнієвої кислоти мають найбільше промислове застосування? Що таке рідке скло? Як здійснити перетворення
 ?
?
660. Як одержують діоксид вуглецю в промисловості та в лабораторії? Написати рівняння відповідних реакцій та реакцій, за допомогою яких можна здійснити такі перетворення:
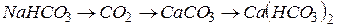
ТВЕРДІСТЬ ВОДИ
ОСНОВНІ ПОНЯТТЯ ТА ВИЗНАЧЕННЯ
Твердість води 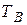
| - зумовлена наявністю іонів 
|
| Твердість води гідрокарбонатна, (тимчасова) | - зумовлена наявністю гідрокарбонатів кальцію і магнію 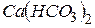 і і 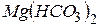
|
| Твердість води некарбонатна (постійна) | - зумовлена наявністю сульфатів і хлоридів кальцію і магнію (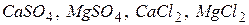 ) )
|
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 534; Нарушение авторских прав?; Мы поможем в написании вашей работы!