
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Будова молекули метану
|
|
|
|
Мал. 22 а Мал. 22 б
1s і 3 р – орбіталі другого рівня гібридизуються (вирівнюються за формою та енергією). Таке вирівнювання орбіталей називається sp3 – гібридизацією.. Експериментально доведено, щ всі чотири гібридні орбіталі атома Карбону в молекулі метану направлені одна відносно одної під тетраедричним кутами 109о28/. Така просторова направленість дозволяє їм перебувати на максимальній відстані один від одного. В результаті перекривання гібридних sp3 –орбіталей і s – орбіталей чотирьох атомів Гідрогену утворюється молекула з міцними ковалентними зв’язками (мал. 23.)
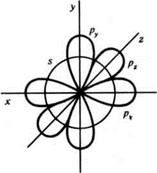


Схема утворення чотирьох гібридних орбіталей атома Карбону
.
109о28/
 а)
а) 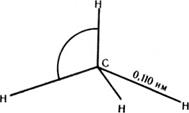 б)
б)
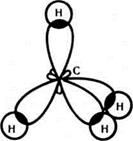
Мал. 23. Схема утворення 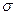 -зв'язків (а); геометрія молекули метану (б)
-зв'язків (а); геометрія молекули метану (б)
Як пояснити утворення подвійного зв’язку в молекулі етилену з точки зору електронної теорії? Фізичні методи дослідження показали, що в молекулі етилену всі ядра атомів розташовані в одній площині. Відстань між ядрами атомів Карбону складає 0,134 нм (в алканів 0,154 нм), а валентні кути в молекулі 120 о. Ці дані не відповідають уявленням про sp3 –гібридизацію. Очевидно, що у випадку подвійного зв’язку буде інший тип гібридизації, він називається sp2 –гібридизацією. При цьому гібридизації піддаються не всі орбіталі збудженого атома Карбону, а тільки три: s – орбіталь і дві р – орбіталі, вони розташовані в одній площині під кутом 120 о.
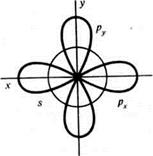
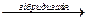
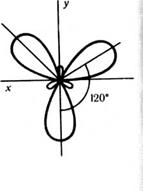
Схема утворення трьох гібридних електронних хмар атома Карбону.
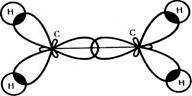
Схема утворення 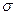 -зв'язків.
-зв'язків.
Мал.24
В кожного атома Карбону залишилося по одній негібридизованій р – орбіталі і тому її форма не змінилась. Ці орбіталі розташовані паралельно одна до одної і перпендикулярно до площини 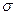 - зв’язків, вони частково перекриваються між собою над і під площиною
- зв’язків, вони частково перекриваються між собою над і під площиною 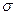 - зв’язків з утворенням нового
- зв’язків з утворенням нового 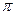 - зв’язку. З встановленням
- зв’язку. З встановленням 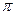 - зв’язку ядра атомів Карбону дещо стягуються, тому довжина подвійного зв’язку дорівнює 0,134 нм. (мал. 25.):
- зв’язку ядра атомів Карбону дещо стягуються, тому довжина подвійного зв’язку дорівнює 0,134 нм. (мал. 25.):
Схема утворення 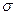 -зв'язків.
-зв'язків.


|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 1330; Нарушение авторских прав?; Мы поможем в написании вашей работы!