
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ковалентні зв’язки
|
|
|
|
1.Пептидні зв’язки – (- СО – NH -) виникають внаслідок взаємодії карбоксильних та 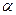 - аміногруп амінокислот, що утворюють пептидний ланцюг.
- аміногруп амінокислот, що утворюють пептидний ланцюг.
2.Дисульфідні зв’язки (- S – S -) – утворюються між залишками молекул цистеїну, що входять до одного або різних пептидних ланцюгів.
2.Нековалентні зв’язки та слабкі взаємодії – фізико – хімічні зв’язки, що беруть участь у взаємодії як певних частин одного пептидного ланцюга, так і різних, близько розташованих ланцюгів, утворюючи вищі рівні конформації білкових молекул.
1.Водневі зв’язки – виникають між двома електронегативними атомами за рахунок атома Гідрогену, ковалентно зв’язаного з одним із електронегативних атомів. Вони найчастіше утворюються між Гідрогеном, що входить до складу груп = NH, - OH, - SH та сусіднім атомом Оксигену, наприклад:
= N – H … O = C =
2. Йонні зв’язки – зв’язують між собою йонізовані амінні та карбоксильні групи.
3. Дипольні зв’язки – електростатичні взаємодії постійних чи індукованих диполів, які можуть виникати між радикалами полярних амінокислот (серину, цистеїну, тирозину тощо), що входять до складу білкових молекул.
4.Гідрофобні взаємодії – слабкі взаємодії. Що виникають між бічними радикалами таких амінокислот, як валін, лейцин, ізолейцин тощо за рахунок їх „виштовхування” з полярної (звичайно, водної) фази.
Первинна структура білків
Під первинною структурою білків розуміють послідовність сполучення залишків амінокислот у поліпептидному ланцюгу. У поняття первинної структури білка або пептиду входять його якісний та кількісний склад та порядок чергування окремих амінокислотних залишків. Порядок хімічного сполучення амінокислотних ланок – найбільш істотна причина різноманітності білків. Наприклад, для білка, в кому міститься лише 10 залишків різних амінокислот, можливе існування 3 628 800 ізомерів, які відрізняються порядком сполучення амінокислотних ланок.
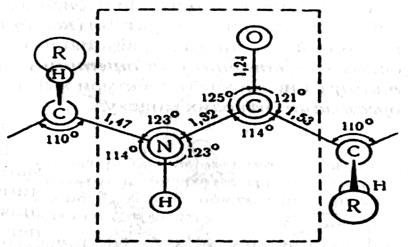
Мал. 14 Параметри структурних елементів поліпептидного ланцюга
(розміри подано в ангстремах; 1 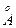 = 0,1 нм)
= 0,1 нм)
Вторинна структура білків – це ряд конформацій, утворення яких зумовлено, головним чином, водневими зв’язками між окремими ділянками пептидного ланцюга або різними поліпептидними ланцюгами. Розрізняють два основних типи впорядкованої вторинної структури білкових молекул: 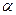 - спіраль та
- спіраль та 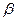 - структуру. (Мал. 15.)
- структуру. (Мал. 15.)
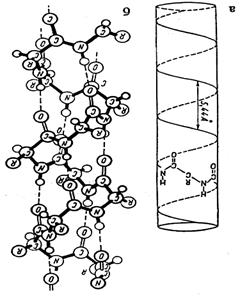
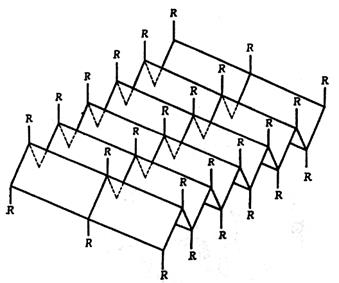
Мал.15. Модель вторинної структури поліпептидного ланцюга у вигляді
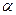 - спіралі (а) і
- спіралі (а) і 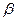 - конформації
- конформації
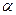 - Спіраль – конформація, яка утворюється при просторовому скручуванні поліпептидного ланцюга за рахунок водневих зв’язків, що виникають між С =О - та NH – групами поліпептидного ланцюга, що віддалені одна від одної на чотири амінокислотних залишки. Водневі зв’язки в
- Спіраль – конформація, яка утворюється при просторовому скручуванні поліпептидного ланцюга за рахунок водневих зв’язків, що виникають між С =О - та NH – групами поліпептидного ланцюга, що віддалені одна від одної на чотири амінокислотних залишки. Водневі зв’язки в 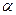 - спіралі спрямовані паралельно до осі молекули.
- спіралі спрямовані паралельно до осі молекули. 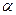 - Спіраль можна уявити собі у вигляді лінії, що йде по боковій поверхні уявного циліндра. На один оберт
- Спіраль можна уявити собі у вигляді лінії, що йде по боковій поверхні уявного циліндра. На один оберт 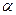 - спіралі припадає 3,6 амінокислотних залишків. Напрямок обертання поліпептидного ланцюга в природних білках – правий. Декілька білкових молекул із вторинною структурою у вигляді спіралей можуть взаємодіяти одна з одною, утворюючи міжмолекулярні комплекси, що являють собою суперспіралізовані (супервторинні) структури.
- спіралі припадає 3,6 амінокислотних залишків. Напрямок обертання поліпептидного ланцюга в природних білках – правий. Декілька білкових молекул із вторинною структурою у вигляді спіралей можуть взаємодіяти одна з одною, утворюючи міжмолекулярні комплекси, що являють собою суперспіралізовані (супервторинні) структури.
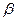 - Структура – структура типу складчастого шару, складається із зигзагоподібно розгорнутих поліпептидних ланцюгів, що розташовані поряд (двох або більшої кількості).
- Структура – структура типу складчастого шару, складається із зигзагоподібно розгорнутих поліпептидних ланцюгів, що розташовані поряд (двох або більшої кількості). 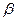 - Конформацію мають білки
- Конформацію мають білки 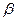 - кератини, які складаються з зигзагоподібних, антипаралельно орієнтованих поліпептидних ланцюгів. Представником
- кератини, які складаються з зигзагоподібних, антипаралельно орієнтованих поліпептидних ланцюгів. Представником  - кератинів є фіброїн – фібрилярний нерозчинний білок шовку та павутиння.
- кератинів є фіброїн – фібрилярний нерозчинний білок шовку та павутиння.
Третинна структура білків являє собою спосіб укладання в тримірному просторі поліпептидного ланцюга з певною вторинною структурою. Залежно від форми та особливостей тримірної просторової організації розрізняють глобулярні та фібрилярні білки.
Глобулярні білки – білки, що мають округлу (кулеподібну або еліпсоподібну) форму. Це альбумін сироватки крові, міоглобін м’язів, гемоглобін, більшість ферментних білків. Глобулярні білки побудовані з одного або з декількох зв’язаних дисульфід ними містками поліпептидних ланцюгів, що згорнуті в щільні кулеподібні форми.
Фібрилярні білки – білки, структурною особливістю яких є витягнута форма молекул. Вони схильні до утворення мультимолекулярних ниткоподібних комплексів – фібрил, що складаються з декількох паралельних поліпептидних ланцюгів.
Фібрилярні білки є структурними компонентами сполучної та інших опорних тканин організму. Прикладами структурних фібрилярних білків є колаген – найбільш розповсюджений білок організму людини, що становить до 30% загальної кількості тканинних білків, еластин сполучної тканини,  - кератин опірних тканин, епідермісу, шкіри, волосся.
- кератин опірних тканин, епідермісу, шкіри, волосся.
Четвертинна структура білків утворюється при об’єднанні (агрегації) декількох поліпептидних ланцюгів або протомерів, кожен з яких має свою характерну впорядковану конформацію.
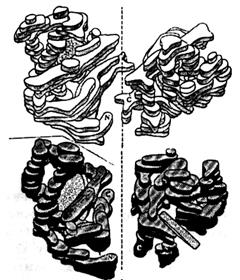
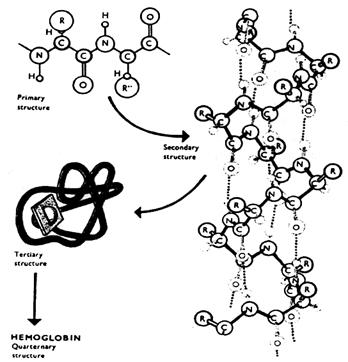
Мал. 16 Четвертинна структура молекули гемоглобіну
Білки з четвертинною структурою можуть включати як однакові протомери (гемоглобін), так і різні. У складі багатьох білків – ферментів містяться різні протомери, що виконують різні біохімічні функції (зокрема каталітичну та регуляторну).
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 1751; Нарушение авторских прав?; Мы поможем в написании вашей работы!