
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема 6. Фізико-хімія дисперсних систем та розчинів високомолекулярних сполук 6 страница
|
|
|
|
 Дозрівання
Дозрівання 
 Синерезис
Синерезис
Драглі з розчинів полімерів утворюються при додаванні електролітів або при їх випарюванні, охолодженні, обмеженому набуханні полімеру у низькомолекулярній рідині:
Додавання електроліту;
Концентрування;
Охолодження;

 ВМС
ВМС  Розчин ВМС
Розчин ВМС  Драглі
Драглі
 Обмежене набухання
Обмежене набухання
За певних умов (струшування, перемішування, вібрація, нагрівання) внутрішня структура часточок драглів руйнується і вони переходять в розчин (вільнодисперсну систему). Після припинення механічної дії під впливом теплового руху часточок і сил міжмолекулярної взаємодії ця структура знову відновлюється. Явище механічного руйнування драглів і наступного переходу золю в гель, називається тиксотропією. Цей процес можна зобразити схемою:
Механічна дія
  Гель Золь
Нагрівання Гель Золь
Нагрівання
|
Процес утворення драглів дуже поширений у природі. Багато складних біологічних і фізико-хімічних процесів супроводжуються желатинуванням. Через стадію желатинування утворюються гелі грунтів і осадові породи (каолін, глинозем тощо), в живих організмах і рослинах утворюються крохмаль, целюлоза, білкові речовини. Перебувають у стадії желатинування різноманітні харчові продукти (желе, мармелад, джем, сир, кисле молоко, плодові та овочеві соки, кисіль, холодець, хліб тощо).
Аерозолі. Дисперсні системи з газуватим дисперсійним середовищем, незалежно від агрегатного стану дисперсної фази (рідкої або твердої), називаються аерозолями. Системи з рідкою дисперсною фазою – це тумани, з твердою – дими, пил і порошки, якщо одночасно вони містять і рідкі і тверді часточки – смоги. В смогах рідка фаза конденсується на поверхні твердих часточок. Такі аерозолі частіше всього присутні в атмосфері великих промислових міст.
Тумани іноді називають фогом (імла), якщо вони достатньо густі і сильно погіршують видимість. Летку золу, продукти неповного згоряння або їх суміш (як тверді, так і рідкі) називають кіптявою або смоком.
Смог – це штучне слово, яке складене зі слів смок і фог, що використовується для визначення любого небажаного забруднення атмосфери. Існують два типи смогів – лос-анжелеський і лондонський; лос-анжелеський смог має фотохімічну природу і обумовлений випускними газами автомобілів, лондонський – обумовлений неповним згорянням вугілля і характеризується відносно високим вмістом диоксиду сульфуру і твердих часточок.

|
| Рис.6.35. Класифікація атмосферних забруднень за розмірами та основні методи визначення розмірів частинок |
Прийнято рахувати аерозольними системами, що містять часточки розміром 10-9 – 10-3 м. Системи з більш крупними часточками називають аерозавісами.
За розміром часточок, що складають аерозольну систему, усі аерозолі поділяють на високодисперсні (діаметр часточок менш ніж 10 нм), тонко дисперсні (10  d
d  100 нм) і грубо дисперсні (діаметр часточок більш ніж 100 нм). На рис.6.35 приведена класифікація атмосферних забруднювачів за розміром їх часточок. В природі аерозолі обумовлюють практично усі метерологічні, в тому числі грозові, явища. В сільському господарстві з використанням аерозолів пов’язані проблеми штучного дощування, застосування отрутохімікатів для боротьби зі шкідниками і хворобами рослин. В техніці – це очищення повітря, різних технологічних газових сумішей, вловлювання цінних матеріалів з газів, що викідаються. В биту і медицині – це застосування аерозольної форми препаратів, ліків, лаків, фарб, тощо. З проблемою захисту від аерозолів, які утворюються під час роботи атомних електростанцій, переробці руд, при згорянні палива, при аваріях в промисловості, вибухах військових речовин, викидів вулканічних газів і т.п., пов’язані ключові питання охорони здоров’я людей і захисту навколишнього середовища.
100 нм) і грубо дисперсні (діаметр часточок більш ніж 100 нм). На рис.6.35 приведена класифікація атмосферних забруднювачів за розміром їх часточок. В природі аерозолі обумовлюють практично усі метерологічні, в тому числі грозові, явища. В сільському господарстві з використанням аерозолів пов’язані проблеми штучного дощування, застосування отрутохімікатів для боротьби зі шкідниками і хворобами рослин. В техніці – це очищення повітря, різних технологічних газових сумішей, вловлювання цінних матеріалів з газів, що викідаються. В биту і медицині – це застосування аерозольної форми препаратів, ліків, лаків, фарб, тощо. З проблемою захисту від аерозолів, які утворюються під час роботи атомних електростанцій, переробці руд, при згорянні палива, при аваріях в промисловості, вибухах військових речовин, викидів вулканічних газів і т.п., пов’язані ключові питання охорони здоров’я людей і захисту навколишнього середовища.
Більшість специфічних властивостей аерозолів пов’язані з особливостями дисперсійного середовища – повітря, його низькою в’язкістю і електропровідністю (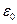 = 8,85 . 1012 ф/м). Наявність зарядів на поверхні аерозольних часточок обумовлює ряд важливих явищ.
= 8,85 . 1012 ф/м). Наявність зарядів на поверхні аерозольних часточок обумовлює ряд важливих явищ.
Осідання аерозольних часточок (наприклад, краплин туману або дощу) обумовлює появу електричного поля з напругою Е порядку кВ на см. Ці значення Е можуть бути і більше, в цьому випадку можливий пробій повітря – блискавка.
Реальні аерозолі полідисперсні. Тому при їх седиментації спостерігається ортокінетична коагуляція часточок (захоплення крупними часточками більш мілких) (рис.6.36, а). Седиментуюча велика часточка, що утворилася, внаслідок опору повітря і сил гравітації витягується до тих пір поки не перевищується межа стійкості рідкого циліндра і ділиться на дві менших часточки (рис.6.36, б). Ці часточки, що утворилися знову збільшуються в процесі седиментації, а потім подрібнюються. Такий процес, що повторюється, прискорює швидкість седиментації аерозольних часточок до їх повного осідання.
 а)
а)
|  б)
б)
|
| Рис.6.36. Руйнування аерозолів: а) ортокінетична коагуляція; б) розкладання великої часточки на дві менших розмірів |
Такий механізм відбувається в атмосфері при руйнуванні туману, дощових хмар. Залежно від концентрації аерозольних часточок і температурних умов відбувається випадання води у вигляді роси, дощу, снігу чи граду. На практиці за таким механізмом руйнують грозові хмари, що несуть загрозу випадання граду і пошкодження сільськогосподарських угідь. Для цього у верхівку хмар за допомогою зенітних гармат доставляють зародкоутворювачі (кристали йодиду аргентуму, хлориду кальцію, твердий диоксиген карбону і деякі інші речовини колоїдного розміру), які викликають швидку конденсацію водяної пари і зростання крапель води (або кристаликів льоду в переохолоджених хмарах), що приводить до їх випадання. Аналогічним чином можна розсіювати тумани, використовуючи для цього авіатехніку.
Існуючі в атмосферному повітрі мікроорганізми, бактерії, віруси, пилок, насіння і спори рослин представляють собою так звані біологічні аерозолі, які переміщуються на величезні відстані і часто є носіямиінфекційних захворювань і епідемій.
Для аерозолів характерні такі специфічні явища, як термофорез та термопреципітація. Термофорез – переміщення аерозольних часточок у напрямку зниження температури, яке обумовлене тиском більш швидких молекул газу з „гарячого боку”. У великих часточках коли поверхня нагріта нерівномірно, то вздовж неї у напрямку менших температур виникає потік газу. Таке явище називають тепловий плин газу. Він породжує силу, яка діє вздовж поверхні часточки у тому ж напрямку, що зумовлює її рух у „холодний бік”.
Термопреципітація – осадження часточок аерозолю на холодних поверхнях. Взаємодія часточок з такою поверхнею приводить до зменшення кінетичної енергії часточок аерозолю.
При односторонньому освітленні часточок аерозолю вони можуть рухатися як у напрямку світлового променя, так і назустріч йому. Таке явище називається фотофорезом і є окремим випадком термофорезу. Так, у нижній стратосфері, де тиск повітря високий частинки рухаються вгору до Сонця. У верхній стратосфері тиск падає і часточки починають рухатися у протилежному напрямку – вниз. Отже, часточки рухаються в обмеженому шарі стратосфери. Це приводить до накопичення і утворення стійких шарів аерозолів, які впливають на прозорість стратосфери, а в цілому і на клімат.
В промисловості для руйнування аерозолів з метою очистки газових сумішей широко використовують дію електричного поля, фільтрування через тонковолокнисті фільтри, осадження в циклонах, електрофільтрах тощо.
Колоїдні ПАР. Карбонові ланцюги молекул ПАР в полярному розчиннику – воді об’єднуються в компактне ядро, а гідратовані полярні групи, що повернені в бік водяної фази, утворюють гідрофільну оболонку. Такий асоціат молекул ПАР (з числом молекул 20-100 і більше) є сферичною колоїдною часточкою (міцелою) (рис.6.37).
Міцелярні дисперсні ПАР виявляють властивості, які належать колоїдно-дисперсним системам: світлорозсіювання, електропро-відність, швидкість дифузії, в’язкість та ін.
Здатність до міцелоутворення володіють не усі ПАР, а тільки ті, які мають оптимальні співвідношення між гідрофобною і гідрофільною частинами, що визначається величиною ГЛБ. До міцелоутворюючих ПАР відносяться натрієві, калієві і амонієві солі жирних кислот з довжиною ланцюга С12-20, алкілсульфати, алкилбензолсульфонати та інші синтетичні йоногенні і нейоногенні ПАР.
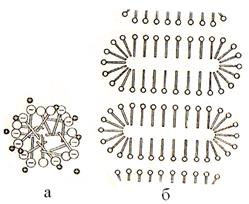
|
| Рис.6.37. Схема будови сферичних (а) і пластинчастих (б) міцел колоїдних пар |
При збільшенні вмісту ПАР в розчині вище деякої критичної концентрації спостерігається помітний зріст світлорозсіювання; ізотерми поверхневого натягу замість звичайного поступового зниження поверхневого натягу мають злом, а при подальшому зростанні концентрації значення поверхневого натягу залишається незмінним (рис.6.38). Аналогічно злом з’являється і на кривих концентраційної залежності питомої і еквівалентної електропровідності розчинів йоногенних ПАР. Концентрація, вище якої починається міцелоутворення, називається критичною концентрацією міцелоутворення (ККМ).

|
| Рис.6.38. Залежність властивостей розчинів колоїдних ПАР від концентрації |
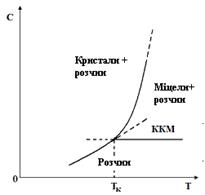
Дослідження водних дисперсій, що утворюють міцели ПАР, показали, що міцелоутворення як шляхом конденсації молекул в міцели, так і шляхом диспергування макрофаги може відбуватися тільки вище деякої температури ТК, яку називають точкою Крафта (рис.6.39). Нижче температури ТК розчинність ПАР мала і є менше ніж ККМ. В цієї області температур існує рівновага між кристалами мила і істинним розчином ПАР, концентрація якого зростає по мірі зростання температури. Тому в розчинах ПАР, для яких точка Крафта лежить в області вище 50 - 800 С, в звичайних умовах міцелоутворення не спостерігається.
|
| Рис. 6.39. Залежність розчинності ПАР від температури |
Для усіх міцелоутворюючих ПАР ККМ лежить в області малих значень концентрацій (10-5 – 10-2 кмоль/м3. Зі зростанням вмісту ПАР в розчині (в десятки і сотні разів, що перевищує ККМ) сферичні міцели перетворюються в анізометричні еліпсоїдальні і циліндричні, а потім в паличкоподібні, стрічкові і пластинчасті міцели (рис.6.37). При цьому кожному значенню концентрації відповідає термодинамічна рівновага
Сферичні L Анізометричні L Стрічкові
міцели міцели міцели
Подібні системи, проміжкові між істинними рідинами і твердими тілами, часто називають рідкими кристалами (рис.6.37). Таким чином система ПАР – вода може при зміні вмісту компонентів переходить в різні стани, від гомогенної системи, через стадію ліофільної колоїдної системи, до макрогетерогенної системи. При цьому різним станам системи відповідає певна термодинамічна рівновага:

 Істинний L Сферичні L Анізометричні L Кристали L Істиний
Істинний L Сферичні L Анізометричні L Кристали L Істиний
розчин міцели в міцели розчин
розчині

 Колоїдна система
Колоїдна система
В неводних розчинах ПАР тобто в розчинах ПАР в карбонгідрогенних середовищах можуть утворюватися міцели з протилежною орієнтацією молекул (рис.6.40). При формуванні таких зворотних міцел полярні групи об’єднуються в гідрофільне (олеофобне) ядро, а карбонгідрогенні радикали, що повернуті в бік рідинного неполярного середовища, утворюють олеофільну оболонку, яка екранує внутрішню гідрофільну частину міцели від контакту з карбонгідрогенним середовищем.

|
| 6.40.Будова зворотної міцели |
Введення в систему ПАР – вода третього компоненту, в залежності від його природи, може або перешкоджати міцелоутворенню або сприяти цьому процесу. Введення, наприклад, низщих спиртів, але в малій кількості, приводить до зниження ККМ, тобто це полегшує міцелоутворення. Це явище – введення в склад міцел третього компоненту, який не розчиняється або слабко розчиняється в дисперсійному середовищі, називається солюбілізацією, або колоїдним розчиненням. Розрізняють пряму солюбілізацію (в водних дисперсіях ПАР) і зворотню (в карбоногідрогенних системах).
Солюбілізація широко застосовується в промисловості при виготовленні синтетичних латексів, для збільшення здобичі нафти, в емульсійній полімеризації, в поліграфічному, харчовому і фармацевтичному виробництвах.
Запитання для самоконтролю
1. Що таке тіксотропія? Наведіть приклади.
2. У чому відмінність вільнодисперсних систем від зв’язанодисперсних?
3. Речовини з яким значенням молекулярної маси прийнято відносити до ВМС? Які типи ВМС вам відомі?
4. Назвіть відомі вам природні ВМС.
5. Чому істинні розчини ВМС відносять до колоїдних систем?
6. Що таке поліелектроліти? Які класифікації поліелектролітів вам відомі?
7. У чому суть явища набухання?
8. У чому полягає різниця між обмеженим та необмеженим набуханням?
9. Що таке набухання?
10. Що являють собою драглі?
11. Що являють собою поверхнево-активні речовини? Як їх класифікують?
12. Що являють собою міцели дифільних пар?
13. Що означає абревіатура ККМ? Поясніть зміст цього поняття?
14. Що таке область Крафта?
15. Що таке солюбілізація?
16. Які міцели колоїдних ПАР називаються зворотними або оберненими?
17. Що таке прямі і зворотні емульсії?
18. Що означає абревіатура ГЛБ? Приведіть пояснення.
19. Назвіть відомі вам області застосування колоїдних ПАР.
20. Що представляють собою піни? Поясніть їх будову.
21. Що таке кратність піни? Поясніть правило Плато.
22. Наведіть приклади застосування пін.
23. Поясність дію піноутворення і піногасників. Наведіть приклади.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 902; Нарушение авторских прав?; Мы поможем в написании вашей работы!