
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема 1.1. Перший закон термодинаміки. Термохімія
|
|
|
|
Розділ 1. ХІМІЧНА ТЕРМОДИНАМІКА
Фізична хімія 1. Хімічна термодинаміка. Фазові
Кредитний модуль
ЗАВДАННЯ ДЛЯ САМОСТІЙНОЇ РОБОТИ
Тема 2.5. Нерівноважні процеси в електрохімічних системах
Тема 2.4. Основні типи гальванічних елементів та їх властивості
Хімічні та концентраційні елементи (ланцюги).
Дифузійний потенціал, механізм його виникнення. Методи врахування та усунення дифузійних потенціалiв. Ланцюги без переносу та з переносом.
Термодинаміка гальванічного елементу. Рівняння Гіббса-Гельмгольца для гальванічного елементу. Визначення напрямку перебігу та термодинамічних параметрiв хімічної реакції, що перебігає у гальванічному елементi. Розрахунок констант рівноваги електрохімічних процесiв.
Методи вимірювання ЕРС гальванічних елементiв та електродних потенціалiв. Нормальний елемент Вестона як еталон електрорушійної сили в компенсаційному методі.
Потенціометрiя. Визначення добутку розчинності важкорозчинних електролітів потенціометричним методом. Визначення середнього іонного коефіцієнта активності електроліту. Потенціометричне визначення pH розчинiв. Потенціометричне титрування.
Електроліз. Закони електролізу Фарадея. Вихід продуктiв електролізу за струмом. Уявні та істинні відхилення від законiв електролізу, їх причини.
Електродна поляризація, її види. Перенапруга водню, застосування цього явища в електролізi. Рівняння Тафеля.
Хімічні джерела струму; вимоги, що до них висуваються. Первинні та вторинні хімічні джерела струму. Акумулятори: кислотні, лужні, літій-іонні. Електрохімічні генератори (паливні елементи). Сучасні джерела енергії - суперконденсатори.
Корозія металів. Механізм електрохімічної корозії. Методи захисту металів від корозії: захисні неметалеві та металеві покриття, катодний та протекторний захист, пасивування металiв. Інгібітори корозії.
рівноваги та розчини»
Запитання і завдання для самоконтролю
1. Що розуміють під системою? Які системи називають гомогенними, гетерогенними, відкритими, закритими, ізольованими?
2. Що таке параметри стану системи? Як виглядає рівняння зв’язку між ними для ідеального газу? Які умови називають нормальними, стандартними?
3. Назвіть ізопроцеси та покажіть на графіку в координатах 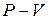 , як змінюються параметри ідеального газу в цих процесах.
, як змінюються параметри ідеального газу в цих процесах.
4. Які характеристики системи є функціями стану? Чому дорівнює їх зміна в циклічному процесі? Наведіть приклади функцій стану.
5. Які процеси називають оборотними та необоротними? Рівноважними та нерівноважними?
6. Що розуміють під внутрішньою енергією системи? Від чого вона залежить?
7. Що таке теплота і робота? Чи є вони функціями стану?
8. Наведіть відомі Вам формулювання та запишіть математичний вираз першого закону термодинаміки для елементарного та скінченого процесів.
9. Яку роботу виконує ідеальний газ в різних ізопроцесах? В якому з них вона є найбільшою?
10. Як змінюється внутрішня енергія в різних процесах за участю ідеального газу?
11. Що таке ентальпія? Від чого вона залежить? Чи змінюється ентальпія в процесі ізотермічного розширення ідеального газу?
12. Чим визначаються і як пов’язані між собою теплові ефекти ізобарного та ізохорного процесів? Проаналізуйте рівняння зв’язку між ними.
13. Що називають тепловим ефектом хімічної реакції? Які реакції є ендотермічними, екзотермічними? Як пов’язані 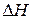 i
i 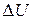 реакцій? Наведіть приклади.
реакцій? Наведіть приклади.
14. Як формулюється та для чого використовують закон Гесса? Поясніть на прикладах.
15. Що таке стандартний стан речовини? Що називають стандартною теплотою утворення хімічної сполуки? Як її позначають? Наведіть
приклади реакцій, що відповідають цьому поняттю.
16. Як розраховують стандартні теплові ефекти хімічного процесу в ізобарних та ізохорних умовах за допомогою стандартних теплот утворення?
17. Що називають теплотою згоряння речовини? Наведіть приклади відповідних реакцій. Як розрахувати тепловий ефект хімічного процесу за теплотами згоряння її учасників?
18. Чи будуть відрізнятися між собою теплові ефекти реакції, яка перебігає в одному випадку термодинамічно необоротно, а в другому – оборотно, якщо початковий та кінцевий стан системи в обох процесах однакові?
19. Як розраховують теплові ефекти реакцій, що перебігають у розчинах?
20. Що називають інтегральною теплотою розчинення кристалічної речовини? Від чого вона залежить? Чим обумовлений знак теплоти розчинення?
21. Що таке теплота нейтралізації? Які фактори на неї впливають? Як пов’язані між собою теплоти нейтралізації сильних та слабких кислот?
22. Що розуміють під теплотою гідратоутворення? Як її визначають?
Типові задачі
1. Розрахунок ізобарного та ізохорного теплових ефектів реакції за стандартних умов.
2. Визначення кількості теплоти, яка виділяється або поглинається внаслідок реакції за участю певної кількості речовини.
3. Написання реакцій, які відповідають поняттям «теплота утворення» та «теплота згоряння» для конкретних хімічних сполук.
Література: [ 1, § 55-57, 62, 63; 2, § ІІ.1-ІІ.5; 3, Гл. 2, § 1-4, Гл. 3, § 1-2; 4, 1.1-1.3, 2.1, 2.5].
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 1104; Нарушение авторских прав?; Мы поможем в написании вашей работы!