
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Дослід 1. Кількісне визначення гідроксипроліну (оксипроліну) в сечі
|
|
|
|
Практична робота
Теоретичні питання
Тема № 10. Дослідження біохімічних складників сполучної тканини.
Мета заняття: Знати склад і біохімічні особливості метаболізму сполучної тканини, її функціонування в нормі і при патології. Уміти кількісно визначати гідроксипролін (оксипролін) у сечі для діагностики деяких захворювань.
Актуальність теми: Однією з важливих проблем сучасної медицини є вивчення порушення метаболізму в сполучній тканині при набутих та спадкових захворюваннях, для чого необхідно знати деякі біохімічні тести з метою своєчасної діагностики та правильного лікування.
Конкретні завдання:
Ø Давати морфологічну та біохімічну характеристику компонентам сполучної тканини (фібрилярні структури, основна міжклітинна речовина).
Ø Пояснювати біохімічні зміни в сполучній тканині при старінні та деяких патологічних станах (мукополісахаридозах, колагенозах).
Ø Оволодіти методом кількісного визначення гідроксипроліну та якісною реакцією виявлення глікозамінгліканів (мукополісахаридів) у сечі, давати оцінку отриманим результатам.
1. Загальна характеристика морфології та біохімічного складу сполучної тканини. Біохімічна будова міжклітинної речовини пухкої волокнистої сполучної тканини: волокна (колагенові, ретикулярні, еластичні); основна аморфна речовина.
2. Білки волокон сполучної тканини: колагени, еластин, глікопротеїни та протеоглікани. Біосинтез колагену та утворення фібрилярних структур.
3. Складні вуглеводи основного аморфного матриксу сполучної тканини – глікозаміноглікани (мукополісахариди). Механізми участі молекул глікозаміногліканів (гіалуронової кислоти, хондроїтин-, дерматан-, кератансульфатів) у побудові основної речовини пухкої волокнистої сполучної тканини. Розподіл різних глікозаміногліканів в органах і тканинах людини.
4. Патобіохімія сполучної тканини. Біохімічні механізми виникнення мукополісахаридозів та колагенозів, їх клініко-біохімічна діагностика.
5. Ревматизм, його клініко – біохімічна діагностика.
Принцип методу. Метод базується на окисненні гідроксипроліну до сполуки, близької за будовою до піролу, яка при конденсації з реактивом Ерліха (п-диметиламінобензальдегід) дає рожеве забарвлення. Інтенсивність забарвлення розчину пропорційна концентрації гідроксипроліну.
Матеріальне забезпечення: реактив Ерліха, 3 н розчин сульфатної кислоти, 6% розчин водню пероксиду, 2,5 н розчин натрію гідроксиду, 0,01 М розчин міді сульфату, водяна баня, ФЕК, мірні піпетки, пробірки, лійка, фільтрувальний папір.
Хід роботи: У першу пробірку відмірюють 1мл профільтрованої сечі, в другу – 1мл дистильованої води (контрольна проба). В обидві пробірки додають по 1мл 0,01 М розчину міді сульфату, по 1 мл 2,5 н розчину натрію гідроксиду, по 1мл 6% розчину водню пероксиду. Проби перемішують 5 хв, після чого нагрівають 3 хв у киплячій водяній бані, а потім пробірки охолоджують водою з крану. У пробірки додають по 4мл 3 н розчину сірчаної кислоти і по 1мл реактиву Ерліха, ставлять на 1 хв у киплячу водяну баню, охолоджують, а потім вимірюють оптичну густину на ФЕКу проти контролю при довжині хвилі 500 – 560 нм (зелений світлофільтр) у кюветі завтовшки 10 мм.
За калібрувальним графіком визначають вміст гідроксипроліну в дослідній пробі і розраховують кількість гідроксипроліну, виділеного з сечею впродовж доби за формулою:
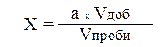 ,
,
де а – кількість гідроксипроліну, знайдена за калібрувальним графіком; V доб. – добовий об’єм сечі мл; V проби – об’єм сечі, взятий для аналізу, мл.
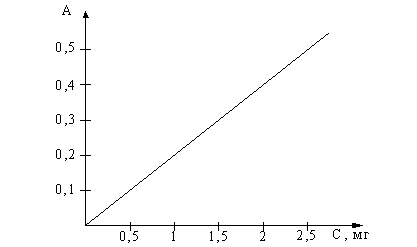
Крива залежності оптичної густини розчину гідроксипроліну від його концентрації
Пояснити отриманий результат. Зробити висновок
Клініко-діагностичне значення. Гідроксипролін – це амінокислота, яка характерна для білків сполучної тканини – колагену (містить 12-14 %) і еластину (1-2 %). Саме вміст гідроксипроліну в сечі та крові характеризує інтенсивність катаболізму колагену та швидкість обміну цієї амінокислоти. Гідроксипролін може знаходитись у стані, зв’язаному з білками, пептидами, а також у вільному стані як у сироватці крові, так і в сечі. У віці людини 10 – 20 років з сечею виділяється до 200 мг гідроксипроліну за добу, а у дорослих – 15-50 мг. Зростання цього показника спостерігають при колагенозах (ревматизм, ревматоїдний артрит, системна склеродермія, дерматоміозит), при гіперпаратиреоїдизмі, хворобі Педжета (до 1 г за добу). Ще більше виділяється гідроксипроліну при спадковій гіпергідроксипролінемії, що спричинено дефектом ферменту гідроксипролін-оксидази, в результаті чого порушується обмін гідроксипроліну.
Дослід 2. Якісна реакція на глікозаміноглікани (проба Беррі-Спінанджера).
Принцип методу. При взаємодії глікозаміногліканів з толуїдиновим синім у кислому середовищі утворюється червоне забарвлення (метахромазія).
Матеріальне забезпечення: толуїдиновий синій (0,04 %-ий розчин в ацетоацетатному буфері з рН 2,0), 10 %-ий розчин ацетатної кислоти, фільтрувальний папір, мікропіпетки.
Хід роботи: На смужку фільтрувального паперу на віддалі 1 см один від одного наносять мікропіпеткою 0,005, 0,01 і 0,025 мл сечі, висушують папір при кімнатній температурі, а потім занурюють його в 0,04 %-ий розчин толуїдинового синього на 1 хв. Виймають смужку паперу і відмивають реактив 10 % розчином ацетатної кислоти. Якщо концентрація глікозаміногліканів в досліджуваній сечі перевищує 10 мг/100 мл, тоді з’являється червоне забарвлення на одній із нанесених плям.
Зробити висновок.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 2333; Нарушение авторских прав?; Мы поможем в написании вашей работы!