
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Приклади розв’язків задач
|
|
|
|
Приклад 1. Визначте масу трьох моль кальцій гідроксиду Са(OН)2.
| Д а н о: ν (Са(OН)2) = 3 моль | Р о з в’ я з о к: Використовуючи формулу для визначення кількості речовини |
| В и з н а ч и т и: m (Са(OН)2) –? | |
 визначаємо масу кальцій гідроксиду: m = ν·M
Молярна маса кальцій гідроксиду дорівнює:
M(Са(OН)2) = 40 + 2 (16 + 1) = 74 г/моль, тоді
m = 3 моль·74 г/моль = 222 г.
визначаємо масу кальцій гідроксиду: m = ν·M
Молярна маса кальцій гідроксиду дорівнює:
M(Са(OН)2) = 40 + 2 (16 + 1) = 74 г/моль, тоді
m = 3 моль·74 г/моль = 222 г.
| |
| В і д п о в і д ь: m (Са(OН)2) = 222 г. |
Приклад 2. Скільки моль міститься в 29,25 кг NaCl?
| Д а н о: m (NaCl) = 29,25 кг | Р о з в’ я з о к:
Кількість речовини визначаємо за формулою:
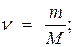
|
| В и з н а ч и т и: ν (NaCl) –? | |
Молярна маса NaCl дорівнює:
М(NaCl) = 23 + 35,5 = 58,5 г/моль.
Тоді кількість моль NaCl:
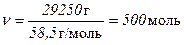
| |
| В і д п о в і д ь: ν (NaCl) = 500 моль. |
Приклад 3. Розрахуйте масу одного атома магнію в грамах.
| Д а н о: N (Mg ) = 1 | Р о з в’ я з о к:
Молярна маса магнію:
М (Mg) = 24 г/моль.
Використовуючи формули
 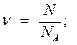
|
| В и з н а ч и т и: m0 (Mg) –? | |
запишемо: 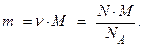 Оскільки N = 1, то маса1 атома визначається за формулою
Оскільки N = 1, то маса1 атома визначається за формулою
 Звідси
Звідси 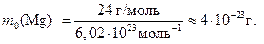
| |
| В і д п о в і д ь: m0 (Mg) ≈ 4·10–23 г. | |
Приклад 4. Визначте еквівалентні маси сульфатної кислоти H2SO4, алюміній гідроксиду Al(OH)3 і алюміній сульфату Al2(SO4)3.
| Д а н о: H2SO4 Al(OH)3 Al2(SO4)3 | Р о з в’ я з о к:
Еквівалентна маса сульфатної кислоти: 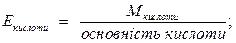 Молярна маса її дорівнює
М (H2SO4) = 2·1 + 32 + 4·16 = 98 г/моль.
Тоді:
Молярна маса її дорівнює
М (H2SO4) = 2·1 + 32 + 4·16 = 98 г/моль.
Тоді:
|
| В и з н а ч и т и: Е (H2SO4)–? Е (Al(OH)3)–? Е (Al2(SO4)3) –? | |
E (H2SO4) = 98/2 = 49 г/моль-екв.
Еквівалентна маса алюміній гідроксиду:
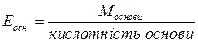 .
Молярна маса Al(OH)3 дорівнює:
М (Al(OH)3) = 27 + 3(16 + 1) =78 г/моль.
Тоді:
E (Al(OH)3) = 78/3 = 26 г/моль-екв.
Для обчислення еквівалентної маси алюміній сульфату використовуємо формулу: .
Молярна маса Al(OH)3 дорівнює:
М (Al(OH)3) = 27 + 3(16 + 1) =78 г/моль.
Тоді:
E (Al(OH)3) = 78/3 = 26 г/моль-екв.
Для обчислення еквівалентної маси алюміній сульфату використовуємо формулу:
 Молярна маса Al2(SO4)3 дорівнює:
М (Al2(SO4)3) = 2·27 + 3(32 + 4·16) = 342 г/моль.
Тоді:
Е (Al2(SO4)3) = 342/2·3 = 57 г/моль-екв.
Молярна маса Al2(SO4)3 дорівнює:
М (Al2(SO4)3) = 2·27 + 3(32 + 4·16) = 342 г/моль.
Тоді:
Е (Al2(SO4)3) = 342/2·3 = 57 г/моль-екв.
| |
| В і д п о в і д ь: E (H2SO4) = 49 г/моль-екв, E (Al(OH)3) = 26 г/моль-екв, Е (Al2(SO4)3) = 57 г/моль-екв. |
Приклад 5. Скільки моль міститься в 0,56 м3 хлору за н.у.?
| Д а н о: V (Cl2) = 0,56 м3 н.у. | Р о з в’ я з о к:
Кількість речовини визначаємо за формулою 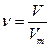 . .
|
| В и з н а ч и т и: ν (Cl2)–? | |
Так як мольний об’єм газу звичайно виражають в дм3/моль, то об’єм переводять в дм3.
0,56 м3 = 560 дм3
Тоді 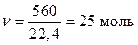 . .
| |
| В і д п о в і д ь: ν (Cl2)= 25 моль. |
Приклад 6. Скільки молекул міститься в 56 м3 кисню за н.у.?
| Д а н о: V (О2) = 56 м3 н.у. | Р о з в’ я з о к:
Для визначення кількості молекул скористаємося формулами:
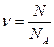 ; ; 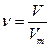
|
| В и з н а ч и т и: N (О2)–? | |
Звідси:  Так як мольний об’єм газу звичайно виражають в дм3/моль, то об’єм переводять в дм3.
56 м3 = 56 000 дм3
Тоді
Так як мольний об’єм газу звичайно виражають в дм3/моль, то об’єм переводять в дм3.
56 м3 = 56 000 дм3
Тоді 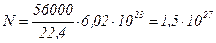
| |
| В і д п о в і д ь: N (О2)= 1,5·1027 молекул. |
Приклад 7. 800 мл деякого газу мають масу 1200 г, а один літр повітря за таких умов має масу 1,36 г. Визначити мольну масу газу.
| Д а н о: V1 = 800 мл = 0,8 л m1 = 1200 мг = 1,2 г Vпов = 1 л mпов = 1,36 г | Р о з в’ я з о к:
При розв’язуванні задачі скористаємося
формулами:
 i i 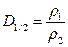 де ρ2 = ρпов; M2 = Мпов = 29 г/моль
Отже, M1 = D1/2·Мпов
де ρ2 = ρпов; M2 = Мпов = 29 г/моль
Отже, M1 = D1/2·Мпов
|
| В и з н а ч и т и: M1 –? | |
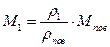 ; ;
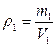 i i 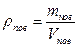 Тоді
Тоді 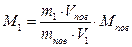 ; ;
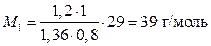
| |
| В і д п о в і д ь: M1 = 39 г/моль. |
Приклад 8. Розрахувати масові частки кожного із елементів у натрій сульфаті.
| Д а н о: Na2SO4 | Р о з в’ я з о к:
Масова частка елементів розраховується за формулою:
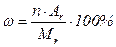
|
| В и з н а ч и т и: ω ( Na ) –? ω ( S ) –? ω ( O ) –? | |
Молекулярна маса натрій сульфату становить:
Мr (Na2SO4 ) = 2·23 + 32 + 4·16 = 142.
Тоді
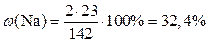
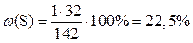
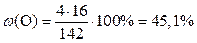
| |
| В і д п о в і д ь: ω (Na)= 32,4 %; ω (S)= 22,5 %; ω (O)= 45,1 %. |
Приклад 9. Визначте молярну масу газу, якщо 0,2 кг його за температури 67 о С і тиску 4 атм. займають об’єм 30,32 л.
| Д а н о: V = 30,32 л = 30,32·10–3 м3 m = 0,2 кг = 0,2·103 г Т = 67 о С + 273 = 340 К р = 4 атм.·101325 = 405300 Па | Р о з в’ я з о к:
При розв’язуванні задачі скористаємося формулою:
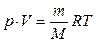 Звідси
Звідси 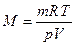
|
| В и з н а ч и т и: M –? | |
Тоді 
| |
| В і д п о в і д ь: M = 46 г/моль. |
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 562; Нарушение авторских прав?; Мы поможем в написании вашей работы!