
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Номенклатура основ
|
|
|
|
Основи - це складні сполуки, які складаються з атомів металу та гідроксогруп. Кількість гідроксогруп вказує на кислотність основи та визначається ступенем окиснення металу.
Основи
Хімічні властивості амфотерних оксидів
Амфотерними називають оксиди, які залежно від умов проявляють властивості кислотних або основних оксидів.
1 Взаємодія з кислотами або кислотними оксидами з утворенням солей:
ZnO + H2SO4 = ZnSO4 + H2O.
Al2O3 + 3N2O5 = 2Al(NO3)3
(N2O5 + H2O → 2H NO3).
2 Взаємодія з основами або основними оксидами з утворенням солей:
BeO + 2NaOH = Na2BeO2 + H2O,
(BeO + H2O → H2 BeO2).
PbO + MgO = MgPbO2,
(PbO + H2O → H2 PbO2)
3 Взаємодія між собою з утворенням солі (звичайно елемент з нижчим ступенем окиснення записують як катіон солі, а метал з вищим ступенем окиснення – у складі аніону):
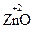 +
+  = Zn (AlO2)2
= Zn (AlO2)2
(Al2O3 + H2O → 2H AlO2).
З точки зору теорії електролітичної дисоціації основами називають електроліти, при дисоціації яких утворюються у вигляді аніонів лише гідроксид-йони.
Основи класифікують:
- за розчинністю на розчинні (луги) та нерозчинні;
- за кількістю гідроксогруп на однокислотні, двокислотні та багатокислотні.
Назви основ утворюються таким чином:

Кількість гідроксогруп співпадає з валентністю (ступенем окиснення) металу.
NaOH – натрій гідроксид,
Mn(ОН)2 – манган (II) гідроксид,
Mn(ОН)3 – манган (III) гідроксид.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1074; Нарушение авторских прав?; Мы поможем в написании вашей работы!