
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Модуль. 2. Кількісний аналіз 11 страница
|
|
|
|
722. Якщо після припинення титрування слабкої основи розчином сильної кислоти в розчині ще міститься ця основа, то похибка буде мати знак.... і буде розраховуватися за формулою:
A. „-”; 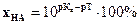
B. „-”; 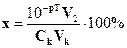
C. „+”; 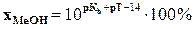
D. „+”; 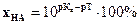
E. *„-”; 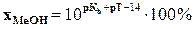
723. Якщо після припинення титрування сильної основи розчином сильної кислоти в розчині ще міститься ця основа, то похибка буде мати знак.... і буде розраховуватися за формулою:
A. „+”; 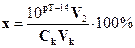
B. „+”; 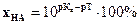
C. „-”; 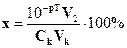
D. „+”; 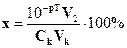
E. *„-”; 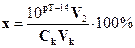
724. Якщо після припинення титрування сильної кислоти розчином сильної основи в розчині ще міститься ця кислота, то похибка буде мати знак.... і буде розраховуватися за формулою:
A. „+”; 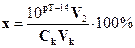
B. „+”; 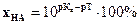
C. * „-”; 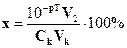
D. „+”; 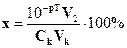
E. „-”; 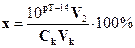
725. Якщо після припинення титрування сильної кислоти розчином сильної основи в розчині міститься надлишок цієї основи, то похибка буде мати знак.... і буде розраховуватися за формулою:
A. * „+”; 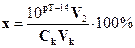
B. „+”; 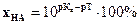
C. „-”; 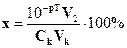
D. „+”; 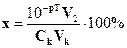
E. „-”; 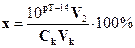
726. Якщо після припинення титрування сильної основи розчином сильної кислоти в розчині міститься надлишок цієї кислоти, то похибка буде мати знак.... і буде розраховуватися за формулою:
A. „+”; 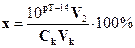
B. „+”; 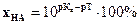
C. „-”; 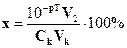
D. *„+”; 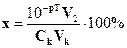
E. „-”; 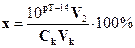
727. В результаті неспівпадання кінцевої точки титрування і точки еквівалентності виникають індикаторні похибки. Якої індикаторної похибки не існує?
A. Кислотної
B. Основної
C. Гідроксонієвої
D. Гідроксильної
E. *Інструментальної
728. Від якого фактору не залежить величина стрибка титрування в методі нейтралізації?
A. Концентрації визначуваної речовини
B. *Розчинності осаду, який утворюється в процесі титрування
C. Концентрації титранту
D. Константи кислотності визначуваної кислоти
E. Температури
729. Від чого залежить величина стрибка титрування в методі нейтралізації?
A. Величини константи стійкості
B. *Концентрації визначуваної речовини
C. Величини добутку розчинності
D. Тиску
E. Кількості доданого метилового червоного
730. Від чого залежить величина стрибка титрування в методі нейтралізації?
A. Константи основності індикатора
B. Кількості доданого метилоранжу
C. Величини добутку розчинності
D. *Концентрації титранту
E. Тиску
731. Величина рТ для індикатора методу нейтралізації означає:
A. *Показник титрування
B. Кислотність середовища
C. Показник титранту
D. Показник речовини, яку відтитровують
E. Такого позначення в аналітичній хімії не існує
732. Виберіть двоколірний рН-індикатор.
A. Йод-крохмальний папірець
B. Фенолфталеїн
C. *Метиловий червоний
D. Еозин
E. Фенілантранілова кислота
733. Від чого залежить величина стрибка титрування в методі нейтралізації?
A. ЕРС
B. *Константи основності визначуваної основи
C. Кількості індикатора
D. Величини константи стійкості
E. Тиску
734. Від чого залежить величина стрибка титрування в методі нейтралізації?
A. Константи кислотності індикатора
B. Вологості і природи розчинника
C. *Константи кислотності визначуваної кислоти і природи розчинника
D. ЕРС, температури, природи розчинника
E. Кількості доданого фенолфталеїну
735. Інтервал переходу забарвлення для індикаторів в протолітометрії розраховують за формулою:
A. 
B. рН = рТ
C. 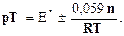
D. * 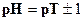
E. 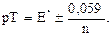
736. Які теорії індикаторів в методі нейтралізації існують?
A. Теорія Бутлерова
B. *Іонна й іонно-хромоформна
C. Таких теорій не існує
D. Тільки іонна
E. Тільки хромоформна
737. Виберіть двоколірний рН-індикатор.
A. Фенолфталеїн
B. Дифеніламін
C. Ферум (ІІІ) тіоціанат
D. *Метилоранж
E. Еріохром чорний Т
738. Виберіть двоколірний рН-індикатор.
A. Мурексид
B. *Лакмус
C. Дифенілкарбазон
D. Калій хромат
E. Фенолфталеїн
739. Виберіть одноколірний рН-індикатор.
A. Лакмус
B. Метилоранж
C. Фероїн
D. Метиловий червоний
E. *Фенолфталеїн
740. Всі нижче перераховані вимоги є вимогами до рН-індикаторів, окрім:
A. Зміна забарвлення індикатора повинна відбуватися різко в невеликому інтервалі значень рН
B. Зміна забарвлення індикатора повинна бути оборотньою
C. *Зміна забарвлення індикатора повинна бути необоротньою
D. Забарвлення індикатора повинно бути якомога більш інтенсивне
E. Забарвлення індикатора при близьких значеннях рН повинно добре відрізнятися
741. Для якого типу кислотно-основної взаємодії в протолітометрії неможливо підібрати індикатор?
A. Між амоній гідроксидом і хлоридною кислотою
B. *Між ацетатною кислотою і амоній гідроксидом
C. Між натрій гідроксидом і хлоридною кислотою
D. Між калій гідроксидом і сульфатною кислотою
E. Між натрій гідроксидом і ацетатною кислотою
742. Який тип кислотно-основної взаємодії не використовується в протолітометрії?
A. *Між ацетатною кислотою і амоній гідроксидом
B. Між натрій гідроксидом і хлоридною кислотою
C. Між калій гідроксидом і сульфатною кислотою
D. Між амоній гідроксидом і хлоридною кислотою
E. Між натрій гідроксидом і ацетатною кислотою
743. Який титрант не використовують в протолітометрії?
A. Сульфатну кислоту
B. Хлоридну кислоту
C. Натрій гідроксид
D. *Амоній гідроксид
E. Калій гідроксид
744. Який титрант не використовують в протолітометрії?
A. Калій гідроксид
B. Хлоридну кислоту
C. Сульфатну кислоту
D. Натрій гідроксид
E. *Ацетатну кислоту
745. Виберіть індикатор методу ацидиметрії.
A. Суспензія арґентум йодиду
B. Еріохром чорний Т
C. Тропеолін 00
D. *Метиловий червоний
E. Мурексид
746. Виберіть індикатор методу ацидиметрії.
A. Ферум (ІІІ) тіоціанат
B. Мурексид
C. *Метилоранж
D. Кальконкарбонова кислота
E. Еозин
747. Виберіть індикатор методу алкаліметрії.
A. Еріохром чорний Т
B. *Фенолфталеїн
C. Флюоресцеїн
D. Калій хромат
E. Фероїн
748. Індикатори в методі нейтралізації згідно іонної теорії індикаторів - це органічні.... іонізовані і неіонізована форми яких мають різне забарвлення.
A. *Слабкі кислоти або основи
B. Сильні основи або слабкі кислоти
C. Сильні кислоти або слабкі основи
D. Відновники або окисники
E. Сильні кислоти або основи
749. Індикатори в методі протолітометрії згідно іонної теорії індикаторів - це органічні.... іонізовані і неіонізована форми яких мають різне забарвлення.
A. Може бути будь-яка речовина
B. Сильні кислоти
C. *Слабкі основи
D. Окисники
E. Відновники
750. Індикатори в методі протолітометрії згідно іонної теорії індикаторів - це органічні...., іонізовані і неіонізована форми яких мають різне забарвлення.
A. Окисники
B. *Слабкі кислоти
C. Сильні кислоти
D. Відновники
E. Сильні основи
751. Іонна теорія індикаторів була запропонована:
A. Арреніусом
B. Фарадеєм
C. Гессом
D. *Оствальдом
E. Менделєєвим
752. В конічну колбу місткістю 100 мл вносять піпеткою 15,00 мл 0,5 моль/л розчину натрій гідроксиду, додають 5.00 мл досліджуваного розчину ацетатної кислоти, 3-4 краплі фенолфталеїну і відтитровують залишок натрій гідроксиду 0,1 моль/л розчином хлоридної кислоти до зникнення рожевого забарвлення розчину. За якою формулою необхідно провести розрахунки маси ацетатної кислоти в 1 мл досліджуваного розчину?
A. 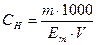
B. 
C. 
D. 
E. * 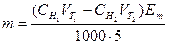
753. Близько 0,5 г (точна наважка) нашатирного спирту помістили у зважену колбу місткістю 150 мл, куди попередньо помістили 50 мл 0,05 моль/л розчину сульфатної кислоти, зважили. Розчин відтитрували 0,1 моль/л розчином натрій гідроксиду з індикатором метиловим червоним. За якою формулою необхідно провести розрахунки маси амоніаку в 1 г нашатирного спирту?
A. * 
B. 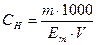
C. 
D. 
E. 
754. При титруванні оксалатної кислоти розчином натрій гідроксиду в присутності фенолфталеїну титрування припиняють при зміні забарвлення:
A. Від червоного до синього
B. Від синього до червоного
C. *Від безбарвного до рожевого
D. Від рожевого до безбарвного
E. Від жовтого до червоного
755. При титруванні оксалатної кислоти розчином калій гідроксиду в присутності фенолфталеїну титрування припиняють при зміні забарвлення:
A. *Від безбарвного до рожевого
B. Від червоного до жовтого
C. Від червоного до синього
D. Від синього до червоного
E. Від рожевого до безбарвного
756. При титруванні розчину натрій карбонату розчином хлоридної кислоти в присутності метилового червоного припиняють при зміні забарвлення:
A. *Від жовтого до рожево-оранжевого
B. Від рожевого до безбарвного
C. Від червоного до синього
D. Від безбарвного до рожевого
E. Від рожево-оранжевого до жовтого
757. При титруванні оксалатної кислоти розчином калій гідроксиду в присутності фенолфталеїну титрування припиняють при зміні забарвлення:
A. Від червоного до синього
B. Від синього до червоного
C. *Від безбарвного до рожевого
D. Від рожевого до безбарвного
E. Від жовтого до червоного
758. Які індикатори використовуються в методі нейтралізації?
A. Індуктори
B. Металохромні індикатори
C. Зовнішні індикатори
D. Редокс-індикатори
E. *рН -індикатори
759. Який з індикаторів не належить до рН-індикаторів
A. Лакмус
B. Фенолфталеїн
C. Метиловий червоний
D. *Фероїн
E. Метилоранж
760. В методі протолітометрії індикатори змінюють забарвлення при:
A. Розчиненні осаду
B. *Зміні рН розчину
C. Утворенні осаду
D. Зміні забарвлення розчину
E. Зміні потенціалу в розчині
761. При титруванні розчину натрій тетраборату розчином хлоридної кислоти в присутності метилового червоного припиняють при зміні забарвлення:
A. Від рожевого до безбарвного
B. Від безбарвного до рожевого
C. Від червоного до синього
D. *Від жовтого до червоно-оранжевого
E. Від червоно-оранжевого до жовтого
762. При титруванні оксалатної кислоти розчином натрій гідроксиду в присутності фенолфталеїну титрування припиняють при зміні забарвлення:
A. *Від безбарвного до рожевого
B. Від червоного до жовтого
C. Від червоного до синього
D. Від синього до червоного
E. Від рожевого до безбарвного
763. Стандартизацію розчину натрій гідроксиду методом піпетування проводять по бурштиновій кислоті. Її еквівалентна маса дорівнює:
A. М.м./1
B. М.м./4
C. *М.м./2
D. М.м./3
E. М.м.·2
764. Стандартизацію розчину калій гідроксиду методом піпетування проводять по оксалатній кислоті. Її еквівалентна маса дорівнює:
A. *М.м./2
B. М.м./3
C. М.м./4
D. М.м./1
E. М.м.·2
765. Яке рівняння відповідає стандартизації розчину калій гідроксиду, відповідно до застосування методу піпетування за первинним стандартним розчином?
A. H2CO3 + 2KOH = K2CO3 + 2H2O
B. H2SO4 + 2KOH = K2SO4 + 2H2O
C. H2SO3 + 2KOH = K2SO3 + 2H2O
D. *H2C4H4O4 + 2KOH = K2C4H4O4 + 2H2O
E. HCl + KOH = KCl + H2O
766. Стандартизацію розчину хлоридної кислоти методом піпетування проводять по натрій тетраборату. Його еквівалентна маса дорівнює:
A. *М.м./2
B. М.м./3
C. М.м./4
D. М.м./1
E. М.м.·2
767. Еквівалентна маса хлоридної кислоти, як титранту методу протолітометрії дорівнює:
A. М.м.·3
B. *М.м./1
C. М.м./3
D. М.м.·2
E. М.м./2
768. Яке рівняння відповідає стандартизації хлоридної кислоти методом піпетування?
A. КOН + HCl = КCl + H2O
B. NaOН + HCl = NaCl + H2O
C. Na2CO3 + 2HCl = 2NaCl + CO2 + H2O
D. *Na2B4O7 + 2HCl + 5H2O = 2NaCl + 4H3BO3
E. NaНCO3 + HCl = NaCl + CO2 + H2O
769. Виберіть титранти методу алкаліметрії:
A. *NaOH, KOH
B. Na4B2O7, HCl
C. НСl, H2SO4
D. NaOH, H2C2O4
E. HCl, H2C2O4
770. Виберіть титранти методу ацидиметрії:
A. NaOH, KOH
B. Na4B2O7, HCl
C. *НСl, H2SO4
D. NaOH, H2C2O4
E. HCl, H2C2O4
771. Яке рівняння відповідає стандартизації розчину калій гідроксиду, відповідно до застосування методу піпетування за первинним стандартним розчином?
A. *H2C2O4 + 2KOH = K2C2O4 + 2H2O
B. H2SO3 + 2KOH = K2SO3 + 2H2O
C. H2SO4 + 2KOH = K2SO4 + 2H2O
D. HCl + KOH = KCl + H2O
E. H2CO3 + 2KOH = K2CO3 + 2H2O
772. Яке рівняння відповідає стандартизації розчину натрій гідроксиду, відповідно до застосування методу піпетування за первинним стандартним розчином?
A. H2CO3 + 2NaOH = Na2CO3 + 2H2O
B. H2SO4 + 2NaOH = Na2SO4 + 2H2O
C. H2SO3 + 2NaOH = Na2SO3 + 2H2O
D. *H2C4H4O4 + 2NaOH = Na2C4H4O4 + 2H2O
E. HCl + NaOH = NaCl + H2O
773. Яке рівняння відповідає стандартизації розчину натрій гідроксиду, відповідно до застосування методу піпетування за первинним стандартним розчином?
A. *H2C2O4 + 2NaOH = Na2C2O4 + 2H2O
B. H2SO3 + 2NaOH = Na2SO3 + 2H2O
C. H2SO4 + 2NaOH = Na2SO4 + 2H2O
D. HCl + NaOH = NaCl + H2O
E. H2CO3 + 2NaOH = Na2CO3 + 2H2O
774. Провели стандартизацію розчину калій гідроксиду по бурштиновій кислоті (метод піпетування). За якою формулою необхідно розрахувати концентрацію титранту?
A. 
B. * 
C. 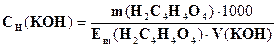
D. 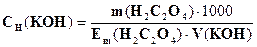
E. 
775. Провели стандартизацію розчину натрій гідроксиду по оксалатній кислоті (метод піпетування). За якою формулою необхідно розрахувати концентрацію титранту?
A. 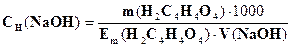
B. 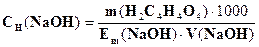
C. * 
D. 
E. 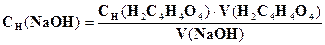
776. Провели стандартизацію розчину хлоридної кислоти по натрій тетраборату (метод піпетування). За якою формулою необхідно розрахувати концентрацію титранту?
A. 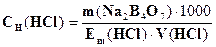
B. 
C. 
D. 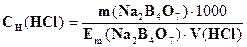
E. * 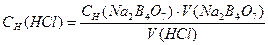
777. Провели стандартизацію розчину хлоридної кислоти по натрій карбонату (метод окремих наважок). За якою формулою необхідно розрахувати концентрацію титранту?
A. 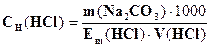
B. 
C. 
D. * 
E. 
778. Стандартизацію розчину хлоридної кислоти методом окремих наважок проводять по натрій карбонату. Його еквівалентна маса дорівнює:
A. М.м.·3
B. М.м./1
C. М.м./3
D. М.м.·2
E. *М.м./2
779. Яке рівняння відповідає стандартизації хлоридної кислоти методом окремих наважок?
A. КOН + HCl = КCl + H2O
B. NaOН + HCl = NaCl + H2O
C. *Na2CO3 + 2HCl = 2NaCl + CO2 + H2O
D. Na2B4O7 + 2HCl + 5H2O = 2NaCl + 4H3BO3
E. NaНCO3 + HCl = NaCl + CO2 + H2O
780. Для стандартизації розчину калій гідроксиду в протолітометрії використовують....
A. *Метод піпетування (по бурштиновій кислоті)
B. Метод окремих наважок (по сульфатній кислоті)
C. Метод окремих наважок (по оксалатній кислоті)
D. Метод піпетування (по хлоридній кислоті)
E. Метод піпетування (по розчину натрій карбонату)
781. Виберіть стандартні речовини, які використовуються для стандартизації лугів в алкаліметрії:
A. Na2B4O7×5H2O, HCl
B. HNO3, H2CO3
C. H2C2O4×2H2O, H2CO3
D. H2C4H4O4, H3BO3
E. *H2C2O4×2H2O, H2C4H4O4
782. Виберіть стандартні речовини, які використовуються для стандартизації кислот в ацидиметрії:
A. H2C2O4×2H2O, H2CO3
B. H2CO3, Na2B4O7×5H2O
C. Na2CO3, КОН
D. *Na2B4O7×5H2O, Na2CO3
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 929; Нарушение авторских прав?; Мы поможем в написании вашей работы!