
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Модуль. 2. Кількісний аналіз 14 страница
|
|
|
|
A. *Малинове
B. Оранжево-рожевий
C. Жовтий
D. Червоне
E. Безколірний розчин
926. Для підвищення сили кислоти необхідно застосовувати:
A. Малополярні розчинники
B. *Розчинники з основними (протоно-акцепторними) властивостями
C. Нівелюючі розчинники
D. Кислотні розчинники (з протонодонорними властивостями)
E. Диференціюючі розчинники
927. У методах титриметричного аналізу використовують індикатори. Які індикатори використовують в методі нейтралізації?
A. редоксіндикатори
B. *кислотно-основні індикатори
C. зовнішні індикатори
D. окисно-відновні індикатори
E. метал-індикатори
928. У титриметричному аналізі використовують метод нейтралізації. Які робочі розчини (титранти) використовують у цьому методі?
A. *NaOH, HCl
B. KI, K2Cr2O7
C. AgNO3, BaCl2
D. КІ, KMnO4
E. NaNO2, Na2S2O3
929. Препарат містить натрію гідрокарбонат і натрію хлорид. Запропонуйте метод кількісного визначення натрію гідрокарбонату:
A. Меркуриметричне титрування
B. Дихроматометрія
C. Церіметрія
D. Меркурометричне титрування
E. *Кислотно-основне титрування
930. До кислотно-основного титрування належать методи:
A. комплексонометрія
B. дихроматометрія
C. метод Гей Люссака
D. меркуриметрія
E. *ацидиметрія
931. В методі нейтралізації застосовують реакції:
A. *кислотно-основної взаємодії
B. комплексоутворення
C. осадження
D. конкуруючі
E. окиснення-відновлення
932. Титрантами методу нейтралізації є стандартні розчини кислот і лугів, які є вторинними стандартними речовинами. Виберіть речовину, за якою стандартизують розчин хлоридної кислоти за методом окремих наважок:
A. CaCO3
B. Na2S2O3
C. HNO3
D. *Na2CO3
E. H2C2O4
933. Як називається момент титрування, коли кількості реагуючих речовин є еквівалентними?
A. Точкою нейтралізації
B. Показником титрування
C. Кінцевою точкою титрування
D. *Точкою еквівалентності
E. Перетитруванням
934. За допомогою яких індикаторів фіксується точка еквівалентності за методом кислотно - основного титрування?
A. Без індикаторів
B. Редокс - індикаторів
C. *рН - індикаторів
D. Адсорбційних індикаторів
E. Індикаторів - реагентів
935. До кислотно-основного титрування належать методи:
A. комплексонометрія
B. *ацидиметрія
C. метод Гей Люссака
D. меркуриметрія
E. дихроматометрія
936. В методі нейтралізації застосовують реакції:
A. *кислотно-основної взаємодії
B. комплексоутворення
C. осадження
D. конкуруючі
E. окиснення-відновлення
937. Титрантами методу нейтралізації є стандартні розчини кислот і лугів, які є вторинними стандартними речовинами. Виберіть речовину, за якою стандартизують розчин хлоридної кислоти за методом окремих наважок:
A. *Na2CO3
B. Na2S2O3
C. HNO3
D. CaCO3
E. H2C2O4
938. За допомогою яких індикаторів фіксується точка еквівалентності за методом кислотно-основного титрування?
A. Без індикаторів
B. *рН - індикаторів
C. Редокс - індикаторів
D. Адсорбційних індикаторів
E. Індикаторів - реагентів
939. В методі кислотно-основного титрування визначають:
A. *кислоти, основи і солі, що гідролізують
B. тільки солі, що гідролізують
C. сильні кислоти і слабкі основи
D. тільки сильні основи
E. тільки сильні кислоти
940. До 10,0 мл 0,1 моль/л розчину хлоридної кислоти додали 12,0 мл 0,1 моль/л розчину натрію гідроксиду. Яким буде забарвлення розчину в присутності фенолфталеїну:
A. Жовтий
B. Оранжево-рожевий
C. *Малинове
D. Червоне
E. Безколірний розчин
941. Для підвищення сили кислоти необхідно застосовувати:
A. Малополярні розчинники
B. Диференціюючі розчинники
C. Нівелюючі розчинники
D. Кислотні розчинники (з протонодонорними властивостями)
E. *Розчинники з основними (протоно-акцепторними) властивостями
942. Як називається метод аналізу, в якому робочим розчином є луг?
A. Гравіметрія
B. Редоксиметрія
C. Комплексонометрія
D. *Алкаліметрія
E. Ацидиметрія
943. Як називається спосіб титрування, за якого до аналізованої речовини А поступово додається речовина В, через деякий час відтитровують продукт їх взаємодії до встановлення точки еквівалентності?
A. Титруванням залишку
B. Титруванням замісника
C. Прямим
D. Зворотним
E. *Непрямим
944. Зворотнє кислотно-основне титрування застосовують при визначенні речовин:
A. KOH
B. NaOH
C. HCl
D. H2SO4
E. *CH3COOH
945. В методі кислотно-основного титрування не проводять титрування.
A. *слабкої основи слабкою кислотою
B. солі слабкої кислоти сильною кислотою
C. слабкої основи сильною кислотою
D. слабкої кислоти сильною основою
E. сильної кислоти сильною основою
946. Як називається титрований розчин, виготовлений за точною масою наважки із початкової речовини?
A. Титрованим
B. Стандартизованим
C. Розчином, приготовленим із стандарт - титру
D. Розчином із встановленим титром
E. *Розчином з приготовленим титром
947. Зміну забарвлення кислотно-основних індикаторів якісно і кількісно пояснює теорія індикаторів:
A. адсорбційна
B. металохромна
C. *іонно-хромофорна
D. хромофорна
E. іонна
948. У методах титриметричного аналізу використовують індикатори. Які індикатори використовують в методі нейтралізації?
A. редоксіндикатори
B. *кислотно-основні індикатори
C. зовнішні індикатори
D. окисно-відновні індикатори
E. метал-індикатори
949. Що називається титром розчину?
A. Маса речовини в грамах, яка міститься в 100 мл води
B. *Маса речовини в грамах, яка міститься в 1 мл розчину
C. Кількість еквівалентів речовини, яка міститься в 1 л розчину
D. Маса речовини в грамах, яка міститься в 1 л розчину
E. Маса речовини в грамах, яка міститься в 1 мл розчинника
950. У методах титриметричного аналізу використовують реакції окиснення-відновлення; комплексоутворення; осадження; нейтралізації. Яку реакцію використовують при титруванні ацетатної кислоти розчином NaOH?
A. реакцію комплексоутворення
B. реакцію осадження
C. *реакцію нейтралізації
D. реакцію окислення бромідів до вільного брому
E. реакцію окислення-відновлення
951. У титриметричному аналізі використовують метод нейтралізації. Які робочі розчини (титранти) використовують у цьому методі?
A. КІ, KMnO4
B. KI, K2Cr2O7
C. AgNO3, BaCl2
D. *NaOH, HCl
E. NaNO2, Na2S2O3
952. Лікарський препарат містить натрію гідрокарбонат і натрію хлорид. Запропонуйте метод кількісного визначення натрію гідрокарбонату:
A. Меркуриметричне титрування
B. Дихроматометрія
C. *Кислотно-основне титрування
D. Меркурометричне титрування
E. Церіметрія
953. При застосуванні в нітритометрії для фіксації кінцевої точки титрування суміші тропеоліну з метиленовим синім в кінці титрування спостерігають:
A. Зміна синього забарвлення на червоне
B. Зміна зеленого забарвлення на синє
C. Зміна синього забарвлення на малинове
D. Зміну малиново-фіолетового забарвлення на зелене
E. *Зміну малиново-фіолетового забарвлення на синьо-голубе
954. Фіксацію кінцевої точки титрування в нітритометрії можна виконати всіма перерахованими способами, крім....
A. За допомогою суміші тропеоліну з метиленовим синім
B. *Кондуктометрично
C. Потенціометрично
D. За допомогою зовнішніх індикаторів
E. За допомогою внутрішніх індикаторів
955. Яку речовину можливо визначити прямим цериметричним титруванням?
A. *K4[Fe(CN)6]
B. KBrO3
C. KIO3
D. K2Cr2O7
E. KMnO4
956. Яку речовину неможливо визначити прямим цериметричним титруванням?
A. As2O3
B. SbCl3
C. *NaCl
D. FeSO4
E. SnCl2
957. В цериметричному титруванні ферум (ІІ) сульфату застосовують індикатор:
A. Дифенілкарбазид
B. *Фероїн
C. Дифенілкарбазон
D. Fe(SCN)3
E. K2CrO4
958. В цериметричному титруванні ферум (ІІ) сульфату застосовують індикатор:
A. Комплексо-утворюючий
B. Адсорбційний
C. рН
D. *Редокс
E. Осаджувальний
959. Яку із запропонованих речовин неможливо визначити хлорйодиметричним титруванням:
A. Окремі відновники
B. Натрій сульфіт
C. *Натрій гідрогенкарбонат
D. Гідрохінон
E. Фенол
960. Сульфіти титруються хлорйодиметрично відповідно до схеми рівняння SO32- + 2ICl + H2O = SO42- + I2 + 2H+ + 2Cl-, тому еквівалентна маса натрій сульфіту рівна:
A. 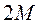
B. 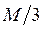
C.  ;
;
D. * 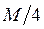
E. 
961. Гідрохінон титрують в слабко лужному середовищі розчином йод монохлориду відповідно до схеми С6H4(OH)2 + ICl + 2OH- = С6H4O2 + I- + 2H2O + Cl-, тому еквівалентна маса гідрохінону рівна:
A. 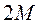
B. 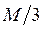
C. 
D. * 
E. 
962. Хлорйодиметричне титрування каломелі базується на реакції Hg2Cl2 + ICl + Cl- = 2HgCl2 + I-, тому еквівалентна маса каломелі рівна:
A. 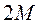
B. 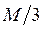
C. 
D. * 
E. 
963. Визначення вмісту води методом окиснювально-відновного титрування проводять, застосовуючи титрант:
A. Реактив Драгендорфа
B. Реактив Тромера
C. *Реактив Фішера
D. Реактив Толенса
E. Реактив Маркі
964. При йодометричному титруванні броматів відповідно до рівняння BrO3- + 6I- + 6H+ = Br- + 3I2 + 3H2O, еквівалентна маса калій бромату рівна:
A. 
B. * 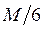
C. 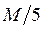
D. 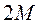
E. 
965. Відповідно до реакції окиснення тіосульфат-йонів 2S2O32- - 2e- = S4O62- еквівалентна маса натрій тіосульфату рівна:
A. * 
B. 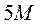
C. 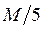
D. 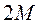
E. 
966. Натрій тіосульфат, як титрант методу..., є... стандартним розчином.
A. Дихроматометрії, вторинним
B. Хлорйодиметрії, первинним
C. Йодиметрії, вторинним
D. *Йодометрії, вторинним
E. Йодиметрії, первинним
967. Пряме йодометричне титрування калій перманганату виконується за допомогою титранту... й індикатора....
A. I2, лакмус
B. I2, метилоранж
C. I2, крохмаль
D. Na2S2O3, лакмус
E. *Na2S2O3, крохмаль
968. Пряме йодометричне титрування калій перманганату відбувається відповідно до рівняння 2KMnO4 + 10KI + 8H2SO4 → 2MnSO4 + 5I2 + 6K2SO4 + 2H2O, тому еквівалентна маса калій перманганату рівна:
A. 
B. 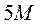
C. * 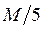
D. 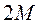
E. 
969. При йодиметричному методі визначення вмісту води в термічно лабільних субстанціях відповідно до рівняння Н2O + I2 + SO2 + 3C5H5N = C5H5N∙HI + C5H5NOSO2, тому еквівалентна маса води рівна:
A. 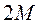
B. 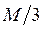
C. 
D. * 
E. 
970. Зворотнє йодиметричне титрування каломелі відбувається відповідно до рівняння Hg2Cl2 + I2 + 6KI = 2K2[HgI4] + 2KCl, тому еквівалентна маса калій перманганату рівна:
A. 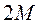
B. 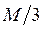
C. 
D. * 
E. 
971. При нітритометричному визначенні сульфаніламідів застосовують індикатори:
A. Метиленовий синій
B. *Тропеолін з метиленовим синім
C. Метилоранж
D. Дифенілкарбазон
E. Дифеніламін
972. Нітритометричне титрування можливе для визначення речовин:
A. K2SO4, NaNO3
B. As2O3, NaNO3
C. NaNO3, SnCl2
D. FeSO4, H2O
E. *SnCl2, FeSO4
973. При нітритометричному титруванні ферум (ІІ) сульфату згідно рівняння 2NaNO3 + 2FeSO4 + 2H2SO4 = Fe2(SO4)3 + 2NO + Na2SO4 + 2H2O, еквівалентна маса ферум (ІІ) сульфату рівна:
A. 
B. 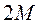
C. 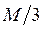
D. 
E. * 
974. При нітритометричному визначенні SnCl2 за реакцією SnCl2 + 2NaNO2 + 4НCl → SnCl4 + 2NO + 2NaCl + 2H2O, еквівалентна маса станум (ІІ) хлориду рівна:
A. 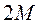
B. 
C. 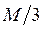
D. * 
E. 
975. Бромометричним титруванням визначають таку пару речовин:
A. Диетиловий етер, бутанол
B. *Фенол, резорцин
C. Стрептоцид, етанол
D. Фенол, метилхлорид
E. Тимол, хлороформ
976. Броматометрія застосовується для визначення такої пари речовин:
A. Диетиловий ефір, резорцин
B. Стрептоцид, хлороформ
C. Хлороформ, аргентум нітрат
D. Фенол, метилхлорид
E. *Тимол, резорцин
977. При броматометричному титруванні арсен (ІІІ) оксиду за реакцією 3As2O3 + 2KBrO3 + 2HCl → As2O5 + 2KCl + 2HBr, молярна концентрація еквівалентів і молярна концентрація титранту рівна:
A. 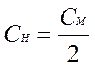
B. 
C. 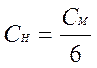
D. * 
E. 
978. При броматометричному титруванні арсен (ІІІ) оксиду за реакцією 3As2O3 + 2KBrO3 + 2HCl → As2O5 + 2KCl + 2HBr, його еквівалентна маса рівна:
A. 
B. 
C. 
D. 
E. * 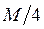
979. Метанол окиснюється калій дихроматом згідно рівняння Cr2O72- + СН3ОН + 8Н+ = 2Cr3+ + СО2 + 6Н2О, тому при дихроматометричному титруванні його еквівалентна маса рівна:
A. 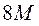
B. * 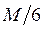
C. 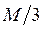
D. 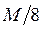
E. 
980. Гідрохінон окиснюється калій дихроматом згідно рівняння 3С6Н4(ОН)2 + Cr2O72- + 8Н+ = 2Cr3+ + С6Н4О2 + 7Н2О, тому при дихроматометричному титруванні його еквівалентна маса рівна:
A. 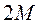
B. 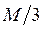
C. 
D. * 
E. 
981. При дихроматометричному визначенні гідрохінону згідно схеми С6Н4(ОН)2 - 2е- → С6Н4О2 + 2Н+ до розчину визначуваної речовини додають надлишок титранту..., який потім відтитровують стандартним розчином:
A. K2Cr2O7, NaNO3
B. FeSO4, K2Cr2O7
C. *K2Cr2O7, FeSO4
D. KMnO4, K2Cr2O7
E. K2Cr2O7, KMnO4
982. Нітрат-йони визначають зворотнім дихроматометричним титруванням - спочатку NO3- реагують з надлишком солі Fe2+
NO3- + 3Fe2+ + 4Н+ = 3Fe3+ + NO + 2H2O, а залишок солі Fe2+ відтитровують калій дихроматом. Еквівалентна маса нітрат-йонів рівна:
A. 
B. 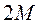
C. * 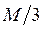
D. 
E. 
983. В основі дихроматометричного визначення вмісту FeSO4 лежить реакція 6Fe2+ + CrO72- + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O, тому його еквівалентна маса рівна:
A. 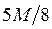
B. 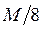
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1774; Нарушение авторских прав?; Мы поможем в написании вашей работы!