
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ЗАНЯТТЯ № 6
|
|
|
|
1. ТЕМА: Приготування розчинів.
2. ОБҐРУНТУВАННЯ ТЕМИ. Розчини з молекулярним та іонним характером дисперсності розчиненої речовини - справжні розчини - найважливіша складова частина біологічних рідин. Водні розчини електролітів та низькомолекулярних речовин забезпечують постійний осмотичний тиск, активну реакцію середовища, буферні властивості рідин організму, регулюють величини мембранних потенціалів, активність ферментів тощо. Так знання теорії розчинів, а також методики їх приготування, необхідні для ycпішнoro засвоєння студентами біохімії, фармакології, фізіології, гігієни та ін.
3.МЕТА. Сформувати уявлення про роль розчинів у життєдіяльності організму і вивчити основні положення теорії розчинів; оволодіти методикою приготування розчинів точної концентрації.
Студент повинен знати:
- основні положення теорії розчинів;
- формули для визначення кількості та маси розчиненої речовини, переводу масових одиниць в об’ємні;
- системні і позасистемні одиниці вимірювання концентрації розчинів;
вміти:
- проводити розрахунки наважки розчиненої речовини для приготування розчину певної концентрації;
- користуватися мірним посудом при приготуванні розчинів.
оволодіти навичками:
- приготування розчинів з концентраціями, що застосовуються в медичній практиці, а також для клінічних та хімічних досліджень (масова частка, молярна концентрація та молярна концентрація еквівалента).
4. ОСНОВНІ БАЗОВІ ЗНАННЯ, ВМІННЯ І НАВИЧКИ, НЕОБХІДНІ
ДЛЯ ЗАСВОЄННЯ ТЕМИ.
І) Основні величини, що характеризують склад розчинів.
2) Формули для обчислення концентрації розчину.
3) Зважування на технохімічних та аналітичних терезах.
(Матеріал шкільної програми та попереднього заняття з хімії)
5. ГРАФ ЛОГІЧНОЇ СТРУКТУРИ

 Теорія розчинів Приготування розчинів
Теорія розчинів Приготування розчинів
 | |||||
 | |||||
 | |||||
Сольватна Термодинаміка По разрахованій З фіксаналів

 теорія розчинів наважці
теорія розчинів наважці
розчинів
Розчинність розчинів масових розчинів об’ємних

 концентрацій концентрацій
концентрацій концентрацій
газів рідин твердих речовин
6. ОРІЄНТОВНА КАРТКА ДЛЯ САМОПІДГОТОВКИ ДО ЗАНЯТТЯ
(для самостійної позааудиторної роботи студентів)
| Зміст і послідовність дій | Вказівки до навчальних дій |
| 1.Теорія розчинів. | 1.1 Сольватна теорія розчинів. 1.2 Термодинаміка процесу розчинення. |
| 2. Розчинність газів, рідин та твердих речовин. | 2.1. Залежність розчинності газів від тиску (закон Генрі-Дальтона), їх природи, температури. 2.2. Вплив електролітів на розчинність газів (закон Сеченова), кесонна хвороба. 2.3. Розчинність рідин та твердих речовин. Закон розподілу Нернста та його значення для пояснення проникності біологічних мембран. |
| 3. Приготування розчинів заданого складу. | 3.1. Приготування розчинів із фіксаналів. 3.2. Приготування розчинів по розрахованій наважці. |
7. ПИТАННЯ ДЛЯ САМОСТІЙНОГО ОПРАЦЮВАННЯ
(самостійна позааудиторна робота студентів)
1) Чому при розчиненні нітрату амонію у воді розчин має нижчу температуру, ніж повітря, а при розчиненні сірчаної кислоти – набагато більшу?
2) Чим відрізняється склад водного розчину цукру від водного розчину хлориду натрію?
3) Чому водолаз з великих глибин повинен підніматися поступово, повільно, а не швидко?
4) Уведення в організм людини 3×10-9 кг адреналіну (Мr = 183,2) викликає збільшення частоти пульсу. Розрахувати діючу в цьому випадку концентрацію адреналіну в організмі, припустивши, що людина масою 70 кг має 5 л крові.
5) Для визначення калію в слині методом полуменевоі фотометрії потрібно приготувати 0,25 л розчину, що містить 0,04 ммоль/л катіону калію та 0,64 ммоль/л катіону натрію.
Як приготувати такий розчин з розчину (І) хлориду калію (С1(К+) = 1ммоль/л) та розчину (2) хлориду натрію (С2(Nа+) = 2 ммоль/л)?
6) Який об’єм розчину з масовою часткою сірчаної кислоти 9,3% (густина 1,06 кг/л) необхідно взяти для приготування 0,05 л розчину з молярною концентрацією еквівалента сірчаної кислоти 0,35 моль/л?
ПРАВИЛЬНІ ВІДПОВІДІ
1) Згідно з теорією розчинів, при розчиненні мають місце два процеси: руйнування, розклад первинної структури (кристалічної, аморфної, надмолекулярної) та побудова сольватів - утворень продуктів розпаду з молекулами розчинника (для води такі утворення називаються гідратами). Перший процес є ендотермічним, тобто проходить з поглинанням енергії, а другий - екзотермічний (проходить з виділенням енергії). Розчинення нітрату амонію супроводжується зниженням температури. Це означає, що руйнування кристалічної структури потребує більше енергії, ніж виділяється при утворенні гідратів. А при розчиненні сірчаної кислоти, навпаки, виділяється набагато більше енергії при утворенні гідратів, ніж у першому процесі.
2) Згідно з теорією, обидва розчини складаються з молекул і асоціатів води та гідратів молекул цукру (розчин цукру) і гідратів катіонів натрію, хлорид-іонів (розчин хлориду натрію). Розчин цукру не містить гідратованих іонів, а в розчині солі немає гідратованих молекул.
3) Якщо водолаз працює на значній глибині, то розчинність азоту повітря, яким він дихає, у нього в крові зростає. Це пов'язано з тим. що із збільшен-ням глибини підвищується і тиск. А, як відомо, розчинність газів із підвищенням тиску зростає. Коли водолаза піднімати на поверхню без необхідної поступовості, то азот починає виділятися з такою швидкістю, що може викликати розрив судин або їх закупорювання. У літературі наведені випадки загибелі водолазів від кесонної хвороби.
4) Вміст адреналіну в крові людинивизначається в ммоль/л.
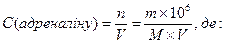 n – кількість речовини
n – кількість речовини
адреналіну, ммоль. m – маса адреналіну, кг;
М – молярна маса адреналіну, кг/кмоль;
106 – перехідний коефіцієнт від кмоль до ммоль
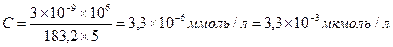
На одиницю маси людини концентрація адреналіну складає: 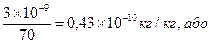
W (адреналіну) = 4,3×10-9%
У позасистемних одиницях концентрація адреналіну має такі значення:
0,43×10 -10 кг/кг × 10-1×10-6 = 4,3×10-6 мг% або 4,3×10-3 мкг%.
5) Визначаємо кількість речовини катіонів калію та натрію у 0,25 л розчину:
n(K+) = C(K+)×V = 0,04×0,25 = 0,01 ммоль
n(Na+) = C(Na+)×V = 0,64×0,25 = 0,16 ммоль
Визначаємо об’єми розчинів (1) та (2):
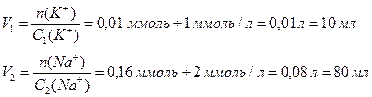
Для приготування 0,25 л потрібного розчину необхідно відібрати піпеткою 10 мл розчину (1) та 80 мл розчину (2), перенести ці об’єми у мірну колбу місткістю 0,25 л, довести рівень розчину дистильованою водою до риски. Готовий розчин перемішати.
6) Визначаємо кількість речовини еквівалента кислоти, що містить розчин, який треба приготувати:
n(1/2H2SO4) = C(1/2H2SO4)×V = 0,35 × 0,05 = 0,0175 моль
Визначаємо масу кислоти:
m(H2SO4) = n(1/2H2SO4) × M(1/2H2SO4) = 0,0175× 49 = 0,8575 г
Визначаємо масу розчину кислоти, який необхідно взяти для приготування заданого розчину:
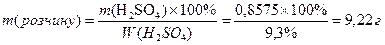
Розраховуємо об’єм цього розчину:
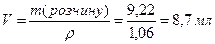
Отже: для приготування 0,05 л розчину з молярною концентрацією еквівалента сірчаної кислоти 0,35 моль/л треба взяти 8,7 мл (піпеткою) розчину сірчаної кислоти з масовою часткою 9,3%, перенести в мірну колбу місткістю 50 мл та довести об’єм розчину у колбі дистильованою водою до риски.
8. ВКАЗІВКИ ДО РОБОТИ СТУДЕНТІВ НА ЗАНЯТТІ.
8.1. Приготування розчинівіз фіксаналів.
Для приготування розчину із фіксаналу необхідно вміст ампули кількісно перенести у мірну колбу та розвести дистильованою водою до мітки. Перенесення вмісту фіксаналу в колбу: етикетку або напис з ампули зняти, ампулу вимити і промити дистильованою водою. У мірну колбу потрібного об’єму (1,0; 0,5; 0,25 л) вставляють лійку діаметром 9-10 см, в якій розміщують бойок з розширенням. Цим бойком пробивають фіксанал з одного боку, тримаючи фіксанал вертикально. Іншим бойком пробивають фіксанал з другого боку і дають змогу вмісту його перейти крізь лійку у колбу. Не змінюючи положення ампули, її обережно, але ретельно промивають дистильованою водою. Об’єм води повинен не менше, ніж у шість разів перевищувати об’єм фіксаналу. Після розчинення вмісту ампули об’єм рідини у колбі доводять дистильованою водою до мітки. Готовий розчин ретельно перемішують.
8.2. Приготування розчинів заданої концентрації по розрахованій наважці.
Кожний студент одержує у викладача картку з індивідуальним завданням: приготувати розчин лікарського препарату певної концентрації з поясненням застосування його в медичній практиці. Спочатку виконує необхідні розрахунки, а потім, з дозволу викладача, готує розчин.
Приготування розчину масової концентрації. Розраховану наважку речовини зважити на технохімічних терезах, перенести її в будь-який немірний посуд та додати розраховану кількість води. Готовий розчин перемішати до розчинення наважки.
Приготування розчинів молярної концентрації та молярної концентрації еквівалента.
Розраховану наважку зважити на аналітичних терезах (рідкі речовини відбирають піпеткою), кількісно перенести у мірну колбу потрібного об’єму (у колбу перед цим внести невеликий об’єм дистильованої води). Наважку спочатку розчинити у воді, а потім долити у колбу дистильовану воду до мітки. Готовий розчин перемішати.
Кожен студент одержує у викладача картку з індивідуальним завданням приготувати розчин певної концентрації.
8.3. Оформлення протоколу лабораторної роботи.
Зробити у зошиті необхідні розрахунки та описати порядок приготування розчину згідно з індивідуальним завданням.
9. ЛІТЕРАТУРА.
1. Мороз А.С., Луцевич Д.Д., Яворська Л.П. Медична хімія. –В: НОВА КНИГА, 2006, с. 87-94, 100-111..
2. Медицинская химия: учеб. / В.А. Калибабчук, Л.И. Грищенко, В.И. Галинская и др.; под ред. В.А. Калибабчук. – К.: Медицина, 2008.
3. Мороз А.С. Ковальова А.Г. Фізична та колоїдна хімія. Львів, Світ. 1994, с. 30-35.
4. Садовничая Л.П.. Хухрянский В.Г. Биофизическая химия. Киев, Вища школа. 1986, с.37-68
5. Ленский А.С. Ввдение в бионеорганическую химию. М., Высшая школа, 1989, с. 93-112.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 682; Нарушение авторских прав?; Мы поможем в написании вашей работы!