
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ЗАНЯТТЯ № 7
|
|
|
|
1. ТЕМА: Основи титриметричного аналізу.
2. ОБҐРУНТУВАННЯ ТЕМИ. Діагностика багатьох захворювань, першза все, базується на даних клінічних, біохімічних, фізико-хімічних методів аналізу. Одним з основних методів хімічного аналізу є титриметричний аналіз. Він охоплює і метод нейтралізації у двох його варіантах: алкаліметрія та ацидиметрія. Метод нейтралізації застосовується для визначення кислотності шлункового соку,сечі,інших біологічних рідин, вмісту хлоридів у сироватці крові. У санітарно-гігієнічному аналізі метод нейтралізації застосовується для дослідження питної води, визначення кислотності харчових продуктів. Основні поняття про теорію та методи титриметричного аналізу, і метод нейтралізації зокрема, необхідні студенту для вивчення біохімії, фармакології, гігієни.
3. МЕТА. Засвоїти теоретичні основи титриметричного аналізу, методу нейтралізації та оволодіти технікою титрування.
Студент повинен знати:
- основні поняття титриметричного аналізу;
- суть методу нейтралізації;
- теорію індикаторів у методі нейтралізації;
- принципи підбору індикаторів для визначення кінця титрування за кривими титрування.
вміти
- підбирати індикатор для конкретного титрування;
- фіксувати кінець титрування в методі нейтралізації за допомогою індикаторів;
- проводити розрахунки за формулами титриметричного аналізу.
оволодіти навичками:
- користування піпетками, бюретками при титруванні;
- технікою титрування;
- визначення кількісного вмісту кислот у розчинах та біологічних рідинах методом нейтралізації (алкаліметрія).
4. ОСНОВНІ БАЗОВІ ЗНАННЯ, ВМІННЯ І НАВИЧКИ, НЕОБХІДНІ ДЛЯ ЗАСВОЄННЯ ТЕМИ.
1) Суть реакції нейтралізації.
2) Складання рівнянь реакцій нейтралізації в молекулярнійтаіонній формах.
3) Поняття про розчини, види концентрації розчинів.
4) Використання формул масової частки, молярної концентрації, молярної концентрації еквівалента для проведення розрахунків.
(Матеріал шкільної програми та попередніх занять з хімії)
5. ГРАФ ЛОГІЧНОЇ СТРУКТУРИ.
Титриметричний (об’ємний) аналіз

 Криві титрування Метод нейтралізації Теорія кислотно-
Криві титрування Метод нейтралізації Теорія кислотно-

 основних
основних
індикаторів
Алкаліметрія Ацидиметрія
 |
Визначення вмісту оцтової кислоти в розчині
6. ОРІЄНТОВНА КАРТКА ДЛЯ САМОПІДГОТОВКИ ДО ЗАНЯТТЯ
(самостійна позааудиторна робота студентів)
| Зміст і послідовність дій. | Вказівки до навчальних дій. |
| 1.Суть титриметричного аналізу. | 1.1. Основні поняття титриметричного аналізу. 1.2. Техніка титрування. 1.3. Розрахунки в титриметричному аналізі. |
| 2. Метод нейтралізації. | 2.1. Реакції, на яких базується метод нейтралізації. 2.2. Точка еквівалентності в методі нейтралізації. |
| 3. Кислотно-основні індикатори. | 3.1. Одно- та двохкольорові індикатори. 3.2. Інтервал переходу забарвлення індикатора. 3.3. Показник титрування індикатора. |
| 4. Криві титрування у методі нейтралізації. | 4.1. Стрибок титрування. 4.2. Принцип підбору індикатора. |
| 5. Застосування алкаліметрії та ацидиметрії. |
7. ПИТАННЯ ДЛЯ САМОСТІЙНОГО ОПРАЦЮВАННЯ
(самостійна позааудиторна робота студентів)
1) Вибрати групу речовин, вмістяких може бути визначений в
розчині методом алкаліметрії
а) НСІ, NaОН, K2CO3 ; в) НСІ, СН3СООН, NаНСО3;
б)КОН, NН3, СаSО4;г) (NH4)2SO4, NH4СІ, NаСІ.
2) Вибрати індикатор,за допомогою якого можна визначити концентрацію сильної кислоти в розчині алкаліметричним титруванням
а) фенолфталеїн (8,2 -10,0) в) лакмуc (4,4 - 6,4)
б) метиловий оранжевий (3,1 - 4,4) г) метиловий червоний (4,4 - 6,2)
3) Вибрати індикатор, що може бути застосований для визначення вмісту речовин, які створюють у біологічній рідині слабокислу реакцію середовища, якщо стрибок на кривій алкаліметричного титрування складав 7,8 - 10,9 рН (у дужках показані інтервали переходу забарвлення індикаторів)
а) фенолфталеїн (8,2 - 10,0)в) метилрот (4,4 - 6,2)
б) метилоранж (3,1 - 4,4) г) нафтилфталеїн (7,4 - 8,6)
4) Вибрати групу кислот, розчини яких застосовують як робочі
у методі ацидиметрії
а) НСІ, Н2S04, СН3СООНв) H3PO4, H2S, НзВОз
б) СН3СООН, H2C2O4, Н3РО4г) НСІ, НNО3, Н2SO4
5) На титрування 25,0 см3 (мл) розчину аміаку витрачено 25,05 cм3 (мл) розчину з молярною концентрацією еквівалента НСl 0,1244 моль/дм3. Визначити вміст аміаку в розчині (вг/дм3).
ПРАВИЛЬНІ ВІДПОВІДІ
1) Правильна відповідьв).
Методом алкаліметрії можна визначити в розчині або в біологічній рідині сильні та слабкі кислоти, кислі солі та речовини з кислою реакцією середовища.
2) Будь-який з наведених індикаторів, тому що інтервал переходу забарвлення всіх цих індикаторів лежить у межах стрибка рН на кривій титрування сильної кислоти.
3) Правильна відповідьа)
Лише фенолфталеїн має інтервал переходу забарвлення, що лежить
у межах стрибка рН на кривій титрування, тому він забезпечить фіксацію точки еквівалентності з найменшою похибкою.
4) Правильна відповідь г).
Робочі розчини в ацидиметрії - це розчини сильних кислот, застосування яких забезпечує великий стрибок на кривій титрування та можливість використання переважної більшості кислотно-основних індикаторів з інтервалом переходу забарвлення у кислому середовищі.
5) Визначаємо молярну концентрацію еквівалента розчину аміаку: 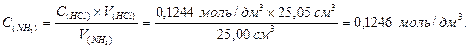 Визначаємо масу аміаку в 1 дм3 (л) розчину:
Визначаємо масу аміаку в 1 дм3 (л) розчину:
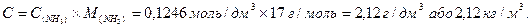
8. ВКАЗІВКИ ДО РОБОТИ СТУДЕНТІВ НА ЗАНЯТТІ
8.1. Ознайомлення з методикою виконання об’ємного аналізу.
Для одержання правильних результатів всі операції в об’ємному аналізі слід виконувати дуже ретельно. Перед початком роботи потрібно переконатися у наявності необхідного посуду і його готовності до роботи, уважно ознайомитися з методикою аналізу, приготувати зошит для запису результатів.
Наповнення бюретки робочим розчином. Бюретку обполіскують спочатку дистильованою водою, а потім розчином, яким будуть її заповнювати. Після цього робочий розчин наливають у бюретку трохи вище нульової поділки. Пухирець повітря із носика бюретки виганяють, відігнувши злегка носик догори і надавлюючи при цьому на затискач (чи кульку) бюретки. Після того, як носик повністю заповнений розчином та вийнята лійка, через яку наливали розчин, встановлюють рівень розчину на нульовій поділці. Натискуючи на затискач, по краплях випускають розчин з бюретки доти, доки нижня частина меніску безбарвного розчину або верхня частина меніску забарвленого розчину не буде на рівні нульової поділки. Проводити відлік слід завжди так, щоб око знаходилося на одному рівні з меніском.
Відмірювання розчинів піпетками.
Хімічні піпетки використовують, щоб відібрати точний об’єм потрібного розчину. Спочатку піпетку обполіскують, набираючи цей розчин приблизно до половини. При цьому занурюють піпетку у розчин майже до дна. Набирають розчин трохи вище мітки. Верхній кінець піпетки швидко затискують вказівним пальцем, піпетку виймаютьіз розчину. Послаблюючи тиск пальця, дають надлишку розчину витекти по краплях, щоб меніск встановився точно проти мітки. Обережно, слідкуючи, щоб розчин не капав, підносять піпетку до колбочки, у яку потрібно перенести відмірений об’єм розчину. Тримаючи піпетку вертикально, відкривають верхній її кінець і дають розчину витекти (носик піпетки при цьому повинен торкатися до внутрішньої стінки горла колби). Залишок розчину не видувають і не витрушують.
Розчин, що підлягає титруванню, часто повинен містити і додаткові компоненти, які створюють певне середовище, або реагують з певною речовиною, перетворюючи її у форму, необхідну для титрування. Розчини цих компонентів відмірюють мірними циліндрами або піпетками.
Проведення титрування.
Конічну колбу з розчином, підготовленим для титрування, розміщують на білому папері під носиком бюретки. Кінчик носика повинен знаходитися на рівні горла колби. Натискуючи великим і вказівним пальцями лівої руки на затискач (або кульку), вилучають розчин у колбочку невеликими порціями. Правою рукою обережно струшують колбу для швидкого перемішування розчину. Про наближення кінця титрування свідчить те, що у місці падіння краплі робочого розчину розчин у колбі набуває характерного для кінця титрування забарвлення. Тоді робочий розчин починають додавати по одній краплі. Після стійкої зміни забарвлення титрування припиняють і визначають об’єм робочого розчину, витраченого на титрування. Титрування проводять не менше трьох разів.
8.2. Визначення масової частки оцтової кислоти.
За допомогою піпетки відібрати 10,0 мл розчину оцтової кислоти і перенести в конічну колбу ємністю 50-100 мл, додати 2-3 краплі фенолфталеїну і титрувати з бюретки робочим розчином гідроксиду натрію до появи блідо-рожевого забарвлення. Визначити (за шкалою бюретки) об'єм робочого розчину лугу, витраченого на титрування. Повторити титрування ще двічі та з одержаних результатів вирахувати середнє арифметичне значення об’єму NaOH-Vсер.(NaOH):
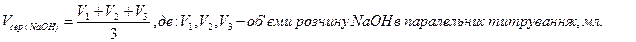 Розрахунок масової частки оцтової кислоти:
Розрахунок масової частки оцтової кислоти:
1) знайти молярну концентрацію еквівалента оцтової кислоти в розчині:
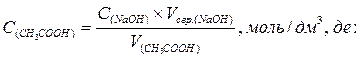
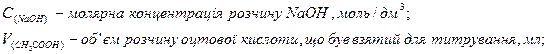
2) знайти масу оцтової кислоти в одному літрі розчину:
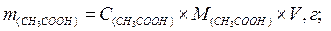
де: V = 1дм3(л) – об’єм розчину кислоти;
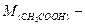 молярна маса еквівалента СН3СООН, г/моль;
молярна маса еквівалента СН3СООН, г/моль;
3) знайти масову частку оцтової кислоти у наважці
(наважка - це певна маса концентрованої оцтової кислоти, із якої готувався 1 дм3(л) розчину, що досліджувався):
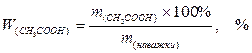
8.3. Оформлення протоколу лабораторної роботи.
Зробити у зошиті необхідні розрахунки та висновок.
9. ЛІТЕРАТУРА.
1. Мороз А.С., Луцевич Д.Д., Яворська Л.П. Медична хімія. –В: НОВА КНИГА, 2006, с. 313-364.
2. Медицинская химия: учеб. / В.А. Калибабчук, Л.И. Грищенко, В.И. Галинская и др.; под ред. В.А. Калибабчук. – К.: Медицина, 2008.
3. Селезнёв К.А. Аналитичская химия. М., Химия, 1973, с. 164-199.
4. Бабков А.В. и др. Практикум по общей химии с элементами количественного анализа. М., Высшая школа, 1978, с. 74-109.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 971; Нарушение авторских прав?; Мы поможем в написании вашей работы!