
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Моносахариди
|
|
|
|
Моносахариди – це прості сахара, які не здатні до реакції гідролізу. Вони самі є кінцевими продуктами реакції гідролізу більш складних вуглеводів.
21.2.1. Будова моносахаридів
В 60 – 80 роках минулого століття роботами відомих вчених Х. Кіліані, П. Бертло, О. Коллі, Б. Толленса, Е. Фішера та ін. було доведено, що в моносахаридах є нерозгалужений карбоновий ланцюг, оскільки в результаті відновлення йодистоводневою кислотою глюкози і фруктози одержали
2-йодогексан:
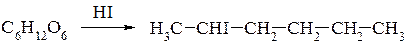
В моносахаридах є карбонільна група, тому в результаті окиснення глюкози утворюється глюконова кислота:
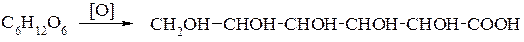
При окисненні фруктози утворюються дві кислоти – щавлева і винна, що говорить про наявність кетонної групи:
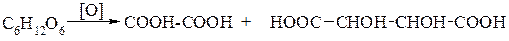
Інші атоми Карбону мають гідроксильні групи, оскільки в результаті реакції ацилювання утворюється пентаацетилглюкоза:
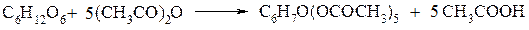
З урахуванням всього цього було зроблено висновок, що моносахариди є гідроксикарбонільними сполуками, тобто є багатоатомними гідроксиальдегідами або гідроксикетонами з відкритим карбоновим ланцюгом.
Таким чином, глюкоза являється багатоатомним а льдегідоспиртом такої будови:
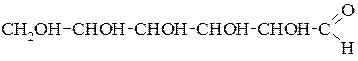
а фруктоза – багатоатомним кетоспиртом такої будови:
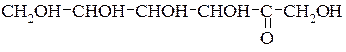
Ці формули були запропоновані Фішером, ще їх називають гідроксикарбонільними.
Моносахариди, які подібно глюкозі містять альдегідну групу, називають альдозами, а моносахариди, що містять кетогрупу – кетозами.
За кількістю атомів Карбону, моносахариди поділяють на тріози
(3–С), тетрози (4–С), пентози (5–С), гексози (6–С), гептози (7–С), октози
(8–С), нонози (9–С), декози (10–С), або їх можна представити так:
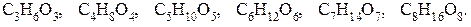
Щоб підкреслити, що до складу моносахариду входить альдегідна група, і також він містить, наприклад, шість атомів Карбону, його назву об’єднують в одне слово і одержують «альдогексоза», аналогічно «кетогексоза» чи «альдопентоза» і т. д.
21.2.2. Стереохімія моноз
Просторові конформації моносахаридів D- і L-ряду.
Моносахариди містять асиметричні атоми Карбону (С*), тому для них характерна наявність великої кількості стереоізомерів. Для альдогексоз — 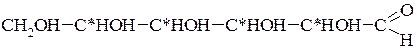
які мають чотири асиметричні атоми Карбону згідно формули N = 2n кількість стереоізомерів дорівнює 24 = 16. Одна половина є антиподами іншої половини. Таким чином, 16 стереоізомерів альдогексоз утворюють 8 пар антиподів. Наприклад, природному моносахариду D-глюкозі відповідає синтетично добутий антипод L-глюкоза.

Нумерацію ланцюга атомів Карбону починають від альдегідної групи, в кетозах з того кінця де ближче знаходиться кетонна група.
Визначення взаємного розташування Н- і ОН-груп у кожного асиметричного центру є важким завданням.
В 1906 р. М.А. Розанов запропонував розглядати приналежність того чи іншого моносахариду до D- чи L-ряду за розміщенням у просторі атомних груп біля останнього асиметричного (найбільш віддаленого від карбонільної групи) атому Карбону (у карбоновому ланцюзі він передостанній).
Якщо конфігурація співпадає з конфігурацією D-гліцеринового альдегіду, то моносахарид відноситься до D-ряду, якщо ж конфігурація співпадає з конфігурацією L-гліцеринового альдегіду, то моносахарид відноситься до
L-ряду.

Таким чином, виходячи з D-гліцеринового альдегіду можна вивести генетичний ряд сахарів D-ряду:
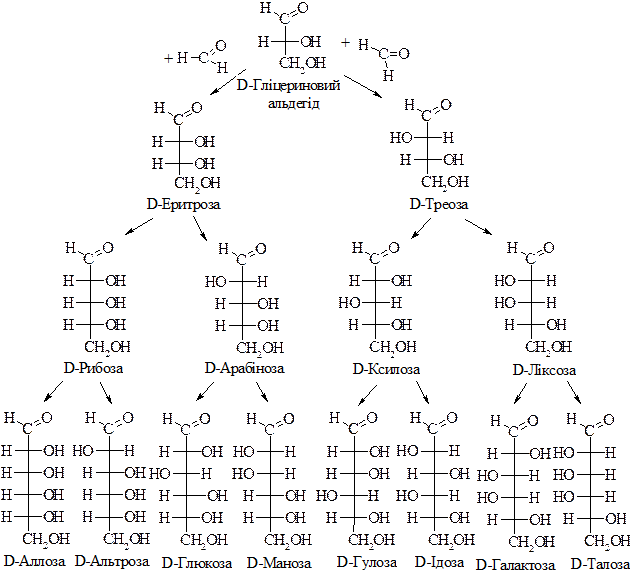
Антиподом (дзеркальним відображенням) кожного з представників цієї схеми моносахаридів є відповідний моносахарид L-ряду.
Позначення «D» і «L» зовсім не визначають напрямок обертання розчинами сахарів площини поляризації плоскополяризованого світла, оскільки обертаюча здатність залежить від положення замісників не тільки біля асиметричного атома Карбону, що визначає приналежність моносахариду до якогось ряду, а і біля всіх інших асиметричних атомів. Наприклад, природна
D-фруктоза обертає площину поляризації світла вліво (-).
21.2.3. Циклічна структура моносахаридів
Альдегідні та кетонні (гідроксикарбонільні) формули Фішера моносахаридів добре пояснювали властивості цих речовин, але поступово накопичувалися деякі факти з хімічних і фізичних властивостей моносахаридів, які не можливо було пояснити цими формулами.
1. Так, було встановлено, що моносахариди, як альдегіди не дають деяких реакцій, характерних для альдегідної групи (з бісульфітом натрію (NaHSO3), з фуксинсульфітною кислотою).
2. Усі моносахариди є оптично активними речовинами. Кут обертання площини поляризації світла свіжого розчину моносахариду при стоянні змінюється (збільшується, або зменшується) доки не досягне сталої величини, характерної для певного моносахариду. Це явище дістало назву – явища мутаротації. Наприклад, свіжоприготовлений розчин глюкози має кут +110°, а при стоянні стає +52,5° і більше не змінюється.
3. Виходячи з формули Фішера, для альдогексоз існує 16 діастереоізомерів. Дійсно, цю кількість альдоз було знайдено в природі і синтезовано Фішером, однак, подальші дослідження показали, що кожний з цих моносахаридів може існувати у двох абсолютно індивідуальних кристалічних формах з різними константами, в тому числі з різними кутами обертання.
Так, наприклад, були добуті дві D-глюкози з кутами обертання (+110° — +113°) і +19,3°. Цікаво те, що при розчиненні обох форм завжди утворюється розчин, кут обертання якого змінюється внаслідок мутаротації і поступово досягає для обох форм сталої величини +52,5°.
Таким чином, число реально існуючих альдоз дорівнює подвійному числу стереоізомерів відповідно формулі Фішера. Подвоєне число стереоізомерів можливо тільки тоді, якщо в гексозі буде 5 асиметричних атомів Карбону. Цьому не відповідала формула Фішера.
4. Одна з гідроксильних груп моносахаридів суттєво відрізняється за своїми властивостями від інших гідроксилів. Так, наприклад, при нагріванні моносахаридів зі спиртами за наявності невеликої кількості сухого гідрогенхлориду утворюється кристалічна речовина – глікозид. Глікозиди, за наявності розбавлених мінеральних кислот, дуже легко гідролізують, причому з однієї молекули глікозиду утворюється одна молекула спирту.
Якщо виходити з формули Фішера, то в молекулі глюкози є
5 гідроксильних груп, кожна з яких повинна була б дати сполуку типу етеру. Чому ж тільки один гідроксил приймає участь в утворені глікозиду? На це питання формула Фішера відповіді не дає. Усі ці фактори знайшли пояснення коли було доведено, що кожний моносахарид може існувати у вигляді ряду таутомерних форм. У розчині моносахаридів поряд з альдегідними чи кетонними формами завжди присутня циклічна таутомерна форма.
Ще в 1870 році О.А. Коллі запропонував для глюкози циклічну напівацетальну форму з трьохчленним окисним циклом:
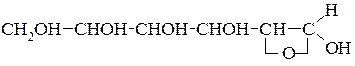
Наявність подібного кільця Коллі пояснив відсутністю деяких реакцій характерних для альдегідної групи глюкози.
Пізніше, у 1883 році Б. Толленс, запропонував аналогічну формулу, але з п’ятичленним окисним кільцем.
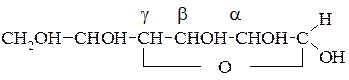
Скрауп запропонував — δ–окисне кільце.
Циклічні формули називають також окисними або напівацетальними.
Механізм утворення циклічної форми з альдегідної можна пояснити так: як відомо, альдегіди легко приєднують спирти, перетворюючись в ацеталі через стадію утворення напівацеталей:
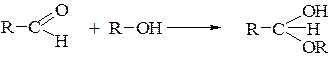
Альдегідна група моносахариду, яка розміщена близько до однієї з гідроксильних груп, взаємодіє з нею і утворює внутрішній напівацеталь.
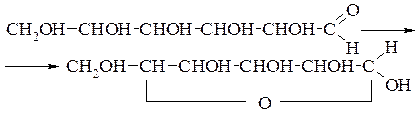
Утворення циклічних форм пояснює всі явища.
Відмічені недоліки формул Фішера:
1. Те, що моносахариди не дають деяких характерних для альдегідів реакцій пояснюється тим, що у водних розчинах моносахаридів переважає циклічна форма. Альдегідна ж форма знаходиться у невеликій кількості (інколи десяті долі %).
2. В циклічній формі моносахаридів з’являється додатково ще один асиметричний атом Карбону, який в альдегідній формі входив до складу альдегідної групи. Залежно від положення напівацетального гідроксилу біля нового асиметричного атома Карбону, розрізняють так звані α-, β-форми (або аномери) моносахаридів.
Якщо напівацетальний гідроксил розміщений по одну сторону відносно карбонового ланцюга з гідроксилом, що визначає приналежність до D- чи
L-ряду, то така форма називається a-формою (a-аномер), якщо по різні сторони – b-форма (b-аномер):

У кристалічному виді моносахариди існують у циклічній формі і є стійкими сполуками. Проте, при розчиненні індивідуального аномера у воді швидко наступає таутомерна рівновага, яка приводить до утворення еквімолярної суміші кількох форм моносахаридів, що веде до зміни кута обертання даного розчину.
3. Подвоєння кількості діастереоізомерів також пояснюється появою нового асиметричного центру. В циклічній формі моносахаридів є п’ять асиметричних атомів Карбону, що приводить до N=2n, 25=32 діастереоізомерів.
4. Утворення глікозидів за участю тільки одного гідроксилу моносахариду добре пояснюється існуванням циклічної форми. В ній є один напівацетальний гідроксил (або глікозидний). Він більш реакційно здатний, ніж інші спиртові гідроксили і взаємодіє зі спиртом, утворюючи глікозид:

Таким чином, циклічна форма сахарів пояснює ті протиріччя у властивостях моносахаридів, які не змогла пояснити гідроксикарбонільна формула Фішера.
21.2.4. Характер окисних кілець
Кільце циклічної форми може бути п'ятичленним. Р. Хеуорс (1929 р.) запропонував окисні формули моносахаридів розглядати, як похідні гетероциклічних сполук пірану і фурану.
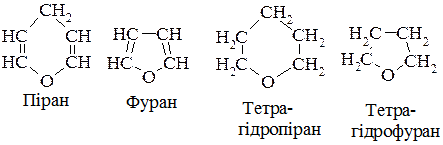
Форми моносахаридів, що мають шестичленний цикл називають піранозами, а п’ятичленний – фуранозами.
Хеуорс запропонував так звані перспективні формули моносахаридів, в яких дуже чітко видно кільце й просторові положення гідроксильних груп. Згідно до його пропозиції, циклічну форму моносахариду умовно вважають плоскою. Для зображення на папері її уявно розміщують таким чином, щоб атом Оксигену піранозного кільця знаходився на найбільшій відстані від очей спостерігача справа (у фуранозному кільці в центрі), а карбоновий ланцюг був повернутий до спостерігача.
Нумерацію ведуть за годинниковою стрілкою вниз, починаючи справа від атома Оксигену. Замісники записують зверху і знизу від площини. Всі ті замісники, які у формулах Толленса знаходяться зліва від ланцюга, записують над кільцем, а ті, що з правої сторони – під кільцем.

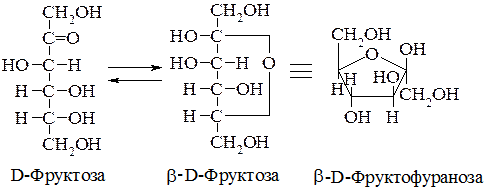
21.2.5. Таутомерна рівновага моносахаридів. Явище мутаротації
Як було відмічено, моносахариди в кристалічному вигляді існують в напівацетальній формі з кільцем із шести атомів Карбону. Так, природна
D-глюкоза є β-D-глюкопіранозою, яка при розчиненні у воді таутомерно перетворюється в гідроксикарбонільну форму, а остання переходить у всі чотири циклічні напівацетальні форми:
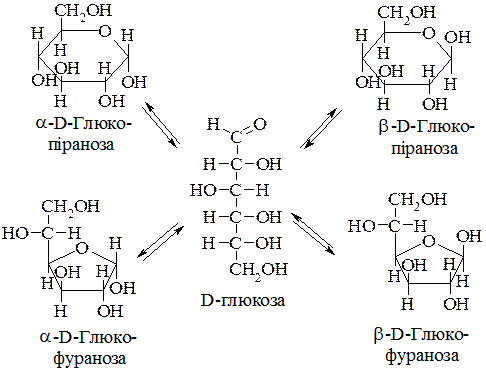
Таким чином, у водному розчині D–глюкоза, як і інші моносахариди, існує в п'яти таутомерних формах: одна гідроксикарбонільна та чотири циклічні напівацетальні.
Між цими формами в розчині встановлюється динамічна рівновага. При цьому, в рівноважній системі переважають циклічні a- і b-піранозні форми, зовсім мало циклічних a- і b-фуранозних форм і далі соті долі відсотків (0,12) гідроксикарбонільної форми.
Процес розчинення моносахаридів у воді супроводжується спеціальним оптичним ефектом, який отримав назву явища мутаротації.
Воно заключається в тому, що кут обертання свіжоприготовлених розчинів моносахаридів змінюється при стоянні поступово, доки не досягне сталої величини для певного моносахариду. Так, a - D-глюкоза, яка має кут +112,1° при стоянні зменшується до +52,2°, а b-D-глюкоза з кутом +19,2° збільшується до +52,2°. Таким чином, основна роль в явищі мутаротації — це перехід a-форми в b-форму і навпаки. Явище мутаротації в свою чергу підтверджує наявність циклічної (напівацетальної) будови моносахаридів.
21.2.6. Поняття про конформаційну ізомерію
Для сахарів в циклічній формі можливий ще один вид ізомерії – конформаційна, яка зв’язана з положенням у просторі атомів Карбону шестичленного циклу.
Для піранозного кільця через його несиметричность, пов’язану з наявністю в ньому атому Оксигену, можливі кілька типів конформацій. Найбільш переважною є крісловидна конформація, причому, така, в якій найбільше число об’ємних замісників розміщено екваторіально. Так для α-глюкози вона матиме такий вид:

|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 3133; Нарушение авторских прав?; Мы поможем в написании вашей работы!