
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Разбавленные кислоты
|
|
|
|
Сульфид натрия
Zn2+ + S2- ® ZnS ¯
3Zn2+ + 2K+ + 2[Fe(CN)6]4- ® Zn3K2[Fe(CN)6]2¯
белый
белый аморфный
Летучие соли кальция окрашивают бесцветное пламя горелки в кирпично-красный, стронция - в карминово-красный, а бария - в жёлто-зелёный цвет.
Летучие соли лития окрашивают бесцветное пламя в карминово-красный, натрия в жёлтый, а калия в светло-фиолетовый цвет.
7. Реакции идентификации неорганических анионов: бромиды, иодиды, карбонаты и гидрокарбонаты, мышьяк (арсениты и арсенаты), нитраты, нитриты, силикаты, сульфаты, сульфиты, фосфаты, хлориды.
1. Ag+ + Br- ® AgBr¯
бледно-жёлтый
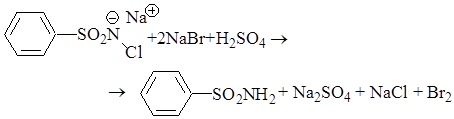
4H+PbO2 + 2Br- ® Pb2+ + Br2+ 2H2O
2. Ag+ + I- ® AgI¯
жёлтый
SO4- + 8I- + 10H+ ® 4 I2¯ + H2S + 4H2O
бурый
3. Ba2+ + СО32- ® BaСО3¯
белый
Осадок растворяется в кислотах.
CO32- + 2H+ ® CO2 + H2O
газ без цвета и запаха
3. Растворимые соли Mg2+
2Mg2+ + 2CO32- + H2O ® (MgOH)2CO3¯ + CO2
белый аморфный
4. 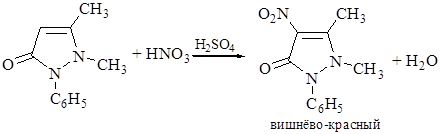
5. H2SO4- + 2NO2- ® ® NO2 + NO + H2O+ SO4-
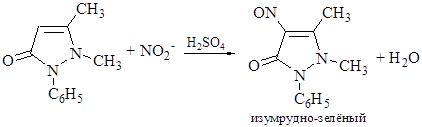
6. Ba2+ + SO42- ® BaSO4¯
белый
7. HSO3- + H+ ® SO2 + H2O
запах горящей серы
2HSO3- + I2 + ® 2SO42- + 2I- +2H+
исчезновение бурой окраски
8. 3Ag+ + PO43- ® Ag3PO4¯
жёлтый
PO43- + 3NH4+ + 12MoO42- + 24H+ ® (NH4)3[PMo12O40]¯ + 12H2O
жёлтый кристаллический
Mg2+ + PO43- + NH4 ® MgNH4PO4¯
белый кристаллический
9. 3Ag+ + AsO33- ® Ag3AsO3¯ 3Ag+ + AsO43- ® Ag3AsO4¯
жёлтый коричнево-бурый
Осадки растворяются в растворах HNO3 и NH3.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 715; Нарушение авторских прав?; Мы поможем в написании вашей работы!