
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теплоемкость газов
|
|
|
|
З-3.5
З-3.4
З-3.3
З-3.2
З-3.1
Задачи
В сосуде находится смесь, состоящая из одного киломоля кислорода и двух киломолей азота, при p1 = 0,1 МПа и t1 = 30 ºС. Эта смесь охлаждается при постоянном объеме до температуры t2 = 10 ºС.
Определить изменение внутренней энергии смеси.
Ответ: 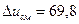 кДж/кг.
кДж/кг.
Объемный состав горючего газа: rCO =10 %, 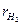 =45 %,
=45 %, 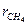 =35 %,
=35 %, 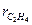 =4 %,
=4 %, 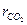 =3 %,
=3 %, 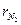 =3 %.
=3 %.
Определить кажущуюся мольную массу, плотность, удельный объем при нормальных условиях, массовую газовую постоянную R, парциальное давление метана в процентах и массовые доли содержания компонентов.
Ответ: 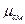 = 12,63;
= 12,63; 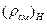 = 0,563 кг/м3; vсм = 1,776 м3/кг; Rсм =0,658 кДж/(кг·К);
= 0,563 кг/м3; vсм = 1,776 м3/кг; Rсм =0,658 кДж/(кг·К); 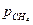 = 35 %; mCO= 0,222;
= 35 %; mCO= 0,222;  = 0,072;
= 0,072; 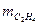 = 0,089;
= 0,089;  = 0,445;
= 0,445; 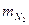 = 0,067;
= 0,067; 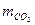 = 0,105.
= 0,105.
Объемный состав сухих продуктов сгорания топлива (не содержащих водяных паров) следующий: СО2 =12,3 %; О2 =7,2 %; N2 =80,5 %.
Найти кажущуюся молекулярную массу и газовую постоянную, а также плотность и удельный объем продуктов сгорания при В =100 кПа и t =800 ºС.
Ответ: 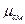 = 30,3; Rсм =274 кДж/(кг·К); v= 2,94 м3/кг;
= 30,3; Rсм =274 кДж/(кг·К); v= 2,94 м3/кг; 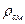 = 0,34 кг/м3.
= 0,34 кг/м3.
Найти газовую постоянную, удельный объем газовой смеси и парциальные давления ее составляющих, если объемный состав смеси следующий: СО2 =12 %; СО =1 %; Н2O =6 %; О2 =7 %; N2 =74 %; а общее давление ее р= 100 кПа.
Ответ: Rсм =281 Дж/(кг·К); v= 0,76 м3/кг; 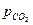 = 12000 Па;
= 12000 Па; 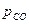 = 1000 Па;
= 1000 Па; 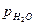 = 6000 Па;
= 6000 Па; 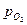 = 7000 Па;
= 7000 Па; 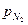 = 74000 Па.
= 74000 Па.
Газовая смесь имеет следующий массовый состав: СО2 =12 %; О2 =8 % и N2 =80 %.
До какого давления нужно сжать эту смесь, находящуюся при нормальных условиях, чтобы плотность ее составляла 1,6 кг/м3.
Ответ: до р =0,213 МПа.
В теплотехнических расчетах пользуются понятием «удельная теплоемкость», хотя называют ее просто «теплоемкость». Под удельной теплоемкостью понимают количество теплоты, которое необходимо сообщить телу, чтобы повысить температуру какой-либо его количественной единицы на 1 ºС. В зависимости от выбранной количественной единицы различают теплоемкости:
· мольную mс, кДж/(кмоль×К);
· массовую с, кДж/(кг×К);
· объемную с/, кДж/(нм3×К).
Эти теплоемкости связаны между собой следующими соотношениями:
с = mс/m; с/ = mс/ 22,4; с/ = с×rн, (4.1)
где rн – плотность газа при нормальных условиях.
1 м3 газа имеет различную массу в зависимости от давления и температуры. В связи с этим объемную теплоемкость всегда относят к массе газа, заключенной в 1 м3 при нормальных условиях. В зависимости от способа подвода тепла к газу (р = const или V = const) различают изобарную ср и изохорную сv теплоемкости. Отношение этих величин носит название показателя адиабаты
k = mcp/mcv = cp/cv. (4.2)
Теплоемкости ср и сv связаны также соотношением Майера
mсp - mcv = mR = 8,314, кДж/(кмоль×К). (4.3)
Для приближенных расчетов при невысоких температурах можно принимать следующие значения мольных теплоемкостей (таблица 3).
Таблица 3
Мольные теплоемкости газов, кДж/(кмоль×К)
| Газы | mcv | mcp | k |
| Одноатомные | 12,56 | 20,93 | 1,67 |
| Двухатомные | 20,93 | 29,31 | 1,40 |
| Многоатомные | 29,31 | 37,68 | 1,30 |
Теплоемкость газов меняется с изменением температуры, причем эта зависимость имеет криволинейный характер. Значения истинных и средних теплоемкостей в интервале от 0º до t берутся непосредственно из таблиц, причем в необходимых случаях производится интерполяция. Количество теплоты, которое необходимо затратить в процессе нагревания 1 кг газа в интервале температур от t1 до t2:
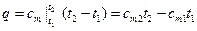 , кДж/кг. (4.4)
, кДж/кг. (4.4)
где cm1 и cm2 – соответственно средние теплоемкости в пределах 0º – t1 и 0º – t2.
Если в процессе участвуют М (кг) или Vн (м3) газа, то
QV = M(cvm2 t2 – cvm1t1) = Vн(c/vm2 t2 – c/vm1 t1), кДж;
QP = M(cpm2 t2 – cpm1 t1) = Vн(c/pm2 t2 – c/pm1 t1), кДж. (4.5)
Теплоемкость газовой смеси следует определять по формулам:
массовая - 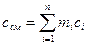 ;
;
объемная - 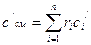 ;
;
мольная - 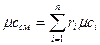 . (4.6)
. (4.6)
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 2727; Нарушение авторских прав?; Мы поможем в написании вашей работы!