
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры решения задач. Задача 1.. Возможно ли взаимодействие оксида алюминия с водой при 1000С по реакции:
|
|
|
|
Задача 1.. Возможно ли взаимодействие оксида алюминия с водой при 1000С по реакции:
А12O3 (Тв) + 3H2O(Ж) = 2Аl(ОН)3 (Tв).
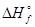 кДж/моль -1675,0 -285,8 -1295,0
кДж/моль -1675,0 -285,8 -1295,0
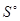 Дж/моль×К 50,9 70,0 70,0
Дж/моль×К 50,9 70,0 70,0
Как повлияет на вероятность протекания этой реакции повышение температуры?
Решение. Для решения задачи необходимо определить величину 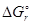 по соотношению (8).
по соотношению (8).
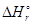 = 2
= 2 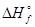 (Аl(ОН)3 (Tв)) -
(Аl(ОН)3 (Tв)) - 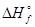 (А12O3 (Тв)) - 3
(А12O3 (Тв)) - 3 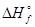 (H2O(Ж)) = 2×(-1295,0) + 1675,0 + 3×285,8 = -57.6 кДж.
(H2O(Ж)) = 2×(-1295,0) + 1675,0 + 3×285,8 = -57.6 кДж.
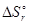 = 2
= 2 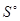 (Аl(ОН)3 (Tв)) -
(Аl(ОН)3 (Tв)) - 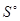 (А12O3 (Тв)) - 3
(А12O3 (Тв)) - 3 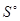 (H2O(Ж)) = 2×70,0 - 50,9 - 3×70,0 = -120,9 Дж/K.
(H2O(Ж)) = 2×70,0 - 50,9 - 3×70,0 = -120,9 Дж/K.
Учитывая, что 1000С = 373.15 К и соотношение размерностей 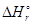 и
и 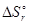 получим:
получим: 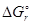 =
= 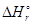 - T
- T 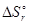 = -57,6 + 373,15×120,9×10-3 = -12,486 кДж.
= -57,6 + 373,15×120,9×10-3 = -12,486 кДж.
Поскольку 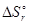 < 0, увеличение температуры уменьшит вероятность протекания реакции.
< 0, увеличение температуры уменьшит вероятность протекания реакции.
Ответ. Так как 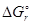 < 0, реакция в заданных условиях возможна. Увеличение температуры уменьшит вероятность протекания реакции.
< 0, реакция в заданных условиях возможна. Увеличение температуры уменьшит вероятность протекания реакции.
Задача 2. Какая из двух реакций более вероятна при температуре 298 К?
Mg (Тв) + O2(Г) = MgО (Тв)
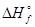 кДж/моль 0 0 -601,2
кДж/моль 0 0 -601,2
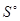 Дж/моль×К 32,6 205,0 26,9
Дж/моль×К 32,6 205,0 26,9
2) Ca (Тв) + O2(Г) = CaО (Тв)
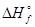 кДж/моль 0 0 -635,1
кДж/моль 0 0 -635,1
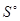 Дж/моль×К 41,6 205,0 39,7
Дж/моль×К 41,6 205,0 39,7
Решение. Ответить на поставленный вопрос можно, сопоставляя энергии Гиббса указанных реакций. Рассчитаем эти величины.
Для первой реакции: 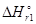 =
= 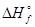 (MgО (Т)) = -601,2 кДж,
(MgО (Т)) = -601,2 кДж,
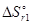 =
= 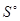 (MgО (Т)) -
(MgО (Т)) - 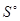 (Mg (Т)) -
(Mg (Т)) - 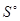 (O2(Г)) = 26,9 – 32,6 – 205,0 = -210,7 Дж/К,
(O2(Г)) = 26,9 – 32,6 – 205,0 = -210,7 Дж/К,
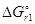 =
= 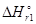 - T
- T 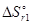 = -601,2 + 298×0,2107 = -538,4 кДж.
= -601,2 + 298×0,2107 = -538,4 кДж.
Для второй реакции: 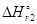 =
= 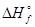 (CaО (Т)) = -635,1 кДж,
(CaО (Т)) = -635,1 кДж,
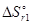 =
= 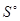 (CaО (Т)) -
(CaО (Т)) - 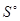 (Ca (Т)) -
(Ca (Т)) - 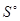 (O2(Г)) = 39,7 – 41,6 – 205,0 = -206,9 Дж/К,
(O2(Г)) = 39,7 – 41,6 – 205,0 = -206,9 Дж/К,
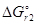 =
= 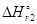 - T
- T 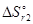 = -635,1 + 298×0,2069 = -573,4 кДж.
= -635,1 + 298×0,2069 = -573,4 кДж.
Ответ. Поскольку 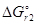 <
< 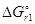 вторая реакция более вероятна.
вторая реакция более вероятна.
Задача 3. При какой температуре установится равновесие в системе, содержащей NO2(Г) и N2O4(Г)? В каком направлении будет возможно самопроизвольное протекание реакции, если понизить температуру?
Решение. Запишем уравнение химической реакции:
2NO2(Г) = N2O4(Г)
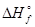 кДж/моль 33,9 9,4
кДж/моль 33,9 9,4
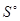 Дж/моль×К 240,5 304,3
Дж/моль×К 240,5 304,3
Определим температуру, отвечающую равновесию.
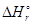 =
= 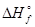 (N2O4(Г))-2
(N2O4(Г))-2 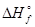 (NO2(Г)) = 9,4 - 2×33,9 = -58,4 кДж.
(NO2(Г)) = 9,4 - 2×33,9 = -58,4 кДж. 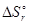 =
= 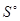 (N2O4(Г)) – 2
(N2O4(Г)) – 2 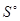 (NO2(Г)) = 304,3 - 2×240,5 = -176.7 Дж.
(NO2(Г)) = 304,3 - 2×240,5 = -176.7 Дж. 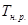 .=
.= 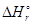 /
/ 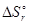 = 58400/176,7 = 330,5 К.
= 58400/176,7 = 330,5 К.
Поскольку 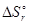 < 0, при Т <
< 0, при Т < 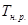 реакция возможна в прямом направлении.
реакция возможна в прямом направлении.
Ответ. Тн.р.= 330,5 К, при понижении температуры возможна реакция в сторону образования N2O4(Г).
VI. РАСЧЕТ СВОБОДНОЙ ЭНЕРГИИ ГИББСА РЕАКЦИЙ С ИСПОЛЬЗОВАНИЕМ ВЕЛИЧИН 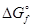
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 392; Нарушение авторских прав?; Мы поможем в написании вашей работы!