
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Обе эти величины могут быть измерены экспериментально
|
|
|
|
Если то газ охлаждается (), если наоборот – нагревается. Если - то эффект отсутствует. Совместно с уравнениями и в переменных это дает так называемую кривую инверсии. Для идеального газа такой эффект отсутствует.
34. Получить абсолютную шкалу температур.
Решение: Необходимо поставить в соответствие друг другу две температурные шкалы 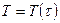 , где
, где 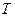 – абсолютная шкала, а
– абсолютная шкала, а 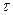 – произвольная.
– произвольная.
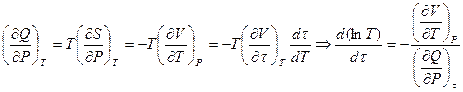 .
.
35. Исследовать магнитокалорический эффект.
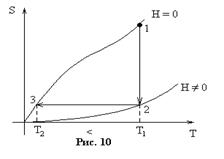 Решение: Магнитоколарический эффект применяется для получения сверхнизких температур (до
Решение: Магнитоколарический эффект применяется для получения сверхнизких температур (до 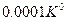 ) парамагнитных солей. Идея заключается в том, что при
) парамагнитных солей. Идея заключается в том, что при 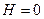 энтропия системы больше, чем при
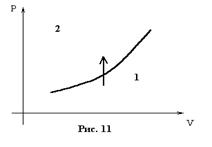
энтропия системы больше, чем при 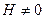 . Участок 1-2 на рисунке описывает изотермическое включение поля, а участок 2-3 – адиабатическое выключение. Запишем первое начало термодинамики с учетом работы магнитного поля
. Участок 1-2 на рисунке описывает изотермическое включение поля, а участок 2-3 – адиабатическое выключение. Запишем первое начало термодинамики с учетом работы магнитного поля 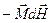 (
(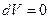 ):
):
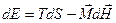 (1)
(1)
Если внутренняя энергия 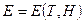 ,
,
то
 (2)
(2)
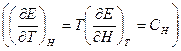 .
.
Подставляя (2) в (1) и выражая 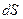 , получаем:
, получаем:
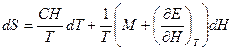 .
.
Приравнивая друг к другу вторые производные от 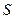 по
по 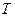 и
и 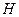 , находим:
, находим:
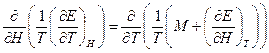
или
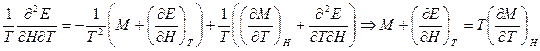
Следовательно
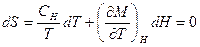 (при адиабатическом выключении).
(при адиабатическом выключении).
Таким образом
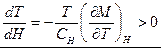 (так как
(так как 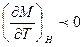 ). То есть при уменьшении
). То есть при уменьшении 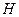 уменьшается
уменьшается 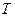 .
.
35. Получить 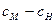 .
.
Решение: Как следует из предыдущей задачи:
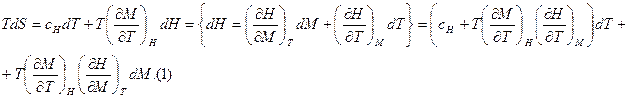
Если 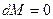 , то из (1)следует, что
, то из (1)следует, что
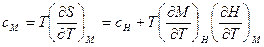 .
.
Таким образом:
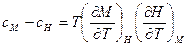
Системы с переменным числом частиц.
Рассмотрим две фазы какого-либо вещества и укажем критерии равновесия фаз (предполагается, что при этом состояния термодинамического и механического равновесия уже достигнуты, т.е. 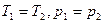 ). В силу аддитивности
). В силу аддитивности 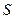 и
и 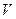
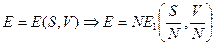
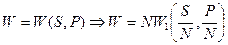
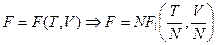
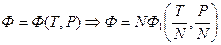 .
.
(индекс 1 означает термодинамический потенциал одной молекулы).
Учтем зависимость от 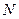 термодинамических параметров слагаемым
термодинамических параметров слагаемым 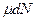 .
.
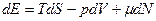
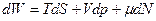
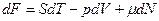
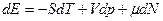
откуда
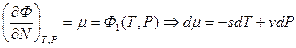 ,
,
(где 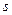 и
и 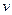 - удельные энтропия и объем)
- удельные энтропия и объем)
и 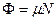 .
.
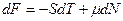 (объем выделен
(объем выделен 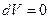 , но число частиц в нем меняется). Следовательно:
, но число частиц в нем меняется). Следовательно:
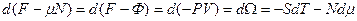 ,
,
где 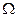 - омега-потенциал.
- омега-потенциал.
Если для двух фаз давления и температуры совпадают, то энтропия максимальна (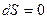 ). Тогда в силу того, что
). Тогда в силу того, что
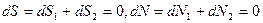 :
:
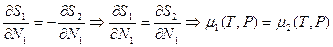 . (*)
. (*)
Кривая (*) на фазовой диаграмме называется кривой равновесия фаз. Следовательно, критерий равновесия фаз – равенство их химических потенциалов. Чтобы получить уравнение этой кривой на диаграмме 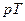 , продифференцируем (*):
, продифференцируем (*):
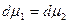
или с учетом выражения для 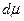 :
:
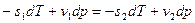
откуда следует уравнение:
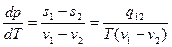 , определяющее кривую равновесия фаз (уравнение Клайперона - Клаузиуса).
, определяющее кривую равновесия фаз (уравнение Клайперона - Клаузиуса).
Здесь 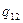 – количество теплоты, в расчете на одну молекулу. Так как
– количество теплоты, в расчете на одну молекулу. Так как 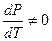 или
или 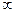 , то
, то 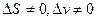 . Это значит, что первые производные (
. Это значит, что первые производные (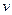 и
и 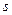 ) при переходе через кривую (т.н. фазовом переходе) претерпевают скачок. Такой переход называется фазовым переходом первого рода.
) при переходе через кривую (т.н. фазовом переходе) претерпевают скачок. Такой переход называется фазовым переходом первого рода.
36. При каком давлении вода будет кипеть при 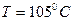 .
.
Решение:
 I способ: Воспользуемся уравнением Клайперона – Клаузиуса.
I способ: Воспользуемся уравнением Клайперона – Клаузиуса. 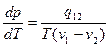 . Поскольку
. Поскольку 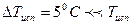 , то можно воспользоваться приближенным соотношением:
, то можно воспользоваться приближенным соотношением: 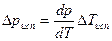 , где
, где 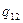 – удельная теплота парообразования (на 1 моль),
– удельная теплота парообразования (на 1 моль), 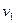 – удельный объем пара,
– удельный объем пара, 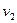 – воды (
– воды (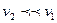 ). Поэтому
). Поэтому
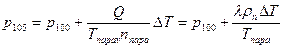 , где
, где 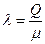 - удельная (на единицу массы) теплота парообразования,
- удельная (на единицу массы) теплота парообразования, 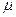 - молярная масса.
- молярная масса.
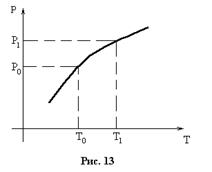
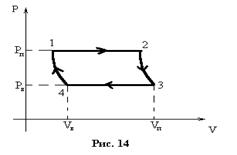 II способ: Рассмотрим цикл Карно для одного моля воды, который испаряется при
II способ: Рассмотрим цикл Карно для одного моля воды, который испаряется при 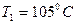 (и соответствующем давлении
(и соответствующем давлении 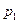 ) и конденсируется при
) и конденсируется при 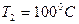 (и давлении
(и давлении 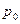 ). При испарении и конденсации
). При испарении и конденсации 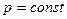 и
и 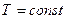 , поэтому изотермы будут одновременно и изобарами. КПД цикла Карно будет равен:
, поэтому изотермы будут одновременно и изобарами. КПД цикла Карно будет равен: 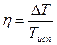 . С другой стороны
. С другой стороны 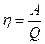 .
.
Но 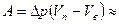 {площадь фигуры}
{площадь фигуры} 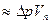 ,
, 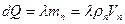 .
.
Приравнивая два выражения 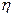 , получаем:
, получаем: 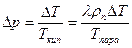 . Численное значение
. Численное значение 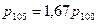 .
.
37. Определить, насколько изменится температура воды, если ее течением переносит на глубину 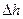 .
.
Решение: Будем считать, что слои воды не обмениваются теплом, т.е. 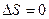 для каждого слоя. Изменение температуры при этом можно определить из соотношения:
для каждого слоя. Изменение температуры при этом можно определить из соотношения: 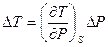 .
.
Из задачи 15 следует, что 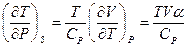 , (
, (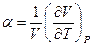 - коэффициент теплового расширения).
- коэффициент теплового расширения).
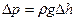 .
.
Поэтому 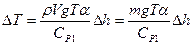 , где
, где 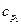 – теплоемкость одного моля воды,
– теплоемкость одного моля воды, 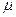 - молярная масса. Если
- молярная масса. Если 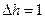 км,
км, 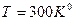 , то
, то 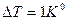 .
.
38. Один моль воды охлаждается от температуры 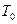 до
до 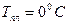 и замерзает. При этом тепло отводится к другому молю воды с той же начальной температурой
и замерзает. При этом тепло отводится к другому молю воды с той же начальной температурой 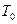 с максимальной эффективностью (так, что суммарная энтропия не изменяется). Какое количество воды при этом испарится? Какую работу производит при этом рефрижератор?
с максимальной эффективностью (так, что суммарная энтропия не изменяется). Какое количество воды при этом испарится? Какую работу производит при этом рефрижератор?
Решение: Процессы испарения и конденсации идут при постоянном давлении. При нагревании и охлаждении:
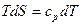 ,
,
следовательно
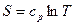 .
.
Изменения энтропии при испарении и конденсации, соответственно равны 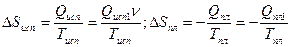 ,
,
где 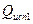 и
и 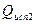 – количества теплоты на 1 моль,
– количества теплоты на 1 моль, 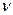 - количество молей. Суммарная энтропия по условию равна нулю. Следовательно
- количество молей. Суммарная энтропия по условию равна нулю. Следовательно
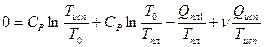 ,
,
откуда можно найти 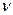 . Работа рефрижератора есть разность количества тепла, отданного для нагревания:
. Работа рефрижератора есть разность количества тепла, отданного для нагревания:
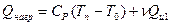
и полученного при охлаждении другого моля (и замораживании его) 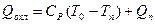 ;
;
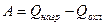 .
.
39. Поршень с малой теплоемкостью скользит без трения внутри изолированного цилиндра. Объемы 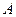 и
и 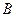 наполнены одинаковым количеством идеального одноатомного газа. Начальная температура газа
наполнены одинаковым количеством идеального одноатомного газа. Начальная температура газа 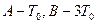 . Каково отношение объемов в начальный момент и после установления термодинамического равновесия? Как изменится энтропия одного моля? Какую полезную работу может совершить система при условии, что передача тепла от одного объема к другому обратима?
. Каково отношение объемов в начальный момент и после установления термодинамического равновесия? Как изменится энтропия одного моля? Какую полезную работу может совершить система при условии, что передача тепла от одного объема к другому обратима?
Решение:
Т.к. все время 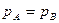 , то
, то 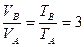 в начальный момент. Т.к.
в начальный момент. Т.к. 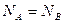 и система теплоизолирована, то после установления термодинамического равновесия.
и система теплоизолирована, то после установления термодинамического равновесия. 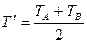 ={усредненная кинетическая энергия}
={усредненная кинетическая энергия} 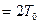 и
и 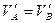 .
.
Изменение энтропии 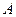 и
и 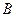 при постоянном давлении (
при постоянном давлении (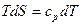 ):
):
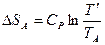 ,
, 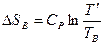 .
.
Подставляя 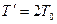 ,
, 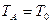 ,
, 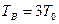 ,
, 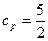 получим
получим 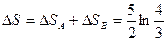 .
.
Если бы передача тепла происходила обратимо (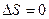 ), то в соответствии с первым началом термодинамики конечную температуру можно было бы определить из соотношения:
), то в соответствии с первым началом термодинамики конечную температуру можно было бы определить из соотношения:
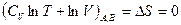
или
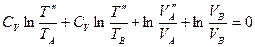 ,
, 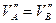 .
.
Положим 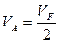 ,
, 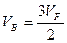 ,
, 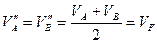 .
.
Тогда
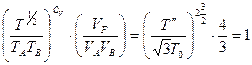 (
(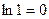 ).
).
Следовательно 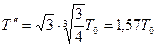 .
.
Работа, в силу теплоизолированности системы есть разность внутренних энергий в начале и конце процесса: 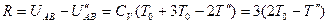 .
.
40. Выразить изменение температуры, энтропии и энтальпии через начальный и конечный объем.
Решение:
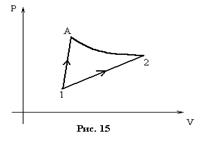
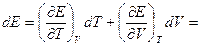 {см. задачу 2} =
{см. задачу 2} =
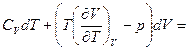 {см. задачу 2 для ВДВ газа} =
{см. задачу 2 для ВДВ газа} = 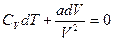 (по условию). Отсюда
(по условию). Отсюда
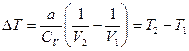 (*)
(*)
Т.к. энтропия – функция состояния, то 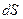 – полный дифференциал и, следовательно,
– полный дифференциал и, следовательно, 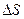 не зависит от пути. Пройдем его через точку
не зависит от пути. Пройдем его через точку 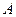 (по изохоре и затем по изобаре). Тогда ((см. задачу 2)
(по изохоре и затем по изобаре). Тогда ((см. задачу 2) 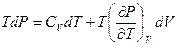 ).
).
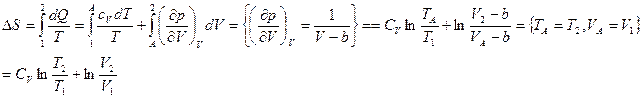
(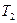 выражается через
выражается через 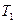 по (*)).
по (*)).
Энтальпия 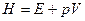 , но т.к.
, но т.к. 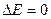 , то
, то 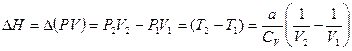 .
.
41. Вода проливается через пористую перегородку (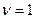 ) под давлением
) под давлением 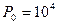 атм в большой сосуд с давлением
атм в большой сосуд с давлением 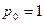 атм. Температура воды
атм. Температура воды 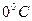 , теплота испарения
, теплота испарения 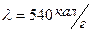 , плотность воды постоянна. Какая часть воды испарится?
, плотность воды постоянна. Какая часть воды испарится?
Решение: Указанный процесс является дросселированием, при котором сохраняется энтальпия (см. задачу 32). Начальная энтальпия воды:
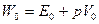 , где
, где 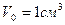 .
.
Энтальпия после продавливания:
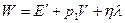 , где
, где 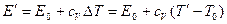 ,
, 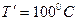 ,
, 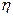 - часть воды, перешедшая в пар. По условию
- часть воды, перешедшая в пар. По условию 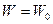 . Следовательно
. Следовательно
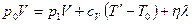 ,
,
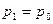 . Поэтому
. Поэтому
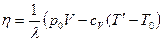 . Численное значение для
. Численное значение для 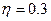 (при данных задачи). Следовательно,
(при данных задачи). Следовательно, 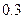 воды переходит в пар.
воды переходит в пар.
42. Колба наполнена газообразным гелием при температуре 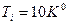 (выше критической точки) и теплоизолирована. Газ может медленно вытекать через капиллярную трубку до тех пор пока давление в колбе не станет равным
(выше критической точки) и теплоизолирована. Газ может медленно вытекать через капиллярную трубку до тех пор пока давление в колбе не станет равным 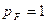 атм, а температура
атм, а температура 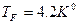 (точка кипения гелия). Считая газ идеальным, найти начальное давление газа в колбе
(точка кипения гелия). Считая газ идеальным, найти начальное давление газа в колбе 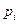 , если в конце процесса колба оказывается полностью наполненной жидким гелием. Удельная теплота испарения гелия
, если в конце процесса колба оказывается полностью наполненной жидким гелием. Удельная теплота испарения гелия 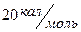 , для газообразного гелия
, для газообразного гелия 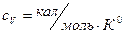 .
.
Решение: Т.к. система теплоизолирована, то 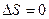 . Это изменение энтропии складывается из двух частей – первая -
. Это изменение энтропии складывается из двух частей – первая - 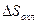 – при охлаждении, вторая - при сжижении
– при охлаждении, вторая - при сжижении 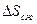 . Из первого начала термодинамики для газа:
. Из первого начала термодинамики для газа:
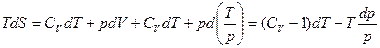 ,
,
откуда
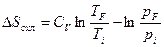 (1).
(1).
В процессе сжижения температура постоянна и равна 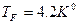 . Следовательно
. Следовательно 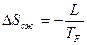 (2).
(2).
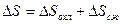 (3).
(3).
Подставляя (1) и (2) в(3), находим потенцированием: 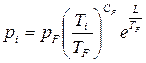 . Численное значение равно
. Численное значение равно 
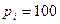 атм.
атм.
43. Шарообразный спутник радиусом 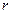 , окрашенный в черный цвет, вращается по круговой орбите вокруг солнца. Температура солнца
, окрашенный в черный цвет, вращается по круговой орбите вокруг солнца. Температура солнца 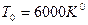 . Угол, под которым солнце видно со спутника,
. Угол, под которым солнце видно со спутника, 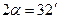 . Какова равновесная температура спутника?
. Какова равновесная температура спутника?
Решение: Плотность энергии 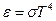 (см. задачу 2 для черного излучения в полости). Поток энергии через отверстие в стенке полости с черным излучением
(см. задачу 2 для черного излучения в полости). Поток энергии через отверстие в стенке полости с черным излучением 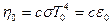 (фотоны движутся со скоростью света). В равновесии энергия, получаемая спутником в единицу времени равна излучаемой за то же время. Энергия, излучаемая солнцем в единицу времени равна
(фотоны движутся со скоростью света). В равновесии энергия, получаемая спутником в единицу времени равна излучаемой за то же время. Энергия, излучаемая солнцем в единицу времени равна 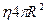 (
(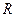 – радиус солнца). Следовательно, энергия, получаемая спутником в единицу времени:
– радиус солнца). Следовательно, энергия, получаемая спутником в единицу времени: 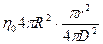 (
(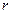 – радиус спутника,
– радиус спутника, 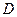 – расстояние от солнца до спутника). Энергия, излучаемая спутником
– расстояние от солнца до спутника). Энергия, излучаемая спутником 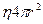 . Приравнивая эти величины, находим:
. Приравнивая эти величины, находим:
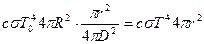 .Вводя обозначение
.Вводя обозначение 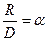 - угловой размер, получаем
- угловой размер, получаем 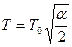 .
.
44. Свободная энергия ферромагнетика в отсутствие внешнего поля 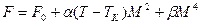 (при
(при 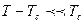 , где
, где 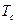 -температура Кюри),
-температура Кюри), 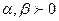 и не зависят от температуры,
и не зависят от температуры, 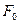 - свободная энергия в ненамагниченном состоянии. Найти равновесную намагниченность и температурную зависимость восприимчивости выше точки Кюри.
- свободная энергия в ненамагниченном состоянии. Найти равновесную намагниченность и температурную зависимость восприимчивости выше точки Кюри.
Решение: 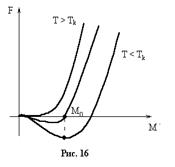 В состоянии равновесия
В состоянии равновесия 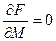 , отсюда
, отсюда 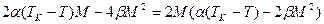 , (1)
, (1)
отсюда 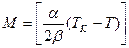 при
при 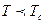 Если же
Если же 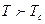 , то левая часть (1) отрицательна и тогда у него есть лишь один корень
, то левая часть (1) отрицательна и тогда у него есть лишь один корень 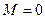 . Схематически зависимость F(M) изображена на рис. 16. Если отключить магнитное поле, то к
. Схематически зависимость F(M) изображена на рис. 16. Если отключить магнитное поле, то к 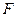 добавиться работа по намагничиванию внешним полем
добавиться работа по намагничиванию внешним полем 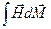 . Отсюда значение поля в зависимости от
. Отсюда значение поля в зависимости от 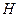 :
:
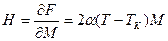 .
.
Восприимчивость при 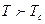
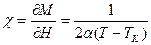 .
.
45. Рассмотреть термодинамику сверхпроводников.
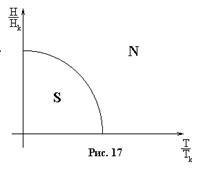 Решение: Экспериментально удалось получить зависимость критического поля от температуры – кривую, отделяющую нормальную область от сверхпроводящей:
Решение: Экспериментально удалось получить зависимость критического поля от температуры – кривую, отделяющую нормальную область от сверхпроводящей: 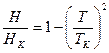
1. 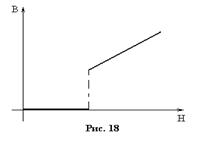 В сверхпроводящей фазе всегда
В сверхпроводящей фазе всегда 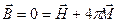 . Это значит, что сверхпроводник является диамагнетиком с
. Это значит, что сверхпроводник является диамагнетиком с 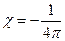 .
.
В свободной энергии 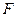 необходимо учесть зависимость как от температуры так и от величины намагниченности
необходимо учесть зависимость как от температуры так и от величины намагниченности
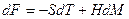
Такой термодинамический потенциал минимален при заданных 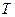 и
и 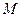 . Однако экспериментально контролировать изменение
. Однако экспериментально контролировать изменение 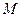 трудно, гораздо легче это делать для внешнего поля
трудно, гораздо легче это делать для внешнего поля 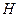 . Введем термодинамический потенциал, который минимален при заданных
. Введем термодинамический потенциал, который минимален при заданных 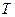 и
и 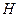 .
.
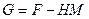 .
.
Тогда 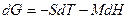
При изменении магнитного поля на величину 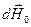 источники поля совершают работу над единицей объема
источники поля совершают работу над единицей объема
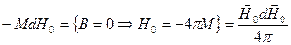 .
.
Следовательно, при изменении поля то 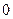 до
до 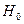 источник поля совершает работу
источник поля совершает работу 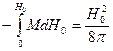 .
.
Эта работа будет запасена в свободной энергии сверхпроводника
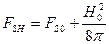 .
.
В точке перехода 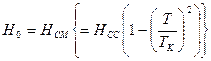 , а
, а 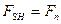 – плотности свободной энергии нормального металла.
– плотности свободной энергии нормального металла.
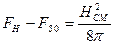 (1)
(1)
и, следовательно
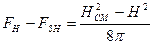 (2)
(2)
(то же для 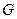 )(при фазовом переходе непрерывны как
)(при фазовом переходе непрерывны как 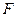 так и
так и 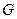 ).
).
Последняя формула показывает, что при данной температуре и 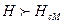
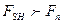 и энергетически выгодно нормальное состояние, а при
и энергетически выгодно нормальное состояние, а при 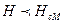 – сверхпроводящее (
– сверхпроводящее (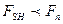 ). При
). При 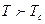
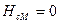 и нормальное состояние будет при любом поле. Поскольку
и нормальное состояние будет при любом поле. Поскольку 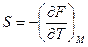 , то
, то
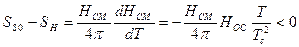
Следовательно, сверхпроводящее состояние более упорядочено (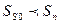 ). При
). При 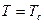
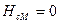 и
и 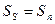 . Это значит, что при переходе при
. Это значит, что при переходе при 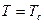 не выделяется теплоты (фазовый переход 2-го рода). При
не выделяется теплоты (фазовый переход 2-го рода). При 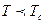
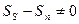 и при таком переходе выделяется теплота (фазовый переход 1-го рода). Найдем эту теплоту. При переходе из сверхпроводящей фазы в нормальную
и при таком переходе выделяется теплота (фазовый переход 1-го рода). Найдем эту теплоту. При переходе из сверхпроводящей фазы в нормальную 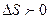 (
(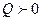 )– теплота поглощается и наоборот - при обратном переходе теплота выделяется. В силу непрерывности
)– теплота поглощается и наоборот - при обратном переходе теплота выделяется. В силу непрерывности 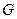 вдоль границы сверхпроводник - нормальный металл в состоянии равновесия
вдоль границы сверхпроводник - нормальный металл в состоянии равновесия
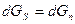
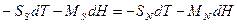 .
.
Отсюда получаем вышеуказанную кривую фазового равновесия:
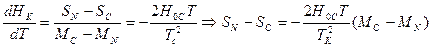
Но 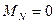 , а
, а 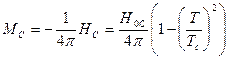 ,
,
поэтому теплота, выделяющаяся при 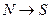 переходе:
переходе:
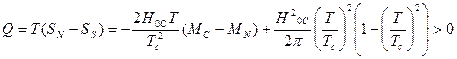 (равно нулю если
(равно нулю если 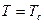 ).
).
Наконец, теплоемкость изменяется скачком при любой температуре:
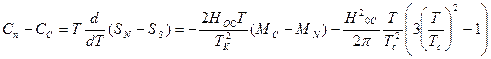 .
.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 488; Нарушение авторских прав?; Мы поможем в написании вашей работы!