
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Решение. Повышение температуры кипения раствора равно
|
|
|
|
Решение.
Решение.
Повышение температуры кипения раствора равно
Δt = 46,529 – 46,3 = 0,229о.
Молярная масса бензойной кислоты равна 122 г/моль.
Из формулы (1) находим эбуллиоскопическую константу
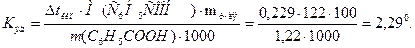
Пример 3. Раствор, содержащий 11,04 г глицерина в 800 г воды, кристаллизуется при – 0,28о С. Вычислить молярную массу глицерина.
Температура кристаллизации чистой воды 0оС, следовательно, понижение температуры кристаллизации раствора равно:
Δtзам =0 - (-0,279) = 0,279о.
Подставляем в уравнение (1) данные, находим молярную массу глицерина:
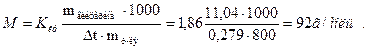
Пример 4. Вычислить массовую долю водного раствора мочевины (NH2)2CO, зная, что температура кристаллизации этого раствора равна – 0,465оС.
Температура кристаллизации чистой воды 0оС, следовательно,
Δtзам =0 – (-0,465) = 0,465о.
Зная, что молярная масса мочевины 60 г/моль, находим массу m (г), растворенного вещества, приходящуюся на 1000 г воды, из формулы:
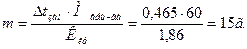
Общая масса раствора, содержащего 15 г мочевины, составляет 1000 + 15 = 1015 г.
Массовую долю мочевины в данном растворе находим из соотношения
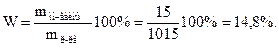
Контрольные задания
241. Чему равно давление насыщенного пара над 10%-ным раствором карбамида CO(NH2)2 при 1000С? Ответ: 98 кПа.
242. Раствор, содержащий 0,512 г неэлектролита в 100 г бензола, кристаллизуется при 5,3оС. Температура кристаллизации бензола 5,5оС. Криоскопическая константа 5,10. Вычислите молярную массу растворенного вещества. Ответ:130,56 г/моль.
243. Вычислите массовую долю водного раствора сахара С12Н22О11, зная, что температура кристаллизации раствора – 0,93оС. Криоскопическая константа воды 1,860. Ответ: 14,5%.
244. Вычислите температуру кристаллизации раствора мочевины (NH2)2CO, содержащего 5 г мочевины в 150 г воды. Криоскопическая константа воды 1,860. Ответ: -1 оС.
245. Раствор, содержащий 3,04 г камфоры С10Н16О в 100г бензола, кипит при 80,714оС. Температура кипения бензола 80,2оС. Вычислите эбуллиоскопическую константу бензола. Ответ: 2,56о.
246. При 1000С давление насыщенного пара 18%-ного водного раствора неэлектролита равно 98,84 кПа. Вычислите молярную массу неэлектролита и назовите его. Ответ: 180 г/моль; глюкоза.
247. Вычислите массовую долю водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,39оС. Эбуллиоскопическая константа воды 0,520. Ответ: 6,45%.
248. Вычислите молярную массу неэлектролита, зная, что раствор, содержащий 2,25 г этого вещества в 250 г воды, кристаллизуется при – 0,279оС. Криоскопическая константа воды 1,860.
Ответ: 60,00 г/моль.
249. Вычислите температуру кипения 5%-го раствора нафталина С10Н8 в бензоле. Температура кипения бензола 80,2оС. Эбуллиоскопическая константа его 2,570. Ответ: 81,25оС.
250. Вычислите осмотическое давление раствора при 220С, в 1,2л которого содержится 20,5 мг сахара (С12Н22О11). Ответ: 122 Па.
251. Раствор, содержащий 25,65 г некоторого неэлектролита в 300 г воды, кристаллизуется при – 0,465оС. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,860. Ответ: 342 г/моль.
252. Вычислите криоскопическую константу уксусной кислоты, зная, что раствор, содержащий 3,0 г антрацена С14Н10 в 100 г уксусной кислоты, кристаллизуется при 15,718оС. Температура кристаллизации уксусной кислоты 16,65оС. Ответ: 3,90.
253. Равные весовые количества камфоры С10Н16О и нафталина С10Н8 растворены в одинаковых количествах бензола. Какой из растворов кипит при более высокой температуре? Ответ: раствор С10Н8.
254. Сколько граммов глюкозы С6Н12О6 должно находиться в 0,5 л раствора, чтобы его осмотическое давление (при той же температуре) было таким же, как раствора, в 1 л которого содержится 9,2 г глицерина С3Н5(ОН)3? Ответ: 9 г.
255. Температура кристаллизации раствора, содержащего 66,3г некоторого неэлектролита в 500г воды, равна –0,558оС. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,86о. Ответ: 442 г/моль.
256. При какой приблизительно температуре будет кристаллизоваться 40%-ный раствор этилового спирта С2Н5ОН? Криоскопическая константа воды 1,86о. Ответ: -27оС.
257. Сколько граммов сахарозы С12Н22О11 надо растворить в 100 г воды, чтобы: а) понизить температуру кристаллизации на 1˚С; б) повысить температуру кипения на 1˚С? Ответ: а) 18,4 г; б) 65,8 г.
258. В 100 г Н2О содержится 4,57 г сахарозы С12Н22О11. Найдите: а) температуру кристаллизации раствора; б) температуру кипения раствора. Ответ: а) -0,25˚С; б) 100,07˚С.
259. Чему равна молярная масса растворенного в 500 г бензола неэлектролита массой 76,1 г, если температура кристаллизации понизилась с 5,4 до 0,3˚С? Криоскопическая константа бензола 5,1˚.
Ответ: 152,2 г/моль.
260. Вычислите массовую долю водного раствора глюкозы С6Н12О6, зная, что этот раствор кипит при 100,26оС. Эбуллиоскопическая константа воды 0,52о. Ответ: 9%.
261. Какое вещество – камфору С10Н16О или нафталин С10Н8 – растворили в бензоле, если внесение 39 г этого вещества в 1000 г бензола привело к снижению температуры кристаллизации на 1,3˚С? Криоскопическая константа бензола 5,1˚. Ответ: камфора.
262. Сколько граммов мочевины (NH2)2CO следует растворить в 250 г воды, чтобы температура кипения повысилась на 0,26о? Эбуллиоскопическая константа воды 0,52о. Ответ: 7,5 г.
263. В каком отношении должны находиться массы воды и этилового спирта С2Н5ОН, чтобы получить раствор, кристаллизирующийся при -20˚С? Криоскопическая константа воды 1,86˚. Ответ: 2:1.
264. При растворении 5,0 г вещества в 200 г воды получается не проводящий тока раствор, кристаллизующийся при -1,45˚С. Определите молярную массу растворенного вещества. Криоскопическая константа воды 1,86˚. Ответ: 32 г/моль.
265. Сколько граммов фенола С6Н5ОН следует растворить в 125 г бензола, чтобы температура кристаллизации раствора была ниже температуры кристаллизации бензола на 1,70? Криоскопическая константа бензола 5,10. Ответ: 3,91 г.
266. При растворении 2,3 г некоторого неэлектролита в 125 г воды температура кристаллизации понижается на 0,3720. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,860. Ответ: 92 г/моль.
267. Вычислите температуру кипения 15%-ного водного раствора пропилового спирта С3Н7ОН, зная, что эбуллиоскопическая константа воды 0,520. Ответ: 101,52оС.
268. На сколько градусов повысится температура кипения воды, если в 100 г воды растворить 9 г глюкозы С6Н12О6? Эбуллиоскопическая константа воды 0,52о. Ответ: на 0,26оС.
269. При какой приблизительно температуре будет кипеть 50%-ный раствор сахарозы С12Н22О11? Эбуллиоскопическая константа воды 0,52о. Ответ: 101,50С.
270. Вычислите массовую долю водного раствора метанола СН3ОН, температура кристаллизации которого –2,790С. Криоскопическая константа воды 1,860. Ответ: 4,58%.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 7792; Нарушение авторских прав?; Мы поможем в написании вашей работы!