
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Комплексні сполуки. 3 страница
|
|
|
|
A. * Hg2+
B. K+
C. I–
D. HgI42–
E. K2[HgI4]
158. Вкажить продукт окиснення тіосульфату натрію йодом:
A. *Na2S4O6
B. S + Na2SO4
C. H2SO4 + Na2SO4
D. S + H2SO4
E. H2SO4
159. Вкажить сполуки,які містять пероксидну групу: H2SO3, Na2S2O3, H2SO5, Na2S4O6, K2Cr2O7
A. * H2SO5
B. H2SO3
C. Na2S4O6
D. K2Cr2O7
E. Na2S2O3
160. Серед наведених сполук вкажить метасіль: Na3AlO3, Na4SiO4, K4P2O7, Na2SiO3, K4PbO4
A. * Na2SiO3
B. Na4SiO4
C. Na3AlO3
D. K4P2O7
E. K4PbO4
161. Вкажіть тип реакції,який використовують для якісного визначення катіону Fe3+:
A. *комплексоутворення
B. осаждення
C. гідролізу
D. окислення-відновлення
E. нейтралізації
162. Вкажіть сполуку, якісне визначення кякої супроводжується появою синього забарвлення ефірного шару:
A. *H2O2
B. Cl2
C. Na2HPO4
D. MnSO4
E. FeSO4
163. Вкажіть, чим визначається геометрична структура комплексної сполуки:
A. * типом гібридизації орбіталей комплексоутворювача
B. зарядом комплексоутворювача
C. кількістю лігандів
D. зарядом внутрішньої сфери комплекса
E. координаційним числом комплексоутворювача
164. Одним з показників якості води є її твердість. Яка з наведених солей може зумовлювати постійну твердість води?
A. *СаSO4
B. NaCl
C. Ca(HCO3)2
D. Mg(HCO3)2
E. K2SO4
165. Для кількісного визначення багатьох лікарських засобів використовують неводні розчини перхлоратної кислоти. Який з наведених оксидів є ангідридом цієї кислоти?
A. *Cl2O7
B. Cl2O
C. ClO2
D. Cl2O3
E. Cl2O6
166. Цианокобаламін (вітамін В12) є комплексною сполукою кобальту. До якого типу комплексних сполук вона він належить?
A. *Хелатних комплексів
B. Ацідокомплексів
C. Аквакомплексів
D. Катіонних комплексів
E. Ценів
167. З якою з наведених речовин розведена азотна кислота реагує без утворення газуватих продуктів реакції?
A. *Mg
B. Cu
C. P
D. Pb
E. S
168. Яка з летких водневих сполук елементів VA групи періодичної системи є найбільш стійкою?
A. *NH3
B. PH3
C. AsH3
D. SbH3
E. BiH3
169. Ступінь окиснення фосфору в гіпофосфітній кислоті дорівнює:
A. *+1
B. –3
C. +3
D. +4
E. +5
170. У якій з наведених сполук ступінь окиснення азоту дорівнює –2?
A. *N2H4
B. NH3
C. NH4Cl
D. NH2OH
E. HCN
171. Вода з високою твердістю непридатна для використання у фармацевтичній промисловості. Які з наведених речовин можна використати з цією метою?
A. *Na2CO3, NaOH
B. CaCO3, Ca(OH)2
C. Na3PO4, CaCl2
D. MgSO4, H2SO4
E. Na2CO3, NaCl
172. Бінарні сполуки, в яких ступінь окиснення Оксигену дорівнює – ½, називають:
A. * надпероксидами
B. Пероксидами
C. Озонідами
D. Оксидами
E. Оксидами – дипероксидами
173. Реакція термічного розкладу:2NaNO3 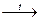
 2NaNO2+O2 належить до окисно-відновних реакцій типу:
2NaNO2+O2 належить до окисно-відновних реакцій типу:
A. * Внутрішньомолекулярних
B. Міжмолекулярних
C. Диспропорціювання
D. Самоокислення – самовідновлення
174. Яка із сполук характеризується найнижчим ступенем окиснення Нітрогену?
A. * NH3
B. NH2NH2
C. HNO3
D. NH2OH
E. NO2
175. В якій із сполук Оксиген проявляє позитивний ступінь окиснення?
A. * OF2
B. CO2
C. H2O2
D. KO2
E. KO3
176. Комплексна сполука складу Na3[Ag(S2O3)2] належить до:
A. * Ацидокомплексів
B. Аквакомплексів
C. Аміакатів
D. Гідроксокомплексів
E. Халатів
177. Заряд центрального іону-комплексоутворювача в червоній кров’яній солі К3[Fe(CN)6] дорівнює:
A. * +3
B. +2
C. +1
D. +4
E. +6
178. Комплексні сполуки [Co(NH3)5Br]SO4 і [Co(NH3)5SO4]Br являються ізомерами:
A. * Іонізаційними
B. Координаційними
C. Гідратними
D. Геометричними
E. Оптичними
179. Склад харчової соди виражається формулою:
A. * NaHCO3
B. Na2CO3
C. K2CO3
D. Na2CO3 · 10H2O
E. CaCO3
180. Яким із зазначених реактивів слід скористатись, щоб визначити наявність у розчині катіону Ca2+?
A. * (NH4)2C2O4
B. HCl
C. HNO3
D. KCl
E. NaBr
181. Гідроксид міді (ІІ) утворює з лугами комплексні сполуки, в яких мідь проявляє координаційне число:
A. * 4
B. 5
C. 6
D. 3
E. 2
182. Гідроксид заліза(ІІІ) проявляє амфотерні властивості тому що:
A. * реагує з кислотами і основами
B. реагує тільки з кислотами
C. реагує тільки з основами
D. диспропорціонує
E. розкладається при нагріванні
183. Серед елементів ІІВ групи амфотерні властивості проявляють:
A. * тільки цинк
B. цинк і кадмій
C. кадмій і ртуть
D. всі елементи
E. тільки ртуть
184. Серед гідроксидів підгрупи галію амфотерними властивостями володіють:
A. * гідроксиди індію і галію
B. тільки гідроксид індію
C. тільки гідроксид галію
D. тільки гідроксид талію
E. гідроксиди елементів усієї підгрупи
185. Із елементів підгрупи германію з водними розчинами лугів при відсутності окислювачів реагують:
A. * олово і свинець
B. тільки олово
C. тільки свинець
D. тільки германій
E. елементи всієї підгрупи
186. Із елементів підгрупи хрому з розплавами лугів в присутності окислювачів взаємодіють:
A. * молібден і вольфрам
B. тільки молібден
C. тільки вольфрам
D. хром і молібден
E. елементи всієї підгрупи
187. Молібдати і вольфрамати можна отримати:
A. * окисленням відповідних металів, в розплавах соди чи поташу
B. окисленням цих металів в кислому середовищі
C. гідролізом їх солей
D. диспропорціонуванням солей цих металів
E. за реакціями обміну
188 При взаємодії з киснем пероксиди утворюють елементи:
A. * тільки натрій
B. тільки калій
C. натрій і калій
D. тільки літій
E. всі лужні метали
189 Із елементів ІІА групи амфотерні властивості проявляють:
A. * тільки берилій
B. берилій і магній
C. тільки магній
D. тільки кальцій
E. всі лужно-земельні метали
190 Тетрафторборна кислота може утворюватися:
A. * при взаємодії трифториду бора з водою, або при взаємодії бору з сумішшю концентрованих азотної і фтороводневої кислот
B. взаємодією гідроксиду бору(ІІІ) з фтороводневою кислотою
C. взаємодією бору з фтороводневою кислотою
D. гідролізом солей борної кислоти
E. лише при взаємодії фторид бору(ІІІ) з водою
191 Жовта кров’яна сіль є реактивом на:
A. * іони Fe3+
B. іони Fe2+
C. іони Ca2+
D. іони FeO42—
E. іони FeO2—
192 Червона кров’яна сіль є реактивом на:
A. * іони Fe2+
B. іони Fe3+
C. іони Ca2+
D. іони FeO42—
E. іони FeO2—
193 Гідроксиди платинових металів(IV) проявляють амфотерні властивості тому що:
A. * реагують з кислотами і основами
B. реагують тільки з основами
C. реагують тільки з кислотами
D. проявляють окислювально-відновні властивості
E. розкладаються при нагріванні
194. Для марганцю найбільш типовим координаційним числом є:
A. * 6,4
B. 5,6
C. 4,3
D. 2,5
E. 6,7
195. Сила кисневмісних кислот хлору зростає від хлорноватистої до хлорної кислоти тому що:
A. * полярність зв’язку водень-кисень збільшується
B. полярність зв’язку водень-кисень зменшується
C. полярність зв’язку водень-кисень не змінюється
D. збільшується стійкість кислот
E. зменшується їх окислювальна здатність
196. В результаті реакцій міді з концентрованою азотною кислотою виділяється:
A. * NO2
B. NO
C. N2O
D. N2
E. NH3
197. Який із наведених оксидів є ангідридом нітритної кислоти?
A. * N2O3
B. N2O5
C. N2O4
D. NO
E. NO2
198. Який із наведених металів не реагує з концентрованою азотною кислотою?
A. * Al
B. Cu
C. Mg
D. K
E. Ba
199. Який із наведених металів не реагує з розведеною сульфатною кислотою?
A. * Cu
B. Fe
C. Zn
D. Al
E. Mn
200. Який з наведених металів не реагує з хлоридною кислотою?
A. * Ag
B. Zn
C. Ca
D. Al
E. Fe
201. Найбільш сильною серед галогеноводневих кислот є:
A. * йодоводнева кислота
B. фтороводнева кислота
C. соляна кислота
D. бромоводнева кислота
E. плавікова кислота
202. Найбільш сильною серед кисневмісних кислот є:
A. * перхлоратна кислота
B. хлоритна кислота
C. гіпохлоритна кислота
D. хлоратна кислота
E. Хлорноватиста кислота
203. Найбільш сильним окисником серед кисневмісних кислот хлору є:
A. * гіпохлоритна кислота
B. перхлоратна кислота
C. хлоратна кислота
D. хлоритна кислота
E. хлорна кислота
204. Купрум (ІІ) гідроксид утворює з лугами комплексні сполуки, в яких купрум проявляє координаційне число:
A. * 4
B. 5
C. 6
D. 3
E. 2
205. Ферум (ІІІ) гідроксид проявляє амфотерні властивості тому що:
A. * реагує з кислотами і основами
B. реагує тільки з кислотами
C. реагує тільки з основами
D. диспропорціонує
E. розкладається при нагріванні
206. Серед елементів ІІВ групи амфотерні властивості проявляють:
A. * тільки цинк
B. цинк і кадмій
C. кадмій і ртуть
D. всі елементи
E. тільки ртуть
207. Із елементів підгрупи германію з водними розчинами лугів при відсутності окиснювачів реагують:
A. * олово і свинець
B. тільки олово
C. тільки свинець
D. тільки германій
E. елементи всієї підгрупи
208. При взаємодії з киснем пероксиди утворюють:
A. *натрій
B. натрій і калій
C. калій
D. літій
E. всі лужні метали
209. Із елементів ІІА групи амфотерні властивості проявляють:
A. *берилій
B. берилій і магній
C. магній
D. кальцій
E. всі елементи ІІА групи
210. Жовта кров’яна сіль K4[Fe(CN)6] є реактивом на:
A. * іони Fe3+
B. іони Fe2+
C. іони Ca2+
D. іони FeO42-
E. іони FeO2-
211. Червона кров’яна сіль K3[Fe(CN)6] є реактивом на:
A. * іони Fe2+
B. іони Fe3+
C. іони Ca2+
D. іони FeO42-
E. іони FeO2-
212. У результаті реакцій міді з концентрованою нітратною кислотою виділяється:
A. * NO2
B. NO
C. N2O
D. N2
E. NH3
213. Який із наведених металів витісняє із хлоридної кислоти водень?
A. * Алюміній
B. Мідь
C. Ртуть
D. Золото
E. Платина
214. Олеумом називають:
A. * Розчин SO3 у сульфатній кислоті
B. Розчин SO2 у сульфатній кислоті
C. Продукт взаємодії SO3 i H2O
D. Розчин сірководню у сульфатній кислоті
E. Розчин сірки у сульфатній кислоті
215. Натрій гідрогенкарбонат застосовують як:
A. * Антацидний засіб
B. Сечогінний засіб
C. Проносний засіб
D. Жовчогінний засіб
E. Заспокійливий засіб
216. Який метал не окиснюється на повітрі, навіть при прожарюванні:
A. * Золото
B. Натрій
C. Цинк
D. Кальцій
E. Барій
217. Яке з наведених тверджень є правильним для силікатної кислоти:
A. * Не проявляє окиснювально-відновних властивостей
B. Добре розчиняється у воді
C. Не витісняє СО2 з розчину карбонатів
D. Є сильною кислотою
E. Отримується розчиненням SіО2 у воді
218. Натрій йодид застосовують у медицині як:
A. * Джерело мікроелементу йоду
B. Плазмозамінник
C. Заспокійливий засіб
D. Антацидний засіб
E. Сечогінний засіб
219. Із карбонатів стійкими до нагрівання є
A. * Натрій карбонат
B. Аргентум карбонат
C. Кальцій карбонат
D. Магній карбонат
E. Купрум (ІІ) карбонат
220. При опіках рекомендують обробляти поверхню рани розчином перманаганату калію з масовою часткою
A. * 2,5-4%
B. 0,1 %
C. 0,1 – 0,5%
D. 0,01 – 0,1%
E. 0,01 %
221. В основі травлення скла лежить реакція взаємодії фторидної кислоти з:
A. * SiO2
B. Si
C. SiO
D. H2SiO3
E. SiF4
222. При потраплянні залізних ошурок в сильно нагріту концентровану сірчану кислоту можливий наступний процесс:
A. 2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2 + 6H2O
B. Fe + H2SO4 = FeSO4 + H2
C. Fe + 2H2SO4 = FeSO4 + SO2 + 2H2O
D. Зализо пасивується концентрованою сірчаною кислотою, тому реакція не відбувається
E. Fe + 3H2SO4 = Fe2(SO4)3 + 3H2
223. Які дві речовини вступили в реакцію, якщо в результаті утворились наступні продукти (вказані всі речовини без стехіометричних коефіцієнтів): ® Fe2(SO4)3 + SO2 + H2O?
A. FeO и H2SO4 (конц.)
B. Fe2O3 и H2SO4 (конц.)
C. Fe и H2SO4 (разб.)
D. Fe(OH)3 и H2SO4 (розв.)
E. F2O3 + H2SO4 (розв.)
224. Які дві речовини вступили в реакцію, якщо в результаті утворюеться одна речовина – гідроксид заліза (III)
A. Fe(OH)2 и H2O2
B. Fe и O2
C. Fe2O3 и H2O
D. Fe и H2O
E. FeO и H2O
225. Розчин SO3 в 100\%-ой сірчаній кислоті називають.
A. *Олеумом
B. Царскою горілкою
C. Плавиковою кислотою
D. Олеїновою кислотою
E. Кислотою Каро.
226. В присутності каталізатора або під дією опромінювання СО взаемодіє з хлором, утворюючі:
A. отруйний газ фосген
B. Тетрахлорид вуглецю та озон
C. Оксид вуглецю (IV) та чотирихлористий вуглець
D. Оксид вуглецю (IV) та оксид хлору (I)
E. Тетрахлорид вуглецю та оксигену
227. Францій, завершує I групу, та радій, завершує II групу, вони є…
A. Радіоактивними елементами
B. Дуже тверді
C. Найрозповсюдженішими у земній корі серед усіх s-елементів
D. Надійними ізоляторами
E. Напівпровідниками
228. Хром також, як алюміній і залізо,…
A. Пасивується холодними концентрованими H2SO4 и HNO3
B. Здатний утворювати сполуки зі ступенем окиснення +6
C. Утворює оксид зі ступенем окиснення +3 зеленого кольору
D. Утворює типовий кислотний оксид
E. Утворює пероксид
229. Назвіть помилкове твердження, яке відноситься до гідроксиду заліза (III); Fe(OH)3 – це …
A. Дуже сильний електроліт
B. Амфотерний гідроксид, який утворює ферити при сплавленні з лугами
C. Практично нерозчинні у воді речовини
D. Речовина бурого кольору
E. Дуже слабка основа
230. Сучасний процес добування аміаку основан на …
A. Його синтезі з азоту та водню при температури 400-5000С та тиску 250-300 атм. з використанням спеціального каталізатора: N2+H2®2NH3
B. Дією гашеного вапна на хлорид амонію при нагріванні: Ca(OH)2+2NH4CI=CaCI2+2NH3+2H2O
C. Розкладом фосфату амонію при нагріванні: (NH4)3PO4to=H3PO4+3NH3
D. Реакція гідролізу ціанаміду: CaCN2+3H2O=2NH3+CaCO3¯
E. Реакція гідролізу аміду натрію: NaNH2+H2O®NaOH+NH3
231. Газ, який неможливо осушити оксидом фосфору (V) це:
A. Аміак
B. Хлор
C. Сірнистий газ
D. Вуглекислий газ
E. Фтор
232. Однакову валентність у водневій сполуці та у вищому оксиді виявляє елемент:
A. *Карбон
B. Фосфор
C. Селен
D. Бром
E. Аргон
233. Вкажіть реакцію яка неможлива:
A. KCl + Br2 = KBr + Cl2
B. KI + Br2 = KBr + I2
C. NaBr+ Cl2 = NaCl + Br2
D. NaI + Cl2 = NaCl + I2
E. KCl + І2 = KІ + Cl2
234. Для виявлення CO2 у повітрі можна використати:
A. * Водний розчин Ca(OH)2
B. Водний розчин NaOH
C. CaO
D. Fe(OH)2
E. Кристалічний NaOH
235. Хлорне вапно використовують як дезинфікуючий засіб. Йому відповідає формула:
A. *CaOCl2
B. Ca(OCl)2
C. Ca(ClO4)2
D. CaCl2
E. Ca(ClO3)2
236. При відновленні калій перманганату у нейтральному середовищі утворюється сполука мангану:
A. *MnO2
B. К2MnO4
C. MnO
D. MnSO4
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 4297; Нарушение авторских прав?; Мы поможем в написании вашей работы!