
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Порядок проведення роботи. 1. Тема:гідроксильні сполуки і їх похідні
|
|
|
|
ЛАБОРАТОРНА РОБОТА №4
1. Тема: Гідроксильні сполуки і їх похідні. Властивості спиртів і фенолів.
2. Мета: Вивчити властивості етилового спирту і гліцерину. Вивчити властивості фенолів.
3. МАТЕРІАЛИ І ОБЛАДНАННЯ:
3.1 етиловий спирт, гліцерин,
3.2 СuSO4 2 н розчин,
3.3 фенолфталеїн 1 % р, лакмус 1 % р.,
3.4 Na металічний,
3.5 Хромова суміш, Н2SO4 конц.,
3.6 Фенол кр., їдкий натрій (2н розчин), фенолят натрію,
3.7 сульфатна кислота, (2Н розчин), хлорид заліза (0,1Н розчин),
3.8 Бромна вода, Н2SO4 (r = 1,84 г/см3 ), НNO3 (r = 1,4 г/см3 ),
3.9 1% розчин пірокатехіну, резорцину, гідрохінону, пірогалолу;
3.10 Їдкий натр (конц.розчин);
3.11 Велика пробірка, газовідвідна трубка.
4.1 Відношення спиртів до індикатора.
4.1.1 Хід роботи: в пробірку дають 3 краплі води і додають 2 краплі
етанолу. Перевіряємо на фенолфталеїн і лакмус.
4.1.2 Спостереження: забарвлення індикаторів не змінюється
4.1.3 Висновок: спирти – практично нейтральна речовина.
4.2 Утворення і гідроліз алкоголятів.
4.2.1 Хід роботи: в суху пробірку поміщають металічний натрій і додають 3 краплі етилового спирту і закривають пробірку пальцем. По закінченню реакції підносять пробірку до полум’я пальника і забирають палець. В отворі пробірки загоряється водень, який виділяється. Залишок етилату натрію розчиняється в 2-3 краплях дистильованої води і додають 1 краплю фенолфталеїну.
4.2.2 Спостереження: з’являється малинове забарвлення
4.2.3 Хімізм реакцій: С2Н5ОН + Na → C2H5ONa + ½H2 C2H5ONa + H – OH → C2H5OH + NaOH
4.2.4 Висновок: атоми водню гідроксильних груп в спиртах проявляють певну активність. В спиртах слабо виражені кислотні властивості.
4.3 Окислення етилового спирту купрум (ІІ) оксидом.
4.3.1 Хід роботи: в пробірку поміщають 2 краплі етилового спирту. Тримаючи спіраль з мідною дротиною пінцетом нагрівають її в полум’ї пальника до появи чорного нальоту CuO. Гарячу спіраль опускають в пробірку з етиловим спиртом.
4.3.2  Спостереження: чорна поверхня спіралі стає золотистою внаслідок відновлення CuO. Відчуваємо запах оцтового альдегіду (запах яблука). O
Спостереження: чорна поверхня спіралі стає золотистою внаслідок відновлення CuO. Відчуваємо запах оцтового альдегіду (запах яблука). O
4.3.3 Хімізм реакцій: С2Н5ОН + CuO → CH3 – C + Cu + H2O
 H
H
4.3.4 Висновок: окислення С2Н5ОН CuO є якісною реакцією.
4.4 Окислення етилового спирту хромовою сумішшю.
4.4.1 Хід роботи: в суху пробірку поміщають 2 краплі етилового спирту і додають 1 краплю розчину H2SO4 і 2 краплі хромової суміші. Нагрівають.
4.4.2 Спостереження: розчин стає синьо-зеленого кольору, одночасно відчувається запах оцтового альдегіду.
4.4.3  Хімізм реакцій: O
Хімізм реакцій: O
 3С2Н5ОН + K2Cr2O7 + H2SO4 → 3CH3 – C + Cr2(SO4)3 + K2SO4 + 7H2O
3С2Н5ОН + K2Cr2O7 + H2SO4 → 3CH3 – C + Cr2(SO4)3 + K2SO4 + 7H2O
H
4.4.4 Висновок: при окисленні спиртів, в першу чергу окислюється карбон, біля якого знаходиться гідроксильна група.
4.5 Взаємодія гліцерину з купруму (ІІ) гідрооксидом.
4.5.1 Хід роботи: помістити в пробірку 2 краплі розчину сульфату міді, 2 краплі розчину їдкого натру і перемішати, в пробірку додати 1 краплю гліцерину і розбовтати.
4.5.2 Спостереження: з’являється темно-синє забарвлення.
4.5.3 Хімізм реакцій:


 Н2С – ОН HO – CH2 H2C – O O – CH2
Н2С – ОН HO – CH2 H2C – O O – CH2





 НС – ОН + НО – Cu – OH + HO – CH → HC – O → Cu ← O – CH + 2H2O
НС – ОН + НО – Cu – OH + HO – CH → HC – O → Cu ← O – CH + 2H2O
Н2С – ОН HO – CH2 HOH2C H H CH2OH
4.5.4  Висновок: кислотні властивості трьохатомного спирту більші ніж одноатомного, збільшення кількості гідроксильних груп підвищує кислотний характер.
Висновок: кислотні властивості трьохатомного спирту більші ніж одноатомного, збільшення кількості гідроксильних груп підвищує кислотний характер.
4.6 Отримання диетилового ефіру.
4.6.1 Хід роботи: в суху пробірку внести 2 краплі етилового спирту і 2 краплі сульфатної кислоти. Суміш обережно нагріти над полум’ям пальника до побуріння розчину. До гарячої суміші дуже обережно добавити ще 2 краплі етилового спирту.
4.6.2  Спостереження: відчувається характерний запах діетилового ефіру.
Спостереження: відчувається характерний запах діетилового ефіру.
4.6.3 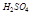 Хімізм реакцій: С2Н5ОН + НОС2Н5 → С2Н5 – О – С2Н5 + Н2O
Хімізм реакцій: С2Н5ОН + НОС2Н5 → С2Н5 – О – С2Н5 + Н2O
4.6.4 Висновок: відбувається міжмолекулярна дегідратація
4.7 Розчинення фенолу у воді.
4.7.1 Хід роботи: поміщають у пробірку 2 краплі рідкого фенолу, добавити 2 краплі води і збовтують. Дати суміші відстоятися. Пізніше суміш у пробірці розшаровується: верхній шар - розчин фенолу у воді, нижній - розчин води у фенолі. Обережно нагріти пробірку над пальником.
4.7.2 Спостереження: утворюється мутна вода. Рідина – емульсія фенолу.
4.7.3 Висновок: фенол погано розчиняється у холодній воді.
4.8 Одержання феноляту натрію.
4.8.1 Хід роботи: в пробірку поміщають 4 краплі емульсії фенолу у воді і добавляють 2 краплі розчину їдкого натрію. Швидко збовтують.
4.8.2 Спостереження: утворюється безбарвний розчин.
4.8.3 Хімізм реакцій: С6Н5 – ОН + NaOH → C6H5 – ONa + H2O
4.8.4 Висновок: феноли володіють кислотними властивостями.
4.9 Розклад феноляту натрію хлоридною кислотою.
4.9.1 Хід роботи: в пробірку поміщаємо 4 краплі фенолу у воді і добавляють 2 краплі розчину їдкого натрію, добавляють каплю розчину хлоридної кислоти.
4.9.2 Спостереження: виділяється вільний фенол у вигляді емульсії.
4.9.3 Хімізм реакцій: С6Н5 – ONa + HCl → C6H5 – OH + NaCl
4.9.4 Висновок: розчини фенолятів лужних металів володіють лужною реакцією.
4.10 Реакція фенолу з хлоридом заліза (ІІІ).
4.10.1 Хід роботи: в пробірку помістити 2 краплі розчину фенолу, добавити 3 краплі води і 1 краплю розчину хлориду заліза.
4.10.2 Спостереження: з’являється червоно-фіолетове забарвлення
4.10.3 Хімізм реакцій: С6Н5ОН + FeCl3 → C6H5OFeCl2 + HCl
4.10.4 Висновок: феноли з FrCl3 дають кольорову реакцію.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 731; Нарушение авторских прав?; Мы поможем в написании вашей работы!