
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные свойства р-элементов
|
|
|
|
Химия элементов этого семейства очень разнообразна. Р-элементы называют «типическими», они находятся в малых 2-ом и 3-ем периодах, а также в главных подгруппах больших периодов. Валентные электроны занимают внешний энергетический уровень и это существенно сказывается на физических и химических свойствах. В это семейство входят металлы, полуметаллы и неметаллы. Агрегатное состояние простых веществ тоже самое различное. Слева направо по периоду с ростом зарядов ядер и уменьшением атомных радиусов увеличиваются окислительные свойства элементов и их электроотрицательность. По подгруппам снизу вверх окислительные свойства и электроотрицательность тоже растут. Поэтому самым сильным окислителем является фтор (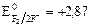 В). Значения электроотрицательности для ряда элементов р-семейства падают в следующем порядке:
В). Значения электроотрицательности для ряда элементов р-семейства падают в следующем порядке:
F, O, Cl, N, Br, J, C, S, H, P, As, B, Si, Sn, Pb, Al.
Восстановительные свойства этих же р-элементов в такой же закономерности возрастают.
Самые типичные неметаллы имеют:
а) молекулярные кристаллические решётки в твёрдом состоянии (при обычных условиях это газы, жидкости или твёрдые вещества с низкими температурами плавления) – F2, O2, P4, S8, Br2 и др.;
б) или атомные кристаллические решётки; поэтому они обладают большой твёрдостью и очень высокими температурами плавления – С, В, Si;
в) для многих элементов р-семейства характерна аллотропия.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 677; Нарушение авторских прав?; Мы поможем в написании вашей работы!