
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. 1. Н2О + Ме = основание (или оксид) + Н2
|
|
|
|
1. Н2О + Ме = основание (или оксид) + Н2
2К + 2Н2О = 2КОН + Н2;
 .
.
2. H2O + С1 2 = HCl + HСlO.
3. H2O + основной оксид = основание
H2O + СаО = Са(ОН)2.
4. H2O + кислотный оксид = кислота
H2O + SO3 = Н2SО4;
H2O + СО2 Û Н2СО3.
5. образует аквакомплексы
CuSО4 + 4H2O = [Cu(H2O)4] SО4.
6. разлагает многие бинарные соединения
К3N + 3Н2О = 3КОН + NН3;
Ca3P2 + 6Н2О = 3Ca(OH)2 + 2PН3;
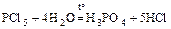 ;
;
LiH + Н2О = LiОН + Н2.
7. практически не диссоциирует
2Н2О Û Н3О+ + ОН- ( ).
).
8. разлагает некоторые соли (гидролиз идет до конца)
SbCl3 + H2O = SbOCl¯ + 2HCl.
9. перегретый водяной пар обладает особыми свойствами:
а) конверсия водяного газа
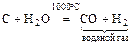 ;
;
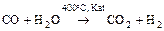 .
.
б) конверсия метана
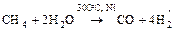 .
.
ВОДОРОД ПЕРОКСИД (перекись водорода; Н2О2)
Из-за несимметричного строения связей Н-О молекула сильно полярна, поэтому между молекулами Н2О2, как и между молекулами Н2О, существуют водородные связи и говорят не об единичных молекулах, а об ассоциатах (Н2О2)х.
Условно строение молекулы можно изобразить Н-О-О-Н; энергии связей различны: Есвязи О-О = 210 кДж/моль; Есвязи О-Н = 468 кДж/моль. Связь О-О более слабая и это сказывается на химических свойствах пероксида: Н2О2 хороший окислитель.
Благодаря возможности образования «кислородных мостиков» известны также надперекиси (ещё менее устойчивы, чем Н2О2): Н2О3 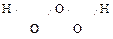 , Н2О4
, Н2О4 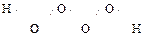 .
.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 646; Нарушение авторских прав?; Мы поможем в написании вашей работы!