
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ammoniae solutio concentrate
|
|
|
|
Ammonia solution, concentrated *
NH4OH
Властивості. Прозора безбарвна сильно лужна рідина. Змішується з нодою і 96 % спиртом.
Ідентифікація.
1. Відносна щільність від 0,892 до 0,910 (ДФУ).
2. Субстанція повинна мати сильно лужну реакцію (ДФУ).
3. Реакція на NH4+ (ДФУ):
Кількісне визначення. Ацидиметрія (зворотне титрування); (s = 1):

Надлишок розчину кислоти хлористоводневої відтитровують розчином натрію гідроксиду по метиловому червоному до переходу червоного забарвлення в жовте:
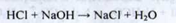
Аміаку розчин концентрований повинен містити не менше 25,0 % і не більше 30% (м / м) аміаку.
Зберігання. При температурі не вище 20 ° С в повітронепроникних контейнерах.
Лікарські засоби, що містять миш'як і вісмут
Миш'яковиста трьох окісь для гомеопатичного використання
Arsenii trioxidum ad praeparationes homeopathicae (Ph. Eur.)
Миш'яковистий ангідрид (Acidum arsenicosum anhydricum)
As2O3
Отримання. Шляхом випалу сірчистих руд в струмі повітря:
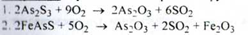
Властивості. Важкі білі склоподібні або фарфороподібні шматки часто слоїстої будови, з крейдовим зламом або важким білим порошком. Дуже повільно розчинний у воді (68-80 частинах), легко розчинний у розчинах HCI, NaOH, К2СО3, гліцерині:

Ідентифікація.
1) Субстанцію розчиняють у НСІ і додають 1-2 краплі розчину натрію сульфіду (Ph. Eur.):
 Жовтий осад або гель.
Жовтий осад або гель.
Осад розчинний у розчинах NH4OH, (NH4) 2СОз.
2) Субстанцію розчиняють у НСI, додають натрію гіпофосфіт і нагрівають (Ph. Eur.); Утворюється темно -коричневий осад:

3) До розчину субстанції в натрію гідроксиді, додають 1-2 краплі AgNO3, утворюється жовтий осад, розчинний у HN03 і NH4OH:

Кількісне визначення.
1. Йодометрія (Ph. Eur.) Субстанція титрується 0,05 М розчином йоду в присутності NaHCO3 (для зв'язування виділяється кислоти йодистоводородні і запобігання оборотності реакції), індикатор - крохмаль, (s = l / 2):
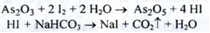
2. Броматометрія, пряме титрування з контрольним досвідом. Титрант КВrO3, індикатор - метиловий червоний. (s = 1.5).

У точці еквівалентності відбувається знебарвлення індикатора виділився бромом:

Застосування. Використовується зовнішньо у стоматології, дерматології і всередину при недокрів'ї, неврастенії.
Зберігання. У добре закупореній тарі.
Вісмуту нітрат основний
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 493; Нарушение авторских прав?; Мы поможем в написании вашей работы!