
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ртуть хлорид ( сулема ) ( Нуdrargyri dichloridum) ( ДФУ )
|
|
|
|
ZnO
Отримання.
1. Проколювання цинкового шпату:

2. Проколювання при 250 ° С свіжо осадженого цинку карбонату основного, одержуваного з цинку сульфату за реакцією:
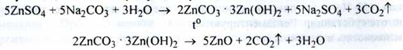
Властивості. М'який аморфний порошок білого кольору або білого зі злегка жовтуватим відтінком, вільний від піщаних частинок. Практично не розчинний у воді і 96 % спирті. (Розчиняється в розведених мінеральних кислотах).
Ідентифікація.
1. Субстанція жовтіє при сильному нагріванні; жовтий колір зникає при охолодженні (ДФУ).
2. Проводять реакції на цинк (а, в) після розчинення у кислоті хлористоводневої розведеної (ДФУ):

3. Реакція освіти зелені Рінмана. Окись цинку прожарюється з кобальта нітрату, при цьому виходить характерне зелене забарвлення - зелень Рінмана:
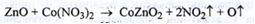
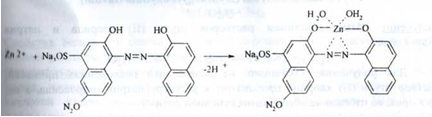
Кількісне визначення. Комплексонометрія після розчинення субстанції в кислоті оцтової, у присутності індикатора ксиленового помаранчевого і гексаметилентетраміну, (s = 1), (ДФУ):
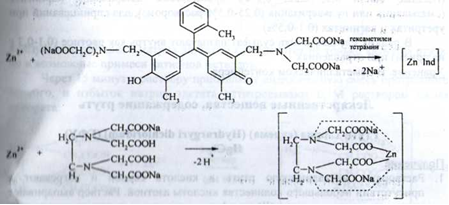
В точці еквівалентності:
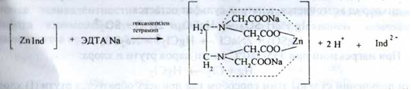
Застосування. Зовнішньо у вигляді присипок, мазей, паст, як в’яжучу, підсушуючуі дезінфікуючий засіб при шкірних захворюваннях.
Зберігання. Так як цинк оксид поглинає вуглекислоту повітря і перетворюється в основний карбонат цинку, його слід зберігати в добре закупореній тарі.
Цинк сульфат гептагідрат (Zinci sulfas heptahydricus) (ДФУ)
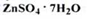
Отримання. Дією кислоти сірчаної розведеної на металевий цинк або цинк оксид: 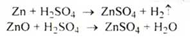
Властивості. Кристалічний порошок білого кольору або безбарвні прозорі кристали, що вивітрюються на повітрі. Дуже легко розчинний у воді, практично не розчинний у 96 % спирті.
Ідентифікація субстанції проводиться реакціями на цинк- іон, зазначеними для цинку оксиду. Сульфат - іон визначається з освіти білого осаду після додавання до розчину субстанції барію хлориду (ДФУ).
Кількісне визначення. Комплексонометрія; (s = 1) (ДФУ).
Застосування. Антисептичний і в’яжучий засіб при кон'юнктивітах (очні краплі 0,1; 0,25; 0,5 %), хронічному катаральному ларингіті (змазування або пульверизації (0,25-0,5 % розчином)), для спринцювань при уретритах і вагінітах (0,1-0,5 %).
У рідкісних випадках цинку сульфат призначають внутрішньо як блювотний (0,1-0,3 г на прийом) при отруєннях.
Зберігання. У неметалічному контейнері.
Лікарські речовини, що містять ртуть
HgCl2
Отримання.
1. Розчиняють металеву ртуть в кислоті сірчаній і нагрівають у присутності невеликої кількості кислоти азотної. Розчин випарюють досуху, а залишок - ртуті (II) сульфат - змішують з натрієхм хлоридом і невеликою кількістю марганцю пероксиду і знову нагрівають. Ртуті дихлорид переганяється, а натрію сульфат залишається:
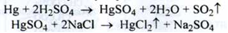
2. При нагріванні при 335-340 ° С суміші парів ртуті і хлору:

При отриманні сулеми цим способом як домішка утворюється ртуті (I) хлорид (Hg2Cl2). Для очищення отриманої сулеми від ртуті (I) хлориду її піддають сублімації, а потім кристалізують із спирту або води, в яких ртуті (I) хлорид не розчинний.
Властивості. Кристалічний порошок білого кольору або білі, або безбарвні кристали, або важка кристалічна маса. Розчинний у воді, ефірі і гліцерині, легко розчинний в 96 % спирті.
Ідентифікація.
1. Проводять реакції на хлориди (ДФУ).
2. Проводять реакції на катіон ртуті (а, b. с) (ДФУ).
Випробування на чистоту. Визначають наявність домішки ртуті (I) хлориду по розчинності в ефірі (розчин субстанції в ефірі не повинен мутніть)
Кількісне визначення.
1. Комплексонометрія, зворотне титрування, індикатор - уїдливий чорний, (s=1), перерахунок на суху речовину (ДФУ):
До субстанції додають надлишок натрію едетат у присутності буферного розчину pH 10,9:
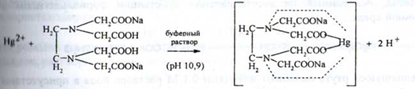
в результаті реакції з натрію едетат зв'язуються не тільки катіони ртуті, а й можливі домішки катіонів металів.
Через 15 хвилин до розчину додають індикаторну суміш протравного чорного, і надлишок натрію едетат відтитровують 0,1 М розчином цинку сульфату:

в точці еквівалентності надлишкова крапля титрування розчину цинку сульфата взаємодіє з індикатором з утворенням комплексу, пофарбованого в пурпуровий колір.
До реакційної суміші додають надлишок калію йодиду:

Виділився натрія едетат (у кількості, еквівалентній катіону ртуті) відтитровують розчином цинку сульфату (див. хімізм реакції б)).
Для розрахунку кількісного вмісту використовують об'єм цинку сульфату в останньому титруванні.
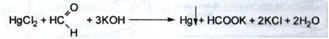
2. Метод, заснований на відновленні субстанції формальдегідом в лужному середовищі:
Виділилася ртуть окислюють надлишком 0,1 М розчину йоду в присутності калію йодиду:
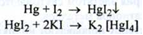
Надлишок йоду відтитровують розчином натрію тіосульфату; (s = 1):

Застосування. Антисептичний засіб, але має високу токсичність. При роботі з ним необхідно дотримуватися великої обережності.
Не слід допускати попадання препарату та його розчинів у порожнину рота, на слизові оболонки і шкіру; розчини можуть всмоктуватися й викликати отруєння.
Застосовують ртуті (II) хлорид в розчинах (1:1000-2:1000) для дезінфекції білизни, одягу, для обмивання стін, предметів догляду за хворими. Вживають також при лікуванні шкірних захворювань.
Таблетки і розчини сулеми підфарбовують еозином.
Зберігання. У захищеному від світла місці.
Ртуті оксид жовтий (Hydrargyri oxydum flavum)
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 1085; Нарушение авторских прав?; Мы поможем в написании вашей работы!