
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Адсорбция газов и паров на однородной поверхности твердого тела
С термодинамической точки зрения адсорбция является самопроизвольным процессом выравнивания химических потенциалов веществ в объеме системы и межфазном (поверхностном) слое. Этот процесс происходит вследствие стремления поверхностной энергии к минимуму или энергии Гиббса всей системы. К явлениям, происходящим вследствие стремления к самопроизвольному снижению поверхностного натяжения, относится адсорбция.
Адсорбцию можно рассматривать как взаимодействие молекул адсорбата с активными центрами поверхности адсорбента. Адсорбция может проходить в многокомпонентных системах. В поверхностный слой предпочтительнее переходит тот компонент, который сильнее уменьшает поверхностное и межфазное натяжение.
Возможны следующие варианты адсорбционных процессов: адсорбцию газов на твердых адсорбентах, адсорбцию растворенного вещества на границах твердое тело-жидкость, на границе жидкость – жидкость, а также адсорбцию на границе жидкий раствор – газ.
Характеристикой величины адсорбции является отношение избытка вещества в поверхностном слое определенной толщины к его количеству в таком же объеме фазы, отнесенному к единице площади поверхности. Эту величину называют гиббсовской адсорбцией и обозначают буквой гамма Г.
Различают физическую (молекулярную) адсорбцию, хемосорбцию (химическое присоединение атома, молекулы) и ионный обмен.
Адсорбция может происходить не только благодаря уменьшению поверхностной энергии. Она может быть результатом химического взаимодействия компонента с поверхностью вещества (хемосорбция), и тогда поверхностная энергия может возрастать на фоне уменьшения энергии всей системы. При химической адсорбции между адсорбатом и адсорбентом образуется химическая связь, и они теряют свою индивидуальность.
Стремление гетерогенной системы к минимуму поверхностной энергии вызывает определенное ориентирование полярных молекул, ионов и электронов в поверхностном слое, вследствие чего соприкасающиеся фазы приобретают заряды противоположного знака, но равной величины (ионный обмен). В результате на поверхности возникает двойной электрический слой. Различают три механизма образования двойного электрического слоя. Согласно одному из них двойной электрический слой образуется в результате перехода ионов или электронов из одной фазы в другую (поверхностная ионизация). Например с поверхности металла в газовую фазу (термоэлектронная эмиссия). Возникшая разность потенциалов на межфазной границе препятствует дальнейшему переходу электронов, наступает равновесие, образуется двойной электрический слой: положительно заряженная поверхность металла – отрицательно заряженное электронное облако. Возможен механизм преимущественного перехода ионов того или иного знака с поверхности вещества в раствор. Двойной электрический слой образуется также в результате ориентирования полярных молекул сопряженных фаз благодаря их взаимодействию. Двойной электрический слой появляется в случае неполярных молекул, способных поляризоваться в силовом поле межфазной границы. Двойной электрический слой образуется и в результате адсорбции.
При физической адсорбции взаимодействие адсорбата и адсорбента происходит за счет Ван-дер-Вальсовских сил и водородных связей. Силы взаимодействия между неполярными молекулами возникают за счет флуктуаций электронной плотности в соседних частицах. Возможен резонанс таких взаимодействий, который приводит к уменьшению энергии системы, что и приводит к притяжению частиц.
Межмолекулярное взаимодействие усиливается, при наличии у молекул постоянных диполей (диполь-дипольный эффект, ориентационный эффект). При взаимодействии между полярной и неполярной молекулами возникает индукционный эффект. Индукционные силы способствуют усилению притяжения. Этот фактор тем сильнее, чем больше поляризуемость молекул.
Характерно, что для всех составляющих сил В-д-В справедлив один и тот же закон изменения энергии притяжения от расстояния:
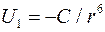 ,
,
где С - константа, которая рассчитывается отдельно для каждого эффекта.
На очень близких расстояниях возникают силы отталкивания, обусловленные перекрыванием электронных оболочек. Энергию данного эффекта описывает эмпирическая формула:
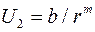 ,
,
где b и m -константы, подбираемые опытным путем.
Как правило, m =12. Полную потенциальную энергию взаимодействия двух атомов (молекул) записывают в виде уравнения Леннарда – Джонса:
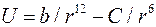 . (3)
. (3)
При адсорбции происходит взаимодействия молекулы адсорбата с большим количеством молекул адсорбента, лежащих на поверхности. Поэтому формула для энергии их взаимодействия отличается от выражения (3). Чтобы рассчитать энергию взаимодействия при адсорбции, необходимо просуммировать энергию взаимодействия адсорбирующегося атома с каждым атомом адсорбента. В результате получена формула:
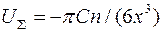 , (4)
, (4)
где x - расстояние от атома адсорбата до поверхности адсорбента.
Такая зависимость от x указывает на дальнодействие адсорбционных сил. Полную потенциальную энергию взаимодействия при адсорбции можно выразить уравнением:
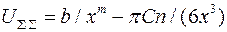 . (5)
. (5)
Из рассмотрения природа адсорбционного взаимодействия вытекает практически важный вывод о том, что адсорбционное взаимодействие будет более эффективным при наличии на поверхности адсорбента микротрещин и пор. В этом случае атом адсорбата окружает большое количество молекул твердого тела.
Если же в адсорбционное взаимодействие основной вкдлад вносят электростатические силы, то в микротрещинах и порах наибольший потенциал оказывается на выступах, где и будет преобладать адсорбция, особенно при образовании водородных связей (адсорбция воды).
|
|
Дата добавления: 2015-06-25; Просмотров: 1393; Нарушение авторских прав?; Мы поможем в написании вашей работы!