
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение констант диссоциации слабых кислот путем измерения рН растворов
|
|
|
|
 Необходимые материалы и оборудование:
Необходимые материалы и оборудование:
- растворы слабых кислот, концентрации I моль/л (уксусная, муравьиная, пропионовая, щавелевая, фосфорная и др.),
- стаканы на 50 и 100 мл,
- мерные колбы на 50 мл,
- пипетка на 10 мл,
- мерный цилиндр на 25 мл,
- электролитический ключ,
- платиновый электрод,
- хлорсеребрянный (или каломельный) электрод,
- хингидрон,
- дистиллированная вода,
- потенциометр Р-307 с нормальным элементом Вестона,
батареей сухих элементов, гальванометром. –
Из исходного раствора слабой кислоты (указывается преподавателем) с концентрацией 1,0 моль/л путем последовательного разведения готовят растворы следующих концентраций, (моль/л): 0,5, О,1, 0,05, 0,01, 0,005, 0,001. Объем раствора должен быть не менее 25 мл и не более 50 мл,
В стаканчик на 50 мл налить 25 мл приготовленного раствора кислоты, добавить хингидрон. Раствор тщательно перемешать стеклянной палочкой. Хингидрона добавляют столько, чтобы образовался насыщенный раствор. Опускают в стаканчик платиновый и хлорсеребрянный электроды и измеряют ЭДС полученного гальванического элемента. По величине ЭЬДС рассчитывают рН раствора.
Такие же измерения проводят со всеми приготовленными растворами.
Полученные результаты сводят в таблицу
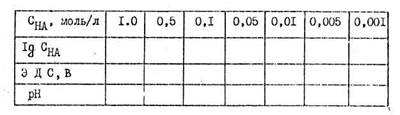
На основе опытных данных построить график в координатах рН = рН(IgСША) и определить константу диссоциации слабой кислоты. Сравнить значение константы диссоциации, найденное из опытных данных, со справочным значением.
РАБОТА 3
|
|
|
|
|
Дата добавления: 2015-06-25; Просмотров: 368; Нарушение авторских прав?; Мы поможем в написании вашей работы!