
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Молекулярная физика и термодинамика. Формула Название формулы Расшифровка обозначений Количество вещества
|
|
|
|
| Формула | Название формулы | Расшифровка обозначений | |
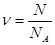 
| Количество вещества | 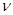 – количество вещества; N – число атомов (или молекул) в данном теле; NA– постоянная Авогадро – количество вещества; N – число атомов (или молекул) в данном теле; NA– постоянная Авогадро
| |
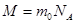
| Молярная масса | М – молярная масса; т0 – масса атома (или молекулы); nA – постоянная Авогадро. | |
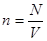
| Концентрация атомов (или молекул) | п – концентрация атомов (или молекул); N – число атомов (или молекул) в данном теле; V– объём тела; | |
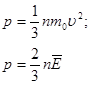
| Основное уравнение молеку–лярно–кинетической теории | p – давление газа; п – концентрация атомов (или молекул); т0 – масса атома (или молекулы); 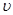 – средняя
квадратичная скорость атомов или молекул; – средняя
квадратичная скорость атомов или молекул; 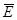 – средняя кинетическая энергия поступательного движения атомов (или молекул) – средняя кинетическая энергия поступательного движения атомов (или молекул)
| |
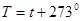
| Связь абсолютной температуры с температурой в °С. | Т – абсолютная температура; t – температура по шкале Цельсия | |
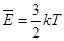
| Средняя кинетическая энергия поступательного движения молекул | 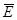 – средняя кинетическая энергия поступательного движения молекул; k – постоянная Больцмана; Т – абсолютная температура. – средняя кинетическая энергия поступательного движения молекул; k – постоянная Больцмана; Т – абсолютная температура.
| |
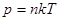
| Давление газа | р – давление газа; п – концентрация атомов (или молекул); k – постоянная Больцмана; Т – абсолютная температура. | |
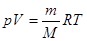
| Уравнение состояния идеального газа | р – давление газа; V – объём газа; т – масса газа; М – молярная масса; R – универсальная газовая постоянная; Т – абсолютная температура. | |
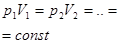
| Закон Бойля–Мариотта (изотермический процесс) | 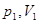 – давление и объём газа в первом состоянии, – давление и объём газа в первом состоянии, 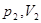 – давление и объём того же газа во втором состоянии – давление и объём того же газа во втором состоянии
| |
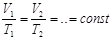
| Закон Гей–Люссака (Изобарный процесс) | 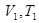 –объём и температура газа в первом состоянии; –объём и температура газа в первом состоянии; 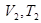 –объём и температура того же газа во втором состоянии. –объём и температура того же газа во втором состоянии.
| |
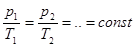
| Закон Шарля (Изохорный процесс) | 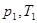 – давление и температура газа в первом состоянии; – давление и температура газа в первом состоянии; 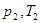 – давление и температура того же газа во втором состоянии; – давление и температура того же газа во втором состоянии;
| |
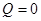
| Адиабатный процесс | Q – количество теплоты, отданное или полученное термодинамической системой | |
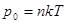
| Давление насыщенного пара | p0 – давление насыщенного пара; п – концентрация атомов (или молекул); – постоянная Больцмана; Т – абсолютная температура. | |
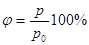
| Влажность воздуха | 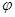 – относительная влажность воздуха; р – парциальное давление водяных паров в воздухе; р0 – давление насыщенного водяного пара при данной температуре. – относительная влажность воздуха; р – парциальное давление водяных паров в воздухе; р0 – давление насыщенного водяного пара при данной температуре.
| |
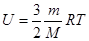
| Внутренняя энергия идеального одноатомного газа | U – внутренняя энергия идеального одноатомного газа; m –масса газа; M – молярная масса; R – универсальная газовая постоянная; Т – абсолютная температура. | |
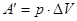
| Работа гази при изобарном процессе | А' – работа газа; р – давление газа; Δ V – изменение объёма газа. | |
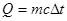
| Количество теплоты для нагревания | Q – количество теплоты для нагревания; т – масса тела; с – удельная теплоемкость; Δ t – изменение температуры. | |
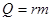
| Количество теплоты для испарения | Q – количество теплоты для испарения; т – масса тела; r – удельная теплота парообразования | |
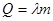
| Количество теплоты для плавления | Q – количество теплоты для плавления; т – масса тела; λ – удельная теплота плавления. | |
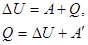
| Первый закон термодинамики | ΔU – изменение внутренней энергии; А – работа внешних сил; Q – количество теплоты; А' – работа газа. | |
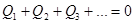
| Уравнение теплового баланса | Q1,Q2,Q3 – количества теплоты, которыми обмениваются тела замкнутой системы. | |
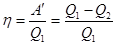
| Коэффициент полезного действия теплового двигателя | 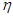 – коэффициент полезного действия теплового двигателя; А' – работа, совершённая двигателем; Q1 – количество теплоты, полученное от нагревателя; Q2 – количество теплоты, отданное холодильнику – коэффициент полезного действия теплового двигателя; А' – работа, совершённая двигателем; Q1 – количество теплоты, полученное от нагревателя; Q2 – количество теплоты, отданное холодильнику
| |
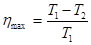
| Коэффициент полезного действия идеального теплового двигателя.(Цикл Карно) | 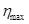 – коэффициент полезного действия идеального теплового двигателя; T1 – температура нагревателя; Т2 – температура холодильника – коэффициент полезного действия идеального теплового двигателя; T1 – температура нагревателя; Т2 – температура холодильника
| |
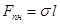
| Сила поверхностного натяжения | Fпн – сила поверхностного натяжения; 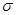 – коэффициент поверхностного натяжения (удельная поверхностная энергия); l – длина границы поверхности, на которую действует сила поверхностного натяжения. – коэффициент поверхностного натяжения (удельная поверхностная энергия); l – длина границы поверхности, на которую действует сила поверхностного натяжения.
| |
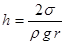
| Высота подъёма жидкости в капилляре | h – высота подъёма смачивающей жидкости в капилляре; 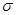 – коэффициент поверхностного натяжения жидкости; – коэффициент поверхностного натяжения жидкости; 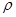 – плотность жидкости; g – ускорение свободного падения; r – радиус капилляра. – плотность жидкости; g – ускорение свободного падения; r – радиус капилляра.
|
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 855; Нарушение авторских прав?; Мы поможем в написании вашей работы!